Vol. 22 - Num. 85
Casos clínicos en Digestivo
Dilatación gástrica misteriosa
Sandra Llorente Pelayoa, Jesús Ramírez Berriosb, Iván Carabaño Aguadoc, Constanza Liébana de Rojasd, Elisa Fernández Cookee, Enrique Salcedo Lobatoc, Enrique Medina Benítezc
aServicio de Pediatría. Hospital Universitario Marqués de Valdecilla. Santander. España.
bSección de Gastroenterología, Hepatología y Nutrición Infantil. Servicio de Pediatría. Hospital Universitario 12 de Octubre. Madrid. España.
cSección de Gastroenterología, Hepatología y Nutrición Pediátrica. Servicio de Pediatría. Hospital Universitario 12 de Octubre. Madrid. España.
dSección de Radiodiagnóstico Infantil. Hospital Universitario 12 de Octubre. Madrid. España.
eSección de Infectología. Servicio de Pediatría. Hospital Universitario 12 de Octubre. Madrid. España.
Correspondencia: S Llorente. Correo electrónico: sandrallorentepelayo@gmail.com
Cómo citar este artículo: Llorente Pelayo S, Ramírez Berrios J, Carabaño Aguado I, Liébana de Rojas C, Fernández Cooke E, Salcedo Lobato E, et al. Dilatación gástrica misteriosa . Rev Pediatr Aten Primaria. 2020;22:67-71.
Publicado en Internet: 10-03-2020 - Número de visitas: 15037
Resumen
La ascaridiasis es una de las parasitosis más comunes a nivel mundial. Es especialmente frecuente en países tropicales subdesarrollados, en los que las condiciones higiénicas y socioeconómicas favorecen la transmisión. El ciclo del parásito es entérico-neumoentérico y se inicia con la ingesta oral de huevos de este. La infestación puede ser asintomática o producir clínica gastrointestinal o respiratoria durante su paso pulmonar (neumonitis eosinofílica y síndrome de Loeffler). Durante la fase intestinal puede producir diarrea leve intermitente, dolor abdominal, náuseas y vómitos. En raras ocasiones aparece obstrucción intestinal, apendicitis aguda, invaginación, colecistitis, pancreatitis, absceso hepático o peritonitis. Se presenta un caso que cursó, de manera atípica, con una dilatación gástrica muy marcada.
Palabras clave
● Ascaris ● Dilatación gástrica ● ParásitosINTRODUCCIÓN
La ascaridiasis es una de las parasitosis más comunes a nivel mundial. Es especialmente frecuente en países tropicales subdesarrollados, en los que las condiciones higiénicas y socioeconómicas favorecen la transmisión1.
El ciclo del parásito es entérico-neumoentérico, y se inicia con la ingesta oral de huevos de este. Las larvas eclosionan en el intestino delgado y atraviesan la mucosa para llegar a la circulación portal. Pasan a través del hígado y acceden posteriormente a los pulmones, desde donde, mediante la tos y la deglución, son reingeridos y alcanzan de nuevo el intestino delgado, ya en su forma adulta. Habitualmente viven en el intestino delgado 1-2 años, durante los cuales sus huevos se eliminan en las heces. Finalmente mueren y son expulsados espontáneamente1-3.
La infestación puede ser asintomática o producir clínica gastrointestinal o respiratoria durante su paso pulmonar (neumonitis eosinofílica y síndrome de Loeffler). Durante la fase intestinal puede producir diarrea leve intermitente, dolor abdominal, náuseas y vómitos. En raras ocasiones aparece obstrucción intestinal, apendicitis aguda, invaginación, colecistitis, pancreatitis, absceso hepático o peritonitis1-3. En los pacientes con clínica gastrointestinal, el diagnóstico se basa en estudios radiológicos y el hallazgo del parásito o sus huevos en heces o secreciones gástricas. Es frecuente la presencia de eosinofilia en sangre periférica. El tratamiento es con antiparasitarios como mebendazol o albendazol4.
Debe sospecharse la infestación por áscaris en los pacientes pediátricos que se presentan con cuadros oclusivos o suboclusivos abdominales especialmente cuando existe el antecedente epidemiológico de viaje al trópico5,6.
A continuación, se expone un caso clínico en el cual, de manera atípica, la expresión de la infestación fue la combinación de dolor abdominal y vómitos intermitentes, en relación con una dilatación gástrica muy marcada.
CASO CLÍNICO
Niña de siete años sin antecedentes personales relevantes, salvo por un viaje a Senegal con su familia hace un año. Presenta en los últimos seis meses episodios recurrentes (tres en total) de marcada distensión abdominal, con vómitos alimentarios y deposiciones escasas líquidas. En este contexto, ha precisado en dos ocasiones colocación de sonda nasogástrica para descompresión por sospecha clínico-radiológica de cuadro suboclusivo, con buena respuesta. Asintomática entre episodios, salvo cierta tendencia al estreñimiento (deposiciones Bristol 1-2 cada 48 horas). Balance ponderoestatural ascendente. El último de los episodios motiva su ingreso para estudio.
En la exploración física presenta un buen estado de nutrición, con un abdomen marcadamente distendido, timpánico, sin masas ni megalias, no doloroso a la palpación. Se realiza inicialmente radiografía simple de abdomen (Fig. 1), que muestra marcada distensión gástrica y abundante gas en todo el tracto gastrointestinal. Se realiza analítica con hemograma en el que únicamente destaca eosinofilia leve (700 eosinófilos/mm3); bioquímica con perfil hepatorrenal, amilasa y proteína C reactiva normales, hormonas tiroideas y anticuerpos antitransglutaminasa negativos. Estudio de heces con coprocultivo, virus enteropatógenos, toxina de C. difficile y parásitos negativos. Se realiza tránsito baritado (Fig. 2), que muestra marcada distensión gástrica y abundante gas intestinal, con poca motilidad gástrica y paso rápido de contraste a duodeno, sin datos de obstrucción ni vólvulo gástrico. Se completa con una ecografía abdominal sin hallazgos significativos. Tras la realización del tránsito presenta de nuevo importante distensión (Fig. 3), que precisa la recolocación de la sonda nasogástrica. Se produce mejoría clínica tras la descompresión. Se cita en consultas externas para completar el estudio. Se plantea en aquel momento la realización de endoscopia o manometría antroduodenal, para valoración de trastornos de motilidad y la realización de nuevos estudios de imagen como enterorresonancia magnética o incluso laparoscopia exploradora para descartar causa anatómica (vólvulo gástrico intermitente, etc.). El enigma se resuelve a los tres días del alta, tras la expulsión en el contexto de un vómito de un helminto no plano, de 30 cm de longitud, compatible con Ascaris lumbricoides (Fig. 4). Tras la expulsión del nemátodo y la administración de tratamiento con mebendazol oral, presenta buena evolución, manteniéndose asintomática hasta la actualidad.
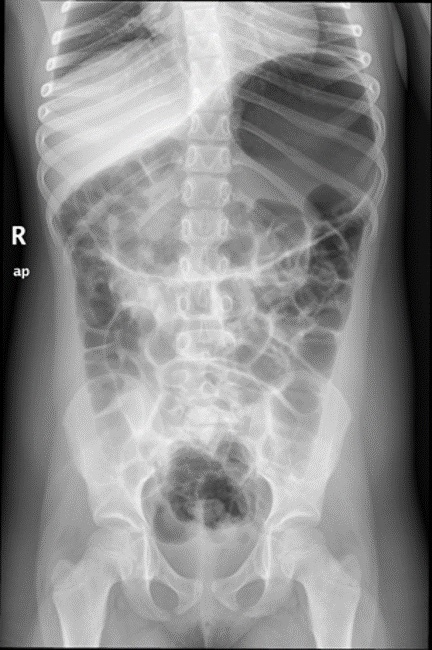
| Figura 1. Radiografía simple de abdomen que muestra una distensión gástrica llamativa y abundante gas en todo el tracto gastrointestinal |
|---|
 |

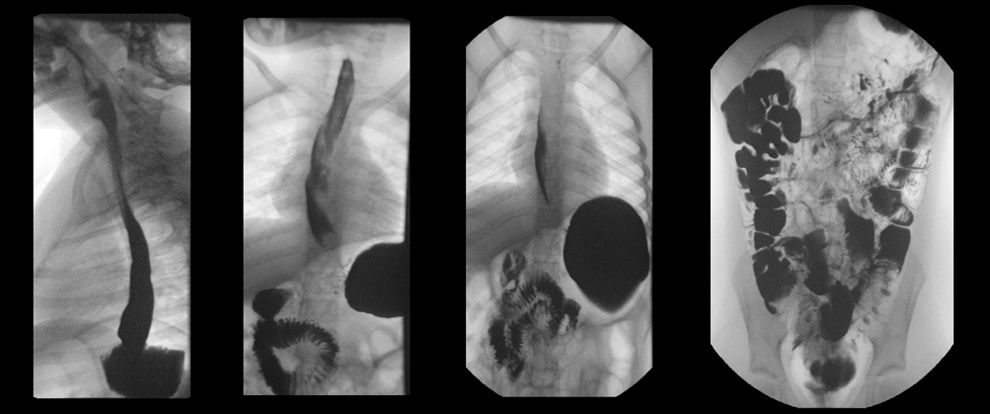
| Figura 2. Tránsito baritado que muestra distensión e hipomotilidad gástrica con paso rápido de contraste a duodeno, sin datos de obstrucción a ningún nivel |
|---|
 |

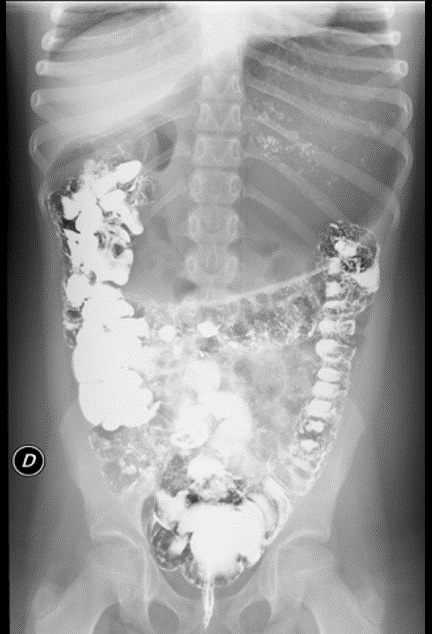
| Figura 3. Radiografía simple de abdomen realizada unas horas tras el tránsito baritado que muestra una distensión gástrica muy marcada |
|---|
 |

DISCUSIÓN
Aunque la mayoría de las infecciones por Ascaris son paucisintomáticas, ocasionalmente se producen complicaciones, de las que la obstrucción intestinal es la más frecuente. El pico de incidencia de las complicaciones anatómicas ocurre entre los dos y los cinco años de edad. Los mecanismos implicados en la obstrucción son la presencia física de parásitos que ocluyen la luz, la inflamación local y el espasmo muscular7. Además, los parásitos pueden actuar como punto fijo que favorece la volvulación o la invaginación. Aunque la obstrucción aguda es la forma clásica, la presentación subaguda es relativamente frecuente, suponiendo hasta el 73% de los casos de obstrucción por Ascaris8,9. En los casos subagudos, los pacientes se presentan con dolor abdominal, vómitos y diarrea o estreñimiento y habitualmente responden a tratamiento médico con antiparasitarios y medidas de soporte, sin precisar abordaje quirúrgico, a diferencia de los casos agudos8,9.
La paciente de nuestro caso manifestaba una importante distensión y alteración de la motilidad gástrica, que hizo plantear la realización de una gastroscopia y un estudio manométrico tras la normalidad de los primeros estudios complementarios.
Los trastornos motores gástricos pueden ser idiopáticos o secundarios a procesos neuropáticos o miopáticos, alteraciones congénitas, trastornos endocrinológicos y metabólicos, medicamentos, infecciones o enfermedades sistémicas (enfermedades del tejido conectivo, fibrosis quística, enfermedades genitourinarias, enfermedad celíaca, enfermedad inflamatoria intestinal, etc.)10. Todos ellos fueron tenidos en cuenta en el plano teórico, y se planteó el estudio manométrico-funcional como una segunda fase de estudio.
Aunque la mayoría de los casos de obstrucción se dan en pacientes con infestación masiva, en los que el bolo de parásitos obstruye la luz, se postula que la simple presencia del gusano puede generar toxinas y productos de desecho que ocasionan trastornos de la motilidad como espasmo muscular o hiperperistaltismo7,11,12, que pueden condicionar pesudooclusión.
Este caso es de interés por su inusual forma de presentación, como cuadros suboclusivos recurrentes, y supone un reto diagnóstico debido a la negatividad de las pruebas complementarias iniciales. Habitualmente, el diagnóstico de las parasitosis intestinales se realiza por examen microscópico de heces, identificando las formas parasitarias que se eliminan; sin embargo, aunque son pruebas específicas, su sensibilidad es pobre, ya que solo permiten el diagnóstico de la infección aguda y patente13. Cuando los helmintos están en fase de larva adulta tardía, pueden no eliminar huevos en heces, hecho que dificulta el diagnóstico. En estos casos pueden emplearse técnicas moleculares específicas, que aumentan la sensibilidad13.
Respecto a las pruebas de imagen, en ocasiones la radiografía simple, el tránsito baritado o la ultrasonografía permiten la identificación del parásito. En niños con infestaciones masivas, la radiografía puede mostrar una masa radiolucente con el típico patrón en remolino y también pueden ser identificables mediante ecografía como múltiples líneas ecogénicas o un pseudotumor6. Estas pruebas en el caso de formas larvarias únicas son menos rentables y requieren un alto índice de sospecha.
Como reflexión final, consideramos que es importante conocer las formas de presentación atípicas de las parasitosis intestinales, para obtener un diagnóstico más precoz, especialmente en aquellos pacientes con antecedentes epidemiológicos sugestivos.
CONFLICTO DE INTERESES
Los autores declaran no presentar conflictos de intereses en relación con la preparación y publicación de este artículo.
BIBLIOGRAFÍA
- Mellado MJ, García-Hortelano M, Cilleruelo MJ. Otras parasitosis importadas. An Pediatr Contin. 2005;3:229-38.
- Maldonado J, Romero J, López MA. Parasitosis intestinales. Tratamiento en gastroenterología, hepatología y nutrición pediátrica de la SEGHNP. Cuarta edición. Madrid: Ergon; 2016. p. 211-225.
- Martínez-Valverde A, Sierra-Salinas. Parasitosis Intestinales. En: Cruz. Tratado de Pediatría. Madrid: Ergon; 2016. p. 27.
- Legesse M, Erko B, Medhin G. Comparative efficacy of albendazole and three brands of mebendazole in the treatment of ascariasis and trichuriasis. East Afr Med J. 2004;81:134.
- Vilamizar E, Mendez M, Bonilla E, Varon H, de Onatra S. Ascaris lumbricoides infestation as a cause of intestinal obstruction in children: Experience with 87 cases. J Pediatr Surg. 1996;31:201-5.
- Mishra PK, Agrawal A, Joshi M, Sanghvi B, Shah H, Parelkar SV. Intestinal obstruction in children due to Ascariasis: A tertiary health centre experience. Afr J Paediatr Surg. 2008;5:65-70.
- Louw JH. Abdominal complications of Ascaris lumhricoides infestation in children. Br J Surg. 1966;53:510-21.
- Villamizar E, Méndez M, Bonilla E, Varon H, de Onatra S. Ascaris lumbricoides infestation as a cause of intestinal obstruction in children: experience with 87 cases. J Pediatr Surg. 1996;31:201-4.
- Wasadikar P, Kulkarni B. Intestinal obstruction due to ascariasis. Br J Surg. 1997;84:410-2.
- Sánchez C, Tolín MM, Bautista A. Trastornos motores esofágicos y gástricos. Tratamiento en gastroenterología, hepatología y nutrición pediátrica de la SEGHNP. 4.ª edición. Madrid: Ergon; 2016. p. 83-97.
- Bhandari PS, Garcha PS. Helmilthic gut obstruction (a case report). Med J Armed Forces India. 1998;54:165-6.
- Kumar M, Varier PS, Ramachandran P. Intestinal obstuction and gangrenous necrosis due to ascariasis. Ind J Surg. 1973;35:54-5.
- Fuentes I, Gutiérrez MJ, Gárate T. Diagnóstico de las parasitosis intestinales mediante detección de coproantígenos. Enferm Infecc Microbiol Clin. 2010;28:33-9.
Comentarios
Este artículo aún no tiene comentarios.






