Dolor precordial con esfuerzo físico causado por una miocarditis aguda
Francisco J. Rubio Péreza, Luis Franco Bonafonteb, Josep María Alegret Coloméc, Rosa María Collell Hernándezd
aUnitat Medicina de l’Esport. Hospital Universitario Sant Joan. Reus. Unitat Medicina de l’Esport, Hospital Comarcal. Amposta. Centre de Tecnificació Esportiva de les Terres de l’Ebre. Generalitat de Catalunya. Tarragona. España.
bUnitat Medicina de l’Esport. Hospital Universitario Sant Joan. Reus. Tarragona. España.
cServicio de Cardiología. Hospital Universitario Sant Joan. Reus. Tarragona. España.
dServicio de Pediatría. Hospital Universitario Sant Joan. Reus. Tarragona. España.
Correspondencia: FJ Rubio. Correo electrónico: fjrubio@grupsagessa.com
Cómo citar este artículo: Rubio Pérez FJ, Franco Bonafonte L, Alegret Colomé JP, Collell Hernández RM. Dolor precordial con esfuerzo físico causado por una miocarditis aguda. Rev Pediatr Aten Primaria. 2016;69:e5-e10.
Publicado en Internet: 28-03-2016 - Número de visitas: 12800
Resumen
Deportista de 15 años que acude a Urgencias por presentar durante un entrenamiento dolor torácico opresivo irradiado a brazo izquierdo de una hora de evolución, acompañado de náuseas y mareo. Pruebas complementarias: ECG: elevación del segmento ST en la cara diafragmática y infradesnivelación en cara lateral; CK 3312 UI/l, troponina T 9,12 µg/l, GOT 408 UI/l. Ecocardiograma y radiografía de tórax normales.
Ante la sospecha de isquemia es derivada a un centro especializado. El diagnóstico final fue de miocarditis aguda, con serología positiva para Mycoplasma pneumoniae. Se detallan los datos clínicos y evolución. Se permite el deporte de competición, aconsejándose controles cardiológicos semestrales, permaneciendo la paciente asintomática hasta la fecha.
Palabras clave
● Electrocardiograma ● Miocarditis ● Muerte súbita ● Resonancia magnéticaCASO CLÍNICO
Enfermedad actual
Jugadora de baloncesto de 15 años que en los dos últimos días presenta dolor torácico opresivo irradiado a brazo izquierdo de aproximadamente 15 minutos de evolución, siempre en reposo, acompañado de náuseas y sensación de mareo; le han administrado ibuprofeno con cierta mejoría del dolor. Acude al Servicio de Urgencias por presentar durante un entrenamiento dolor de características similares al descrito que se ha iniciado hace una hora y aún persiste, acompañado de náuseas y mareo, que no se modifica con la respiración ni los cambios posturales.
No refiere contusión ni fiebre previa. La deportista había realizado meses antes la revisión médico-deportiva, siendo dada apta para el deporte de competición. Asintomática con esfuerzo hasta el día de hoy.
Antecedentes personales sin interés. Antecedentes familiares: abuelo y bisabuelo maternos fallecidos por cardiopatía isquémica.
Exploración física: buen estado general, afebril. Corazón rítmico sin soplos. Murmullo vesicular conservado, pulsos periféricos presentes y simétricos, abdomen normal, neurológico normal. Sin lesiones cutáneas. Presión arterial (PA): 83/53 mmHg. Saturación de oxígeno (SatO2): 100%.
Pruebas complementarias
- Electrocardiograma (ECG): elevación del segmento ST en la cara diafragmática sin presencia de onda Q y descenso en cara lateral.
- Analítica sanguínea al ingreso: creatincinasa (CK) 3312 UI/l, troponina T 9,12 µg/l, transaminasa glutámico oxalacética (GOT) 408 UI/l, el resto de parámetros dentro de la normalidad. Analítica de orina: tóxicos negativos.
- Ecocardiograma: ventrículo izquierdo no dilatado ni hipertrófico, con buena contractilidad. Fracción de eyección: 64%. Ventrículo derecho no hipertrófico ni dilatado y con buena contractilidad. Aurícula izquierda no dilatada. Tabiques interauricular e interventricular íntegros. Válvula aórtica tricúspide con cierre simétrico con flujo normal. Válvula pulmonar normal con insuficiencia pulmonar con gradiente máximo 10 mmHg. Origen de las arterias coronarias normal, sin dilatación de ostium. Raíz aortica normal, cayado y aorta descendente sin alteraciones. Válvulas mitral y tricúspide normales. Patrón de función diastólica normal en ambos ventrículos. No hay líquido pericárdico. Flujo en la aorta abdominal pulsátil. Vena cava inferior de 23 mm, con buen colapso inspiratorio.
- Radiología de tórax: índice cardiotorácico < 0,5, sin condensaciones ni derrame.
Ante la sospecha de patología isquémica se deriva a la paciente a un centro especializado; a su llegada no tiene dolor torácico, sin cambios en la exploración física y con las constantes mantenidas. Se realiza:
- Analítica sanguínea: GOT 412 UI/l, transaminasa glutámico pirúvica (GPT) 52 UI/l, troponina T 8,01 µg/l, CK 2833 UI/l y creatincinasa MB (CK-MB) 272,2 UI/l, con el resto de parámetros normales.
- ECG, ecocardiograma y radiología de tórax: sin cambios respecto a los anteriores.
- Resonancia magnética (RM) cardiaca: situs solitus, compatible con miocarditis aguda.
Con el diagnóstico de miocarditis aguda ingresa inicialmente en la Unidad de Cuidados Intensivos Pediátricos (UCIP). No tiene dolor torácico. Afebril. Tendencia a la bradicardia sinusal con tensiones correctas. Mantiene una importante elevación de las enzimas cardiacas y de la CK sistémica. En el ECG se observa una elevación del segmento ST en cara diafragmática. No presenta acidosis ni alteración de la perfusión tisular. Mantiene hemograma y función renal sin disilectrolitemias.
Dada la posible orientación diagnóstica de miocarditis con rabdomiolisis, se cursa serología que es positiva para Mycoplasma pneumoniae, anticuerpos IgM (EIA) y reacción en cadena de la polimerasa (PCR), que son negativos. Se inicia tratamiento con antibióticos y gammaglobulina endovenosa.
La paciente se mantiene afebril, sin aumento de reactantes en la fase aguda. Las CK sistémicas y las enzimas cardiacas descienden y el ECG se normaliza. A los ocho días, se realiza ecocardiograma, que, a diferencia del día del ingreso, presenta un ventrículo izquierdo no dilatado ni hipertrófico, con buena función global, aunque el septo basal se contrae menos y la fracción de eyección es algo menor, del 60% (frente al 64%). El resto de parámetros evaluados es similar.
Fue dada de alta hospitalaria con completa resolución de la clínica. Se recomienda seguir controles por su cardiólogo y evitar el deporte de competición durante un mínimo de seis meses.
A los dos y seis meses del alta se realiza control cardiológico, ECG, Holter y ecocardiograma que son normales. En el control de los seis meses se realiza ergometría, la paciente permanece asintomática con ECG de esfuerzo sin signos de isquemia y ausencia de arritmias.
Ante la ausencia de síntomas, con exploración cardiológica, ECG, ecocardiograma, Holter y ergometría normales, se prescribe ejercicio físico: tres días a la semana, 30 minutos de ejercicio de resistencia cardiovascular a una intensidad del 55-65% de la frecuencia cardiaca de reserva, y ejercicio de fuerza-resistencia muscular a un 20-30%.
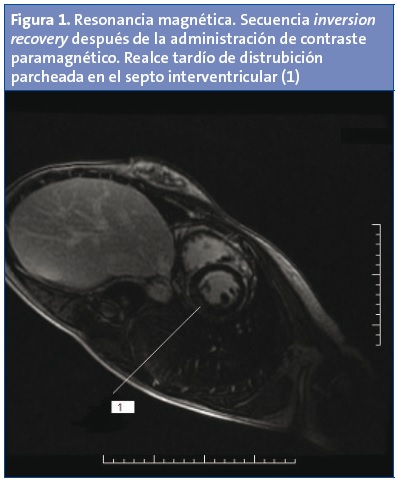
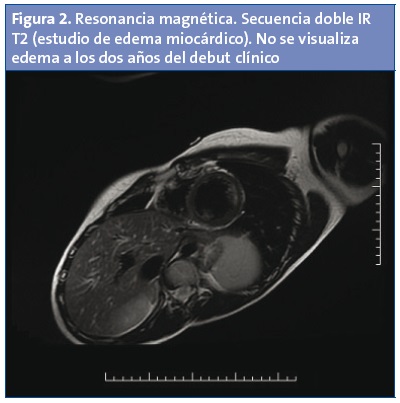
A los 12 meses, se realiza control cardiológico, ECG, ecocardiograma y Holter, que son normales. La ergometría sin eventos clínicos ni eléctricos de interés, con un rendimiento físico similar a la anterior prueba de esfuerzo. Además, se realiza RM cardiaca con realce tardío de distribución parcheada en el septo interventricular (Fig. 1), sin apreciarse edema miocardico (Fig. 2).
Con estos datos se permite el deporte de competición, aconsejándose controles semestrales, permaneciendo hasta la fecha la paciente asintomática.
DISCUSIÓN
En España, las causas más prevalentes de muerte súbita (MS) de origen cardiovascular en deportistas menores de 35 años son la displasia arritmogénica del ventrículo derecho, la miocardiopatía hipertrófica y las anomalías coronarias congénitas1. La miocarditis aguda tiene una incidencia entre un 5-12% de los casos de MS en jóvenes deportistas según las series consultadas.
En aproximadamente 1/20 casos de MS no se encuentra una causa a pesar de realizar una necropsia; en estos casos las posibles causas son: síndrome de QT largo, síndrome de QT corto, síndrome de Brugada, defectos progresivos en el sistema de conducción, taquicardia ventricular catecolaminérgica polimórfica y fibrilación ventricular idiopática2-3.
La miocarditis es un proceso inflamatorio local o general, caracterizado por la infiltración inflamatoria de la pared miocárdica con aparición de zonas de necrosis o de degeneración celular4. La etiología de miocarditis más frecuentes son5-7:
- Infecciones: por virus es la causa más común (Coxsackie A y B, citomegalovirus, hepatitis C, herpes virus humano 6, virus de la inmunodeficiencia humana, parvovirus B19, Epstein-Barr, virus varicela-zóster); bacterias (clamidia, Mycoplasma pneumoniae, estreptococo, Treponema pallidum, Borrelia, Corynebacterium diphtheriae, micobacterias); protozoos (Tryipanosoma cruzi); parásitos (Toxoplasma, Schistosoma, Larva migrans); hongos (Aspergillus, Candida, coccidios, criptococos, Histoplasma).
- Hipersensibilidad: catecolaminas, antidepresivos tricíclicos, diuréticos, digoxina, cefalosporinas, sulfamidas, dobutamina.
- Tóxicos: alcohol, cocaína, metales pesados, antraciclinas, interleucina-2.
- Enfermedades inmunológicas: lupus eritematoso sistémico, artritis reumatoide, sarcoidosis, síndrome hipereosinofílico, enfermedad de Churg-Strauss, miocarditis de células gigantes, enfermedad inflamatoria intestinal, diabetes mellitus, tirotoxicosis, arteritis de Takayasu, granulomatosis de Wegener.
La incidencia de la MS es muy difícil de establecer. En EE. UU. se ha encontrado una incidencia del 0,33-0,44/100 000 en deportistas menores de 40 años. En Francia, en atletas jóvenes, del 0,5-2/100 000, en Italia del 0,4/100 000 en deportistas, en Suecia en jóvenes deportistas de entre 17-34 años del 0,9/100 000, en Dinamarca del 1,21/100 000 y en Japón del 1,32/100 000, ambos en deportistas.
La presentación clínica es muy variable y heterogénea, des de formas asintomáticas, a leves que se limitan a signos menores como disnea, dolor torácico y palpitaciones en los días siguientes a un episodio febril, a formas más graves que cursan con insuficiencia cardiaca aguda, angina, shock cardiogénico o incluso muerte súbita8. Debido a la poca especificidad de sus síntomas clínicos de presentación, la miocarditis es habitualmente difícil de reconocer clínicamente en su episodio inicial y, probablemente, es por ello una enfermedad infradiagnosticada.
La evaluación de los atletas con sospecha de miocarditis debe incluir9-11:
- Anamnesis relacionada con posibles patologías cardiacas.
- Examen físico: auscultación cardiaca, valoración de pulsos arteriales, determinación de la tensión arterial.
- Biomarcadores como la CK-MB y particularmente las troponinas que, aunque carecen de especificidad, ayudan en el diagnóstico y, en el caso de la troponina T, son un buen marcador pronóstico.
- El ECG, aunque tiene baja especificidad, sigue siendo una importante herramienta diagnóstica. Los hallazgos pueden ser alteraciones inespecíficas, cambios en la onda T y en el segmento ST similares a un cuadro coronario agudo, arritmias supraventriculares y ventriculares y nuevas ondas Q12.
- El ecocardiograma es primordial en la evaluación diagnóstica inicial, permite evaluar el tamaño de las cavidades y la función ventricular. Las miocarditis fulminantes generalmente presentan cavidades cardiacas conservadas con engrosamiento de la pared y las agudas tienen marcada dilatación de las cavidades.
- La resonancia magnética nuclear (RM) se ha convertido en la técnica de diagnóstico de imagen de elección para el diagnóstico y seguimiento. La combinación de métodos, secuencias en T2 y en T1 con realce temprano de gadolinio y realce tardío permiten obtener información sobre las características del tejido en la etapa inicial inflamatoria y en la fase de daño miocárdico. Tiene la gran ventaja de ser una técnica no invasiva, con una excelente resolución anatómica y tisular, y aporta una información completa de la función ventricular, de la existencia o no de edema/inflamación miocárdica y de la presencia de áreas de fibrosis miocárdica13,14.
- La biopsia endomiocárdica es el método diagnóstico por excelencia de la miocarditis, y se deben seguir los criterios diagnósticos histopatológicos de Dallas. La biopsia puede ser negativa por la naturaleza parcheada de las lesiones y se deberá realizar más de una toma y utilizar técnicas inmunohistológicas y moleculares15.
- Otros métodos de imagen diagnósticos son: gammagrafía con galio 6716,17 y la gammagrafía con anticuerpos monoclonales antimiosina18-20.
La evolución más frecuente es la recuperación espontánea. Sin embargo, la miocarditis puede dar lugar en un 5-10% recidivas y desarrollar miocardiopatía dilatada21,22 e incluso desencadenar arritmias graves y provocar la MS.
A pesar de los avances en el conocimiento de sus mecanismos fisiopatológicos, y una mayor evidencia en la eficacia de la terapia inmunosupresora, las recomendaciones en el tratamiento de la miocarditis siguen siendo, en la mayoría de los casos, las del manejo de la causa y de la insuficiencia cardiaca si la hubiera. Queda por esclarecer cuál será el papel de los tratamientos antivirales, en los que se han visto resultados esperanzadores.
Recomendaciones23-27
- Los deportistas con sospecha o diagnóstico definitivo de miocarditis no deben participar en ningún deporte, al menos durante seis meses desde el comienzo de las manifestaciones clínicas.
- A partir de los seis meses pueden retomar el entrenamiento y participar en todos los deportes competitivos si reúnen los siguientes criterios:
- Ecocardiografía: los diámetros, la función ventricular y la motilidad parietal deben ser normales.
- Ausencia de arritmias clínicamente significativas: formas repetitivas o complejas de extrasistolia ventricular o supraventricular documentadas por Holter y ergometría.
- Normalización de biomarcadores de inflamación (troponinas, CPK-MB) y de insuficiencia cardiaca.
- Normalización de los cambios del ECG (excepto cambios menores del ST-T).
Para evitar un nuevo episodio de miocarditis y de MS se recomienda evitar el deporte de competición durante cuatro semanas después de una infección inespecífica24. No hay deportes más peligrosos que otros, el riesgo lo determinan la existencia de patología susceptible de provocar MS y la intensidad del esfuerzo24.
CONFLICTO DE INTERESES
Los autores declaran no presentar conflictos de intereses en relación con la preparación y publicación de este artículo.
ABREVIATURAS: CK: creatincinasa · CK-MB: creatina quinasa MB · ECG: electrocardiograma · GOT: transaminasa glutámico oxalacética · GPT: transaminasa glutámico pirúvica · MS: muerte súbita · PA: presión arterial · PCR: reacción en cadena de la polimerasa · RM: resonancia magnética · SatO2: saturación transcutánea de oxígeno · UCIP: Unidad de Cuidados Intensivos Pediátricos.
BIBLIOGRAFÍA
- Manonelles P, Aguilera B, Boraita A, Luengo E, Pons C, Suárez MP. La muerte súbita en el deporte. Registro en el Estado español. Apunts Med Esport. 2007;153:26-35.
- Maron BJ, Doerer JJ, Haas TS, Tierney DM, Mueller FO. Sudden deaths in young competitive athletes: analysis of 1866 deaths in the United States, 1980-2006. 2009;119:1085-1092.
- Maron BJ, Haas T, Ahluwalia A, Rutten-Ramos SC. Incidence of cardiovascular sudden deaths in Minnesota high school competitive athletes: impact on considerations for national 12-lead ECG preparticipation screening. J Am Coll Cardiol. 2014;63:1636-43.
- Asif M, Yim ES, Hoffman JM, Froelicher V. Update: causes and symptoms of sudden cardiac death in young athletes. Phys Sportsmed. 2015;43:44-53.
- Boraita A, Baño A, Berrazueta JR, Lamiel R, Luengo E, Manonelles P, et al. Guía de práctica clínica de la Sociedad Española sobre actividad física en el cardiópata. Rev Esp Cardiol. 2000;53:654-726.
- Laraudogoitia E, Díez I. Miocarditis y miocardiopatías. Rev Esp Cardiol Supl. 2006;6:21-9.
- Magnani JW, Dec GW. Myocarditis: current trends in diagnosis and treatment. Circulation. 2006;113:676-890.
- Liu PP, Mason JW. Advances in the understanding of myocarditis. 2001;104:1076-82.
- Theleman KF, Nuipper JJ, Roberts WC. Acute myocarditis sudden death without heart failure. Am J Cardiol. 2001;88:1078-83.
- Pressler A, Schmid A, Freiberger V, Scherr J, Uder M, Halle M. Myocarditis, myocardial fibrosis and eligibility for competitive sports. Int J Cardiol. 2011;152:131-2.
- Frick M, Pachinger O, Pölzl G. Myocarditis and sudden cardiac death in athletes. Diagnosis, treatment, and prevention. 2009:34:299-304.
- Schultz JC, Hilliard AA, Cooper LT, Rihal CS. Diagnosis and treatment of viral myocarditis. Mayo Clin Proc. 2009;84:1001-9.
- Sarda L, Colin P, Boccara F. Myocarditis in patients with clinical presentation of myocardial infarction and normal coronary angiograms. J Am Coll Cardiol. 2001;37:786-92.
- Gagliardi MG, Bevilacqua M, Di Renzi P, Picardo S, Passariello R, Marceletti C. Usefulness of magnetic resonance imaging for the diagnosis of acute myocarditis in infants and children, and comparison with endomyocardial biopsy. Am J Cardiol. 1991;68:1089-9.
- Friedrich MG, Strohm O, Shultz-Menger J, Marciniak H, Luft FC, Dictz R. Contrast media-enhanced magnetic resonance imaging visualizes myocardial changes in course of viral myocarditis. 1998;97:1802-9.
- Aretz HT, Billingham ME, Edwards WD. Myocarditis: a histopathologic definition and classification. Am J Cardiovasc Pathol. 1987;1:3-14.
- Friedrich MG, Strohm O, Shultz-Menger J, Marciniak H, Luft FC, Dictz R. Contrast media-enhanced magnetic resonance imaging visualizes myocardial changes in course of viral myocarditis. 1998:97:1802-9.
- Veluvolu P, Balian AA, Goldsmith R. Lyme carditis evaluation by Ga-67 and MRI. Clin Nucl Med. 1992;17:823-7.
- Yasuda T, Palacios IF, Dec GW. Indium 111-monoclonal antimyosin-antibody imaging in the diagnosis of acute myocarditis. 1987;76:306-11.
- Bergler-Klein J, Sochor H, Stanek G, Globits S, Ullrich R, Glogar D. Indium 111-monoclonal antimyosin antibody and magnetic resonance imaging in the diagnosis of acute Lyme carditis. Arch Intern Med. 1993;153:2696-700.
- Kuhl U, Lauer B, Souvatzoglu M, Vosberg H, Schultheiss HP. Antimyosin scintigraphy and immunohistologic analysis of endomyocardial biopsy in patients with suspected myocarditis: evidence of myocardial cell damage and inflamation in the absence of histològic signs of myocarditis. J Am Coll Cardiol. 1998;32:1371-6.
- Kindermann I, Barth C, Mahfoud F. Update on myocarditis. J Am Coll Cardiol. 2012;59:779-92.
- Basso C, Carturan E, Corrado D, Thiene G. Myocarditis and dilated cardiomyopathy in atletes: diagnosis, management, and recomendations for sport activity. Cardiol Clin. 2007;25:423-9.
- Pellicia A, Corrado D, Bjornstad HH. Recommendations for participation in competitive sport and leisure-time physical activity in individuals with cardiomyopathies, myocarditis and pericarditis. Eur J Cardiovasc Prev Rehabil. 2006;13:876-85.
- Scharhag J, Meyer T. Return to play after acute infectious disease in football players. J Sports Sci. 2014;32:1237-42.
- Montero-Cabezas JM. Tratamiento de la miocarditis y sus complicaciones. Cardiocore. 2012;47:147-50.
- Sociedad Española de Cardiología Pediátrica y Cardiopatías Congénitas y Subdirección General de Deportes y salud del Consejo Superior de Deportes (CSD). Guía Clínica de Evaluación cardiovascular previa a la práctica deportiva en Pediatría. Madrid: CSD; 2015. Disponible en https://goo.gl/WMBIv8
Comentarios
Este artículo aún no tiene comentarios.






