Vol. 24 - Num. 96
Originales
Infecciones del tracto urinario: etiología y susceptibilidades antimicrobianas
Francisco Miguel Escandell Ricoa, Lucía Pérez Fernándezb
aProfesor. Departamento de Enfermería. Universidad de Alicante. Alicante. España.
bCoordinadora de Enfermería. CS de Almoradí. Almoradí. Alicante. España.
Correspondencia: FM Escandell . Correo electrónico: francisco.escandell@ua.es
Cómo citar este artículo: Escandell Rico FM, Pérez Fernández L. Infecciones del tracto urinario: etiología y susceptibilidades antimicrobianas . Rev Pediatr Aten Primaria. 2022;24:e355-e362.
Publicado en Internet: 16-12-2022 - Número de visitas: 42251
Resumen
Introducción: la infección del tracto urinario (ITU) es una de las enfermedades más prevalentes en la práctica clínica. Con el fin de mejorar el tratamiento empírico, se ha estudiado la etiología de las infecciones urinarias en Pediatría y el perfil de sensibilidad antibiótica de los microorganismos responsables.
Material y métodos: estudio transversal, descriptivo y retrospectivo (2020-2021), en el que se incluyeron los microorganismos aislados con recuento significativo en muestras de orina de pacientes con ITU. Se analizó la etiología global y en función de la edad y el sexo. Se consideró únicamente una muestra de orina por paciente y episodio de ITU.
Resultados: Escherichia coli fue el microorganismo más aislado tanto en el conjunto de la población (62%) como en cada uno de los grupos analizados según edad y sexo. Su aislamiento en mujeres fue significativamente superior que en hombres (χ², p = 0,043). Su sensibilidad fue: 94% a fosfomicina y 86% a amoxicilina-ácido clavulánico.
Conclusiones: Escherichia coli continúa siendo el microorganismo más frecuentemente aislado en ITU. Por ello, para las ITU bajas, la amoxicilina-clavulánico y la nitrofurantoína podrían ser opciones adecuadas. Nuestro medio debería recomendar fosfomicina, ya que muestra varias ventajas para su uso, como la dosificación una vez al día, bajos efectos secundarios, resultados clínicos y microbiológicos adecuados y poco efecto sobre la microbiota intestinal.
Palabras clave
● Escherichia coli ● Fosfomicina ● Infección del tracto urinario ● Pruebas de sensibilidad microbianaINTRODUCCIÓN
La infección del tracto urinario (ITU) es una de las infecciones bacterianas más frecuentes en Pediatría, ya que el 8-10% de las niñas y el 2-3% de los niños tendrán una ITU sintomática antes de los 7 años1. La prevalencia global de ITU en niños menores de 2 años es aproximadamente del 5%2-4. La recurrencia de ITU antes del año de vida es cerca del 75% en los niños; y después del primer año de vida, las niñas presentan recurrencias en 40% y los varones en 30%5.
En la mayoría de los casos, el agente causal corresponde a los gérmenes que habitualmente colonizan la región perineal en la niña y el espacio subprepucial en el niño. Los menores de 2 años febriles con este diagnóstico tienen afectación del parénquima renal, por lo que el riesgo de disfunción renal es mayor en estas edades6,7.
El germen más frecuentemente implicado en la producción de ITU es Escherichia coli, responsable de más del 75% del total de las infecciones y de casi el 90% de las infecciones no complicadas. Algunas revisiones revelan que el porcentaje ha disminuido hasta un 54-67% a la vez que ha aumentado la incidencia de otros microorganismos como: Klebsiella, Proteus, Enterobacter, Citrobacter y Pseudomonas, sobre todo en aquellos pacientes con exposición previa a antibióticos o anomalías genitourinarias8.
El diagnóstico a tiempo de una ITU y su tratamiento adecuado pueden prevenir complicaciones a corto plazo, como una pielonefritis severa o sepsis de origen urinario que aparece hasta en el 30% de los recién nacidos y en el 20% de los lactantes menores de tres meses9. En lactantes y niños pequeños, los signos y síntomas de la enfermedad son inespecíficos. La fiebre sin foco suele ser la única manifestación inicial de una infección renal, lo que puede dificultar un diagnóstico oportuno y tratamiento innecesario en niños sin riesgo10,11.
El objetivo del estudio es describir la etiología de las infecciones urinarias en Pediatría y el perfil de sensibilidad antibiótica de los microorganismos responsables del Departamento de Salud 21 correspondiente con una zona rural del sur del Mediterráneo.
MATERIAL Y MÉTODOS
Diseño y ámbito de estudio
Se realizó un estudio transversal, descriptivo y retrospectivo, del 1 de enero de 2020 al 31 de diciembre de 2021, en el que se incluyeron los microorganismos aislados con recuento significativo en muestras de orina de pacientes con ITU. Se consideró únicamente una muestra de orina por paciente y episodio de ITU. El Departamento de Salud 21 da cobertura pediátrica a 27 000 habitantes. Se analizó la etiología global de ITU y por grupos en función de la edad (menores de 3 meses, de 3 a 6 meses, de 6 a 12 meses, de 12 a 18 meses y de 18 a 24 meses) y sexo de los pacientes.
Procedimiento
El cultivo se realizó mediante siembra de la orina en el medio cromogénico. La identificación microbiológica se realizó según el aspecto macroscópico de las colonias en el medio cromogénico y espectrometría de masas. La determinación de la sensibilidad antimicrobiana se realizó mediante la técnica Kirby-Bauer en agar Mueller-Hinton. La inclusión de antibióticos, pruebas fenotípicas de detección de mecanismos de resistencia, así como la interpretación de la sensibilidad, se realizaron siguiendo las recomendaciones del Clinical and Laboratory Standards Institute12.
La recogida de información se realizó desde la historia clínica digital (Abucasis, Orion clinic, Gestlab) a través de un cuaderno de recogida de datos electrónico con acceso exclusivo del investigador principal, omitiendo datos de carácter personal. En todo momento los participantes estuvieron identificados con un código propio del estudio de forma que todos llevaron las siglas ITUP y a continuación tres números de forma correlativa (ITUP 001, ITUP 002…).
Análisis estadístico
Realizamos un análisis descriptivo de todas las variables calculando sus frecuencias y porcentajes. Se aplicó la prueba de Chi-cuadrado para las variables categóricas. Los programas utilizados fueron Excel para la base de datos y el software SPSS (versión 25.0; IBM Corp., Armonk, NY) y los resultados se consideraron significativos si p <0,05.
Consideraciones éticas
Para la realización del estudio se solicitó la autorización del Comité de Ética e Investigación (CEI) del Departamento de Salud 21 (código de registro PI-2022-015).
Se consideraron los principios éticos para las investigaciones médicas en seres humanos, dispuestas por la Declaración de Helsinki de la 18.ª Asamblea de la Asociación Médica Mundial, de junio de 1964, como modo de participación en el estudio. Se respetó a su vez la confidencialidad y el uso de datos personales según la Ley orgánica 3/2018, de 5 de diciembre, de protección de datos personales y garantía de los derechos digitales. No precisó el consentimiento informado a los pacientes, puesto que es un estudio epidemiológico retrospectivo donde se utilizaron fuentes secundarias de la información. Los datos estuvieron protegidos de uso no permitido a personas ajenas a la investigación y, por tanto, fueron considerados estrictamente confidenciales. En el procesamiento de los datos y estrategias de análisis se respetó la confidencialidad del participante.
RESULTADOS
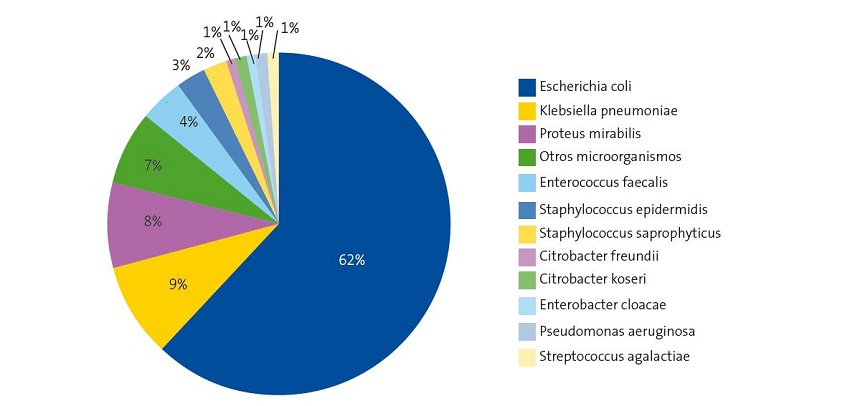
Durante el periodo de estudio se aislaron 388 uropatógenos. 275 (71%) correspondían a las niñas. En la Figura 1 se muestra la etiología de ITU en nuestra población de estudio.
La Tabla 1 recoge la frecuencia de aislamiento de los principales microorganismos, según edad y sexo. La ITU se desarrolló con mayor frecuencia en las niñas y disminuyó con la edad.
| Tabla 1. Infecciones del tracto urinario: etiología y susceptibilidades antimicrobianas. Distribución de uropatógenos, según el sexo y la edad de los pacientes (periodo de estudio: 2020-2021) | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Niños | |||||||||||||||
| Microorganismo |
<3 meses n = 51 |
Microorganismo |
3-6 meses n = 20 |
Microorganismo |
6-12 meses n = 20 |
Microorganismo |
12-18 meses n = 15 |
Microorganismo |
18-24 meses n = 7 |
||||||
| n | % | n | % | n | % | n | % | n | % | ||||||
| Escherichia coli | 17 | 33,3 | Escherichia coli | 8 | 40 | Escherichia coli | 13 | 65 | Escherichia coli | 7 | 46,6 | Escherichia coli | 3 | 43 | |
| Proteus mirabilis | 12 | 23,5 | Klebsiella pneumoniae | 3 | 15 | Klebsiella pneumoniae | 2 | 10 | Proteus mirabilis | 3 | 20 | Proteus mirabilis | 2 | 28,5 | |
| Klebsiella pneumoniae | 8 | 15,6 | Klebsiella oxytoca | 2 | 10 | Proteus mirabilis | 1 | 5 | Enterococcus faecalis | 2 | 13,3 | Pseudomonas aeruginosa | 1 | 14,3 | |
| Enterococcus faecalis | 4 | 7,8 | Enterococcus faecalis | 1 | 5 | Enterococcus faecalis | 1 | 5 | Morganella morganii | 1 | 6,6 | Klebsiella pneumoniae | 1 | 14,3 | |
| Pseudomonas aeruginosa | 2 | 4 | Pseudomonas aeruginosa | 1 | 5 | Klebsiella oxytoca | 1 | 5 | |||||||
| Klebsiella oxytoca | 1 | 2 | Proteus mirabilis | 1 | 5 | Enterobacter cloacae | 1 | 5 | |||||||
| Enterobacter cloacae | 1 | 2 | Enterobacter cloacae | 1 | 5 | ||||||||||
| Citrobacter Koseri | 1 | 2 | Citrobacter Koseri | 1 | 5 | ||||||||||
| Staphylococcus saprophyticus | 1 | 2 | |||||||||||||
| Otros microorganismos* | 4 | 7,8 | Otros microorganismos* | 2 | 10 | Otros microorganismos* | 1 | 5 | Otros microorganismos* | 2 | 13,3 | ||||
| Niñas | |||||||||||||||
| Microorganismo |
<3 meses n = 196 |
Microorganismo |
3-6 meses n = 30 |
Microorganismo |
6-12 meses n = 15 |
Microorganismo |
12-18 meses n = 16 |
Microorganismo |
18-24 meses n = 18 |
||||||
| n | % | n | % | n | % | n | % | n | % | ||||||
| Escherichia coli | 147 | 75 | Escherichia coli | 18 | 60 | Escherichia coli | 9 | 60 | Escherichia coli | 12 | 75 | Escherichia coli | 10 | 55,5 | |
| Klebsiella pneumoniae | 13 | 6,6 | Klebsiella pneumoniae | 3 | 10 | Klebsiella pneumoniae | 1 | 6,6 | Proteus mirabilis | 2 | 12,5 | Proteus mirabilis | 6 | 33,3 | |
| Klebsiella oxytoca | 13 | 6,6 | Enterococcus faecalis | 3 | 10 | Citrobacter Koseri | 1 | 6,6 | Klebsiella pneumoniae | 1 | 6,2 | Klebsiella pneumoniae | 2 | 11,1 | |
| Enterococcus faecalis | 7 | 3,4 | Pseudomonas aeruginosa | 1 | 3,3 | Enterococcus faecalis | 1 | 6,6 | Morganella morganii | 1 | 6,2 | ||||
| Staphylococcus saprophyticus | 5 | 2,5 | Proteus mirabilis | 1 | 3,3 | ||||||||||
| Proteus mirabilis | 4 | 2 | Staphylococcus saprophyticus | 1 | 3,3 | ||||||||||
| Morganella morganii | 3 | 1,4 | |||||||||||||
| Enterobacter cloacae | 2 | 1 | |||||||||||||
| Pseudomonas aeruginosa | 1 | 0,5 | |||||||||||||
| Streptococcus agalactiae | 1 | 0,5 | |||||||||||||
| Otros microorganismos * | 1 | 0,5 | Otros microorganismos * | 3 | 10 | Otros microorganismos * | 3 | 20 | |||||||

E. coli (62%) fue el microorganismo más frecuentemente aislado, tanto en el conjunto de la población como en cada uno de los grupos de edad y sexo evaluados (Figura 1 y Tabla 1). Hubo importantes diferencias en cuanto a su frecuencia de aislamiento, según edad y sexo, oscilando entre el 75% (niñas menores de 3 meses) y el 33,3% (niños menores de 3 meses). Comparando la frecuencia de aislamiento de E. coli según el sexo y la edad, se observó que el porcentaje de E. coli aislado en niñas fue significativamente superior que en niños (χ², p = 0,043) y que iba disminuyendo con la edad. Klebsiella pneumoniae y Proteus mirabilis siguieron en orden de frecuencia.
En el grupo de 0 a 6 meses, se aislaron Enterococcus faecalis y Pseudomonas aeruginosa con mayor frecuencia que en los otros grupos de edad analizados (Tabla 1).
Un 1,5% de los aislamientos correspondió a Staphylococcus saprophyticus, siendo este superior en el grupo de las niñas (5,8%). En menor frecuencia destacamos la presencia de Morganella morganii y Citrobacter koseri en todos los grupos de edad y sexo.
Respecto a la sensibilidad antibiótica de los uropatógenos más frecuentemente aislados, E. coli mostró un amplio rango de sensibilidad, desde el 86% frente a amoxicilina-ácido clavulánico, hasta el 94% frente a fosfomicina.
En la Tabla 2 se muestra el porcentaje global de sensibilidad del año 2021 para cada uno de los antibióticos, ponderado según la frecuencia de aislamiento de cada microorganismo, edad y sexo. Se observa una mayor tasa de sensibilidad a los antibióticos en las niñas, respecto a la de los niños. Respecto a la tasa de sensibilidad en los quimioterápicos urinarios, fosfomicina es superior al 95% en niñas y al 92% en niños, mientras que nitrofurantoína es superior al 89%, en niñas y superior al 86% en niños.
| Tabla 2. Infecciones del tracto urinario: etiología y susceptibilidades antimicrobianas. Sensibilidad antibiótica (%) ponderada por la frecuencia de aislamientos en función del sexo y de la edad (año 2021) | |||||
|---|---|---|---|---|---|
| Niños | |||||
| Antibióticos |
<3 meses n = 51 |
3-6 meses n = 20 |
6-12 meses n = 20 |
12-18 meses n = 15 |
18-24 meses n = 7 |
| Amoxicilina-clavulánico | 82,3 | 75 | 95 | 80 | 71,4 |
| Cefuroxima | 76,4 | 70 | 90 | 73,3 | 71,4 |
| Cefixima | 59 | 60 | 85 | 40 | 57,1 |
| Norfloxacino | 51 | 35 | 45 | 40 | 57,1 |
| Ciprofloxacino | 43 | 35 | 45 | 40 | 51,4 |
| Fosfomicina | 94,1 | 85 | 100 | 100 | 85,7 |
| Nitrofurantoina | 88,2 | 80 | 100 | 100 | 71,4 |
| Niñas | |||||
| Antibióticos |
<3 meses n = 196 |
3-6 meses n = 30 |
6-12 meses n = 15 |
12-18 meses n = 16 |
18-24 meses n = 18 |
| Amoxicilina-clavulánico | 90,8 | 83,3 | 93,3 | 100 | 88,8 |
| Cefuroxima | 88,2 | 76,6 | 66,6 | 100 | 77,7 |
| Cefixima | 59,6 | 66,6 | 60 | 62,5 | 66,6 |
| Norfloxacino | 60,2 | 56,6 | 53,3 | 56,2 | 66,6 |
| Ciprofloxacino | 51 | 70 | 73,3 | 25 | 61,1 |
| Fosfomicina | 94,3 | 96,6 | 100 | 100 | 88,8 |
| Nitrofurantoina | 88,2 | 96,6 | 86,6 | 100 | 83,3 |

DISCUSIÓN
Este estudio permite conocer la etiología de las infecciones urinarias en Pediatría y el perfil de sensibilidad antibiótica de los microorganismos responsables del Departamento de Salud 21 correspondiente con una zona rural del sur del Mediterráneo.
En nuestro medio, al igual que en otros estudios internacionales13, encontramos que el agente causal más común fue E. coli (62%), con predominio del sexo femenino, como también refieren otros autores14. Después de E. coli, el resto de las enterobacterias (38%) constituyen el segundo grupo de bacterias causantes de ITU, por frecuencia de aislamiento. Otros estudios muestran que la frecuencia de aislamiento de cada una de las enterobacterias depende del periodo de estudio, población evaluada, distribución geográfica, edad de los pacientes, infecciones de repetición, patologías urinarias y/o tratamientos antibióticos previos12,15.
Al igual que otros estudios16, Proteus mirabilis fue más común en niños que en niñas. La frecuencia de aislamiento de Klebsiella pneumoniae (9%) estuvo en segundo lugar, y se observa una similar distribución tanto por sexo como por cualquier grupo de edad. La frecuencia de aislamiento de Enterococcus faecalis (4%) también es elevada, en similitud con otros estudios17, donde mencionan factores de riesgo relacionados con huésped y uso de antibióticos18.
El aislamiento de Staphylococcus saprophyticus (2%) se observa más en niñas y varía entre las diferentes series, según la población de estudio. Nuestros resultados concuerdan con los de otros, donde Staphylococcus saprophyticus es un uropatógeno más común en niñas19,20. Por lo tanto, reconocer el papel del Staphylococcus saprophyticus como posible agente etiológico en niñas es esencial para guiar el tratamiento antibiótico empírico apropiado, ya que el patrón de resistencia antimicrobiana de esta bacteria puede diferir21.
Los resultados de nuestro estudio muestran que la sensibilidad conjunta de los microorganismos causantes de ITU a amoxicilina-ácido clavulánico fue del 86%, un porcentaje que podría permitir su utilización como fármaco empírico. Las quinolonas son antibióticos ampliamente utilizados en pacientes con infecciones agudas, complicadas o no. A pesar de los estudios que confirman que España es uno de los países europeos con mayor porcentaje de resistencias de E. coli a quinolonas22, estas se han mostrado al menos tan eficaces como cotrimoxazol y más eficaces que algunos betalactámicos23. En nuestro estudio, la tasa de sensibilidad conjunta de los microorganismos causantes de ITU a quinolonas fue del 52%, destacando al igual que otros estudios24 una mayor actividad en las quinolonas de segunda generación (norfloxacino) frente a bacterias gramnegativas.
Los datos de las guías de la Infectious Diseases Society of America (IDSA) publicados en 2022 refieren que las decisiones de tratamiento empírico deben guiarse por los patógenos más probables, la gravedad de la enfermedad del paciente, la fuente probable de la infección y cualquier factor adicional específico del paciente. Del mismo modo, es importante distinguir entre la colonización bacteriana y la infección, ya que la terapia antibiótica innecesaria solo promoverá el desarrollo de resistencia y puede causar daños innecesarios relacionados con los antibióticos al paciente25.
Con respecto a la profilaxis antibiótica, se deberían tener en cuenta los patrones de resistencias locales e intentar seleccionar los antibióticos de menor espectro de acción para evitar la aparición de resistencias26. Nuestros hallazgos, al igual que otros estudios, recomiendan la utilización de nitrofurantoína como un tratamiento eficaz para las infecciones del tracto urinario no complicadas27.
A diferencia de los grupos de antibióticos previamente mostrados, la sensibilidad de E. coli a fosfomicina y nitrofurantoína continúa siendo mayor del 90%. Al igual que otros estudios, consideramos que estos fármacos podrían ser muy útiles como tratamiento empírico de la ITU no complicada28. En otro estudio multicéntrico español, muestran un rango de sensibilidad de E. coli a fosfomicina variable de 95,6 a 99,4% según las diferentes comunidades incluidas29.
Una limitación del estudio puede ser su diseño y la obtención de la muestra de un único Departamento de Salud. Sería adecuado realizar estudios con diseños prospectivos. Una de las fortalezas del estudio es que incluye los datos anuales de ITU comunitario de un Departamento de Salud, imprescindibles para establecer un tratamiento empírico actualizado, revisar y actualizar las guías clínicas sobre las infecciones del tracto urinario, y como base de cualquier Programa de Optimización de Uso de los Antibióticos (PROA). Son datos esenciales para tratar de forma adecuada las infecciones, evitar el fracaso de los tratamientos, así como el desarrollo de resistencias. Deben realizarse periódicamente estudios epidemiológicos locales para actualizar estos datos y poder realizar estudios de evolución de resistencias.
CONCLUSIÓN
Los perfiles de sensibilidad a los antimicrobianos han ido variando a lo largo del tiempo, entre un Departamento de Salud e incluso dependiendo de los ámbitos comunitarios, por lo que las recomendaciones de tratamiento no pueden ser universales, sino que deben basarse en los estudios de sensibilidad locales a los principales patógenos. Además, deben considerarse otros parámetros como la eficacia y la seguridad, el coste, la duración de las pautas, la comodidad de administración y la capacidad de selección de microorganismos resistentes.
En conclusión, E. coli continúa siendo el microorganismo más frecuentemente aislado en ITU con una tasa de sensibilidad a fosfomicina superior al 90% y a la amoxicilina-ácido-clavulánico del 86%. Por ello, para las ITU bajas, la amoxicilina-clavulánico y la nitrofurantoína podrían ser opciones adecuadas. Nuestro medio debería recomendar fosfomicina, ya que muestra varias ventajas para su uso, como la dosificación una vez al día, bajos efectos secundarios, resultados clínicos y microbiológicos adecuados y poco efecto sobre la microbiota intestinal.
CONFLICTO DE INTERESES
Los autores declaran no presentar conflictos de intereses en relación con la preparación y publicación de este artículo.
ABREVIATURAS
CEI: Comité de ética e investigación · ITU: infección del tracto urinario · PROA: programa de optimización de uso de los antibióticos.
CONSIDERACIONES ÉTICAS
La aprobación del estudio se obtuvo del Comité de Ética en Investigación del Departamento de Salud 21 (código de registro PI-2022-015).
BIBLIOGRAFÍA
- Hellström A, Hanson E, Hansson S, Hjälmas K, Jodal U. Association between urinary symptoms at 7 years old and previous urinary tract infection. Arch Dis Child. 1991;66:232- 4.
- Baraff LJ. Management of fever without source in infants and children. Ann Emerg Med. 2000;36:602-14.
- Mintegi S, González M, Pérez A, Pijoán JI, Capapé S, Benito J. Infants aged 3-24 months with fever without source in the emergency room: characteristics, management and outcome. An Pediatr (Barc). 2005;62:522-8.
- Lee GM, Fleisher GR, Harper MB. Management of febrile children in the age of the conjugate pneumococcal vaccine: a cost-effectiveness analysis. Pediatrics. 2001;108:835-44.
- Mattoo TK. Are prophylactic antibiotics indicated after a urinary tract infection? Curr Opin Pediatr. 2009;21:203-6.
- Coulthard MG, Lambert HJ, Vernon SJ, Hunter EW, Keir MJ, Matthews JN. Does prompt treatment of urinary tract infection in preschool children prevent renal scarring: mixed retrospective and prospective audits. Arch Dis Child. 2014;99:342-7.
- Shaikh N, Ewing AL, Bhatnagar S, Hoberman A. Risk of renal scarring in children with a first urinary tract infection: A systematic review. Pediatrics. 2010;126:1084-91.
- Alberici I, Bayazit AK, Drozdz D, Emre S, Fischbach M, Harambat J, et al. Pathogens causing urinary tract infections in infants: a European overview by the ESCAPE study group. Eur J Pediatr. 2014;174:783-90.
- Bhat RG, Katy TA, Place FC. Pediatric urinary tract infections. Emerg Med Clin North Am. 2011;29:637-53.
- Pinzón Fernández MV, Zúñiga Cerón LF, Saavedra Torres JS. Infección del tracto urinario en niños, una de las enfermedades infecciosas más prevalentes. Rev Fac Med. 2018;66:393-8.
- Kaufman J, Temple-Smith M, Sanci l. Urinary tract infections in children: an overview of diagnosis and management. BMJ Paediatr Open. 2019;3:e000487.
- Anesi JA, Lautenbach E, Nachamkin I, Garrigan C, Bilker WB, Omorogbe J, et al. The role of extended-spectrum cephalosporin-resistance in recurrent community-onset Enterobacteriaceae urinary tract infections: a retrospective cohort study. BMC Infect Dis. 2019;19:163.
- Leung AKC, Wong AHC, Leung AAM, Hon KL. Urinary tract infection in children. Recent Pat Inflamm Allergy Drug Discov. 2019;13:2-18.
- Samancı S, Çelik M, Köşker M. Antibiotic resistance in childhood urinary tract infections: A single-center experience. Turk Pediatri Ars. 2020;55:386-92.
- Sorlozano A, Jiménez Pacheco A, De Dios Luna del Castillo J, Sampedro A, Martínez-Brocal A, Miranda Casas C, et al. Evolution of the resistance to antibiotics of bacteria involved in urinary tract infections: a 7-year surveillance study. Am J Infect Control. 2014;42:1033-8.
- García Vera C. Infecciones urinarias. Rev Pediatr Aten Primaria. Supl. 2013;(22):71-80.
- Tripathi A, Shukla S, Singh A, Prasad K. Prevalencia, resultado y factor de riesgo asociado con Enterococcus faecalis y Enterococcus faecium resistentes a la vancomicina en un hospital de atención terciaria en el norte de la India. Indian J Med Microbiol. 2016;34:38-45.
- Hooton TM, Roberts PL, Cox ME, Stapleton AE. Voided midstream urine culture and acute cystitis in premenopausal women. N Engl J Med. 2013;369:1883-91.
- Lo DS, Shieh HH, Barreira ER, Ragazzi SL, Gilio AE. High frequency of Staphylococcus saprophyticus urinary tract infections among female adolescents. Pediatr Infect Dis J. 2015;34:1023-5.
- Palou J, Pigrau C, Molina I, Ledesma JM, Angulo J; Grupo Colaborador Español del Estudio ARESC. Etiología y sensibilidad de los uropatógenos identificados en infecciones urinarias bajas no complicadas de la mujer (Estudio ARESC): implicaciones en la terapia empírica. Med Clin (Barc). 2011;136:1-7.
- Eriksson A, Giske CG, Ternhag A. La importancia relativa de Staphylococcus saprophyticus como patógeno del tracto urinario: distribución de bacterias entre las muestras de orina analizadas durante 1 año en un importante laboratorio sueco. APMIS. 2013;121:72-8.
- Schito GC, Naber KG, Botto H, Palou J, Mazzei T, Gualco l, et al. The ARESC study: an international survey on the antimicrobial resistance of pathogens involved in uncomplicated urinary tract infections. Int J Antimicrob Agents. 2009;34:407-13.
- Hooton TM, Scholes D, Gupta K, Stapleton AE, Roberts PL, Stamm WE. Amoxicillin-clavulanate vs ciprofloxacin for the treatment of uncomplicated cystitis in women: a randomized trial. JAMA. 2005;293:949-55.
- Alós JI. Quinolonas. Enferm Infecc Microbiol Clin. 2009;27:290-7.
- Tamma PD, Aitken SL, Bonomo RA, Mathers AJ, van Duin D, Clancy CJ. Infectious Diseases Society of America Guidance on the Treatment of Extended-Spectrum β-lactamase Producing Enterobacterales (ESBL-E), Carbapenem-Resistant Enterobacterales (CRE), and Pseudomonas aeruginosa with Difficult-to-Treat Resistance (DTR-P. aeruginosa). Clin Infect Dis. 2021;72:e169-e183.
- Hawkey PM, Jones AM. The changing epidemiology of resistance. J Antimicrob Chemother. 2009;64:3-10.
- Zhanel GG, Hisanaga TL, Laing NM, DeCorby MR, Nichol KA, Palatnik LP, et al. Antibiotic resistance in outpatient urinary isolates: final results from the North American Urinary Tract Infection Collaborative Alliance (NAUTICA). Int J Antimicrob Agents. 2005;26:380-8.
- Fasugba O, Mitchell BG, Mnatzaganian G, Das A, Collignon P, Gardner A. Five-year antimicrobial resistance patterns of urinary Escherichia coli at an Australian tertiary hospital: time series analyses of prevalence data. PLoS One. 2016;11:e0164306.
- Andreu A, Planells I; Grupo Cooperativo Español para el Estudio de la Sensibilidad Antimicrobiana de los Patógenos Urinarios. Etiología de la infección urinaria baja adquirida en la comunidad y resistencia de Escherichia coli a los antimicrobianos de primera línea. Estudio nacional multicéntrico. Med Clin (Barc). 2008;130:481-6.