Vol. 24 - Num. 96
Originales
Ondansetrón para el control de vómitos asociados a gastritis y gastroenteritis aguda en urgencias de Pediatría: uso, abuso y buen uso
Alicia García Marína, Germán Lloret Ferrándizb, Javier González de Diosc
aFacultad de Medicina. Universidad Miguel Hernández. Alicante. España.
bServicio de Pediatría. Hospital General Universitario de Alicante. Alicante. ISABIAL-Instituto de Investigación Sanitaria y Biomédica de Alicante. España.
cServicio de Pediatría. Hospital General Universitario de Alicante. Departamento de Pediatría. Universidad Miguel Hernández. ISABIAL-Instituto de Investigación Sanitaria y Biomédica. Alicante. España.
Correspondencia: J González. Correo electrónico: javier.gonzalezdedios@gmail.com
Cómo citar este artículo: García Marín A, Lloret Ferrándiz G, González de Dios J. Ondansetrón para el control de vómitos asociados a gastritis y gastroenteritis aguda en urgencias de Pediatría: uso, abuso y buen uso . Rev Pediatr Aten Primaria. 2022;24:351-61.
Publicado en Internet: 22-11-2022 - Número de visitas: 42903
Resumen
Introducción: el ondansetrón es un antiemético ampliamente utilizado en la práctica clínica para el control de vómitos asociados a gastritis y/o gastroenteritis aguda en niños. Sin embargo, la evidencia disponible es controvertida, sus indicaciones no están claramente definidas y no existe una unanimidad de uso en las guías de práctica clínica.
Material y métodos: se realizó un estudio de cohortes retrospectivo en el que se incluyó un total de 825 niños entre 0 y 14 años con vómitos asociados a gastritis y/o gastroenteritis aguda que acudieron a Urgencias de Pediatría de un hospital terciario durante el año 2019. Se analizó la asociación entre el uso de ondansetrón y la necesidad de rehidratación intravenosa, las hospitalizaciones, el tiempo de permanencia en Urgencias y las nuevas consultas a Urgencias dentro de las 72 horas posteriores.
Resultados: de la muestra estudiada, el 38,8% de los pacientes recibieron ondansetrón. La administración de ondansetrón redujo el riesgo de ingreso (OR 0,19; IC 95%: 0,04-0,84) y disminuyó el tiempo de permanencia en Urgencias (p = 0,000). No se encontraron diferencias significativas en la reducción de la necesidad de rehidratación intravenosa (OR 0,65; IC 95%: 0,40-1,05) ni en las nuevas visitas a Urgencias dentro de las 72 horas siguientes (OR 1,38; IC 95%: 0,82-2,31).
Conclusiones: nuestros resultados sugieren que el uso de ondansetrón podría ser beneficioso en niños mayores de 6 meses con vómitos asociados a gastritis y/o gastroenteritis aguda y que presenten deshidratación de leve a moderada.
Palabras clave
● Gastroenteritis aguda ● Niños ● Ondansetrón ● VómitosINTRODUCCIÓN
La gastroenteritis aguda (GEA) ocupa el segundo lugar en la frecuencia de visitas a Urgencias de Pediatría (UPED) en países desarrollados1-3. El vómito es también un motivo común de consulta a UPED4, y puede presentarse de forma aislada (gastritis) o asociado a GEA, pudiendo ser un componente importante de la misma3,5-7. La problemática de los vómitos radica en que su presencia dificulta la rehidratación oral. En este punto es donde entran en juego los antieméticos, que facilitan la rehidratación oral, menos invasiva que la rehidratación intravenosa3,6.
El ondansetrón es el único antiemético que ha demostrado eficacia en la reducción de vómitos asociados a gastritis/GEA en niños2, y no existe una base científica lo suficientemente sólida para respaldar el uso de otros antieméticos en estos casos5,8,9. Actualmente, el uso de ondansetrón está indicado para el tratamiento de vómitos asociados a quimioterapia, radioterapia o poscirugía en niños mayores de 6 meses10. Sin embargo, en la práctica clínica se emplea para el tratamiento de vómitos secundarios a gastritis/GEA, a pesar de que su uso no está recomendado de forma rutinaria11.
Por otro lado, diversos estudios sugieren que los niños con vómitos asociados a gastritis/GEA y con deshidratación de leve a moderada podrían beneficiarse del uso del ondansetrón, ya que disminuye la frecuencia de vómitos y favorece la rehidratación oral12-14. Sin embargo, varios estudios coinciden en el aumento de episodios de diarrea en los pacientes a los que se administró ondansetrón13-15, lo que podría contribuir a un aumento de las visitas posteriores a UPED y favorecer la deshidratación. Otro efecto adverso relacionado con su uso es la prolongación del intervalo QT2,10,16.
Asimismo, algunos estudios concluyen que el ondansetrón disminuye la frecuencia de vómitos, reduce la necesidad de rehidratación intravenosa y disminuye el tiempo de estancia en UPED, pero no modifica las tasas de hospitalización ni las visitas posteriores6,17. Sin embargo, los datos publicados son contradictorios, pues otros estudios sugieren que disminuye las nuevas visitas a UPED y las tasas de ingresos o, incluso, que el ondansetrón no disminuye la necesidad de rehidratación intravenosa18-20.
Algunas guías recomiendan el ondansetrón para el control de vómitos en niños con gastritis/GEA, como la Canadian Pediatric Society, aunque no de forma rutinaria si el síntoma predominante es la diarrea, debido a que es el efecto adverso más frecuente21. Otras guías, como la National Institute for Health and Care Excellence (NICE), no recomiendan el uso de antieméticos para el control de vómitos asociados a GEA22. Por otra parte, la guía de la European Society of Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN) tampoco recomienda el uso rutinario de ondansetrón, pero señala que podría ser efectivo y que se necesitan más estudios al respecto2. A pesar de esto, el uso de ondansetrón es común en la práctica clínica23.
Por tanto, debido a la controversia existente sobre el uso de ondansetrón, no existe un consenso en las diferentes guías de prácticas clínicas. Así, vemos que las indicaciones de ondansetrón están claramente definidas cuando los vómitos se asocian a quimioterapia, radioterapia o poscirugía, pero no lo están en los casos de gastritis/GEA, quedando su uso bajo criterio médico. Los objetivos de nuestro estudio son: como objetivo principal, analizar el patrón de uso de ondansetrón en UPED de un hospital terciario en niños de 0 a 14 años (ambos inclusive) con vómitos asociados a gastritis/GEA y plantear unas indicaciones basadas en las mejores pruebas científicas tras la revisión de la literatura científica; y, como objetivos secundarios, valorar la necesidad de rehidratación intravenosa, ingresos, tiempo de permanencia en UPED y nuevas consultas en las primeras 72 horas en los pacientes a los que se les administró ondansetrón frente a aquellos que recibieron otros tratamientos.
MATERIAL Y MÉTODOS
Diseño del estudio y selección de pacientes
Estudio observacional de cohortes retrospectivo llevado a cabo mediante la revisión de historias clínicas electrónicas de una muestra de pacientes de 0 a 14 años (ambos inclusive) con vómitos asociados a gastritis/GEA que acudieron a UPED del hospital terciario durante el año 2019.
Tras analizar los datos, observamos que durante el año 2019 se atendieron a un total de 37 617 niños en UPED, de los cuales 3645 (9,68%) presentaron un diagnóstico de vómitos y/o GEA, y cuya distribución en meses se expresa en la Tabla 1. Para limitar el tamaño muestral, se recogieron los datos de los pacientes en los martes y sábados de las semanas impares del año 2019, y en los jueves y domingos de las semanas pares de dicho año.
| Tabla 1. Distribución de los casos de vómitos y/o gastroenteritis aguda en los meses del año 2019 en urgencias de Pediatría del Hospital Universitario de Alicante | ||||
|---|---|---|---|---|
| Casos | Casos/día | Urgencias | % Total urgencias | |
| Enero | 266 | 8,58 | 3513 | 7,57% |
| Febrero | 295 | 10,53 | 3329 | 8,86% |
| Marzo | 423 | 13,64 | 3536 | 11,96% |
| Abril | 298 | 9,93 | 2982 | 9,99% |
| Mayo | 210 | 6,77 | 2825 | 7,43% |
| Junio | 254 | 8,46 | 2691 | 9,43% |
| Julio | 309 | 9,96 | 2677 | 11,54% |
| Agosto | 243 | 7,83 | 2681 | 9,06% |
| Septiembre | 275 | 9,16 | 2772 | 9,92% |
| Octubre | 371 | 11,96 | 3576 | 10,37% |
| Noviembre | 384 | 12,8 | 3228 | 11,89% |
| Diciembre | 317 | 10,22 | 3807 | 8,32% |
| TOTAL | 3645 | 9,98 | 37 617 | 9,68% |

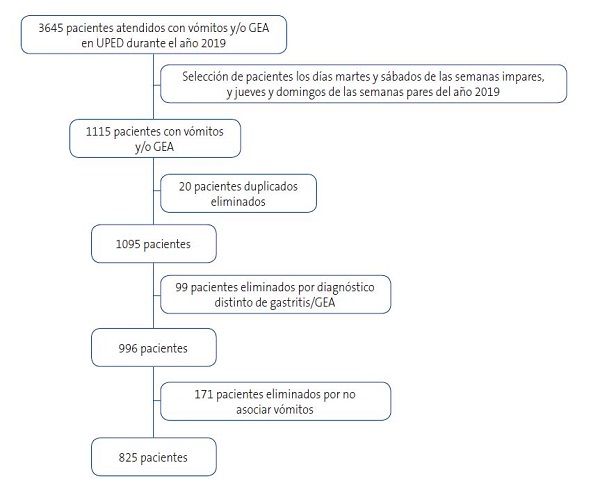
Se excluyeron del estudio a todos aquellos pacientes que presentaron vómitos por una causa distinta a gastritis/GEA, y todos aquellos que presentaron gastritis/GEA sin vómitos asociados, obteniendo un tamaño muestral final de 825 pacientes. En la Figura 1 se expone el diagrama de flujo de selección de pacientes en nuestro estudio y los pacientes excluidos del estudio se recogen en la Tabla 2.
| Figura 1. Diagrama de flujo de selección de pacientes |
|---|
 |

| Tabla 2. Diagnósticos de pacientes excluidos del estudio | |
|---|---|
| Diagnósticos | Pacientes |
| Infección de vías respiratorias altas | 44 |
| Problemas dermatológicos | 9 |
| Traumatismos | 6 |
| Ingesta de objetos o productos | 5 |
| Herpangina-aftas orales | 3 |
| Cefalea | 2 |
| Cirugías recientes | 2 |
| Dolor abdominal | 2 |
| Leucemia linfoblástica | 2 |
| Presíncope | 2 |
| Hematemesis | 2 |
| Fisura anal | 2 |
| Adenitis mesentérica | 2 |
| Problemas oftalmológicos | 2 |
| Síndrome febril | 1 |
| Rinitis aguda | 1 |
| Bronquiolitis | 1 |
| Convulsión febril | 1 |
| Intoxicación por benzodiacepinas | 1 |
| Hernia inguinal | 1 |
| Desconexión del medio | 1 |
| Atragantamiento puntual | 1 |
| Portador de válvula ventrículo-peritoneal | 1 |
| Reflujo gastroesofágico | 1 |
| Síndrome de Mallory Weiss | 1 |
| Hepatomegalia a estudio | 1 |
| Vómitos resueltos | 1 |
| Sospecha de diarrea causada por amoxicilina-clavulánico | 1 |

La aplicación de ondansetrón fue siempre por vía sublingual en UPED y con una dosis estandarizada por intervalo de peso: 2 mg en menores de 15 kg, 4 mg entre 15 y 30 kg, y 8 mg en mayores de 30 kg24.
Variables de estudio
A partir del listado de pacientes proporcionado por el servicio de Admisión y Documentación Clínica del hospital, realizamos la recogida de datos mediante la revisión de historias clínicas a través del programa informático Orion Clinic® v11.0 (Agencia Valenciana de Salud, España). Para su posterior análisis, los datos se almacenaron en un documento de Microsoft® Excel v16.0 (Microsoft®, EE. UU.). Todos los datos fueron anonimizados.
Se recogieron datos clínicos y epidemiológicos de los pacientes, entre los que se incluyen la edad, sexo, peso, temperatura, glucemia y cetonemia. Las variables relacionadas con la sintomatología fueron el dolor abdominal, la presencia o no de deshidratación, el número de vómitos y deposiciones líquidas y el tiempo de evolución. Para determinar el grado de deshidratación a partir de la información disponible en las historias clínicas, se empleó la escala de Gorelick25. Los datos relacionados con el tratamiento que recibió el paciente incluyeron la administración de ondansetrón sublingual, rehidratación oral y/o rehidratación intravenosa.
También se incluyeron como variables de estudio el tiempo de permanencia en UPED (desde que el paciente llega a UPED hasta que se da de alta o es ingresado), nuevas consultas en las 72 horas posteriores (donde no se tuvieron en consideración las visitas a centros de salud o pediatra de zona) e ingresos.
Estudio estadístico
El análisis estadístico se llevó a cabo mediante el programa IBM SPSS® Statistics for Windows, v25.0. Para analizar las diferencias significativas entre ambos grupos estudiados, empleamos la Chi cuadrado de Pearson (χ2) para variables cualitativas, y la prueba t de Student o prueba de U de Mann-Whitney para variables cuantitativas, según siguieran o no una distribución normal. La prueba utilizada para estimar si las variables siguen o no una distribución normal fue la prueba de Shapiro-Wilks. Para las variables categóricas, la medida de asociación utilizada fue la odds ratio (OR) con un intervalo de confianza (IC) del 95%. En todos los análisis realizados se consideró significación estadística un valor de p <0,05.
Aspectos éticos
El estudio se realizó de acuerdo con los requerimientos del Comité Ético del hospital. Se concedió la exención del consentimiento informado en el estudio, respetando en todo momento la protección de datos y anonimizando los mismos.
RESULTADOS
Del total de pacientes incluidos en el estudio (n = 825), 320 (38,79%) recibieron ondansetrón sublingual. En las Tablas 3 y 4 se recogen las características de la población estudiada.
| Tabla 3. Características de la población estudiada (variables cuantitativas) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Ondansetrón(n = 320) | No ondansetrón (n = 505) | ||||||||
| Variables cuantitativas | N válido (%) | Mediana | Media (DS) | (mín; máx) | N válido (%) | Mediana | Media (DS) | (mín; máx) | p valor |
| Edad (años) | 320 | 4,73 | 5,73 (3,75) | (0,3; 14,9) | 505 | 2,81 | 4,19 (3,61) | (0,02; 14,9) | 0,000 |
| <1 año | 7 (2,2) | 95 (18,8) | |||||||
| 1,1-5 años | 160 (50,0) | 256 (50,7) | |||||||
| 5,1-10 años | 100 (31,3) | 107 (21,2) | |||||||
| 10,1-15 años | 53 (16,6) | 47 (9,3) | |||||||
| Peso (kg) | 319 | 18,3 | 22,97 (13,7) | (7,15;92) | 500 | 14,7 | 19,05 (13,63) | (3,03; 84,5) | 0,000 |
| Temperatura (°C) | 313 | 36,4 | 36,5 (0,9) | (34,5;40,2) | 502 | 36,5 | 36,63 (0,9) | (34,5; 39,7) | 0,023 |
| <37 °C | 241 (77,0) | 367 (73,1) | |||||||
| 37-38 °C | 49 (15,7) | 97 (19,3) | |||||||
| >38 °C | 23 (7,3) | 38 (7,6) | |||||||
| Glucemia (mg/dl) | 173 | 101 | 101,44 (24,25) | (44;179) | 170 | 96 | 95,36 (26,21) | (31; 211) | 0,026 |
| <70 mg/dL | 19 (10,98) | 33 (19,41) | |||||||
| 70-160 mg/dL | 152 (87,86) | 135 (79,41) | |||||||
| >160 mg/dL | 2 (1,16) | 2 (1,18) | |||||||
| Cetonemia (mmol/L) | 100 | 1,4 | 2,0 (1,85) | (0,1;6,3) | 87 | 2,1 | 2,56 (2,08) | (0,1;6,9) | 0,057 |
| Número de vómitos | 220 | 5 | 6,55 (4,55) | (1;35) | 347 | 3 | 4,012 (3,89) | (1;40) | 0,000 |
| Evolución de vómitos (horas) | 311 | 8 | 15,77 (20,59) | (0;120) | 474 | 12 | 23,41 (25,4) | (0; 120) | 0,000 |
| Número de deposiciones líquidas | 274 | 0 | 1,64 (2,65) | (0;20) | 392 | 0 | 2,28 (4,3) | (0;32) | 0,000 |
| Evolución de deposiciones líquidas (horas) | 306 | 0 | 9,4 (20,16) | (0;120) | 468 | 3,5 | 18,09 (27,92) | (0;120) | 0,000 |

| Tabla 4. Características de la población estudiada (variables cualitativas) | |||
|---|---|---|---|
| Ondansetrón (n = 320) (%) |
No ondansetrón (n = 505) (%) |
||
| Variables cualitativas | N (%) | N (%) | p valor |
| Sexo | 0,502 | ||
|
180 (56,3) | 272 (53,9) | |
| Dolor abdominal | 131 (40,9) | 159 (31,5) | 0,006 |
| Deshidratación | 19 (5,9) | 33 (6,5) | 0,730 |
|
19 (5,9) | 26 (5,1) | |
|
0 (0) | 6 (1,2) | |
|
0 (0) | 1 (0,2) | |
| Deposiciones líquidas | 126 (39,38) | 294 (58,22) | 0,000 |
| Intento de rehidratación oral | 54 (16,87) | 266 (52,67) | 0,000 |

Al estratificar a los pacientes según su edad, los menores de 1 año se concentraron en el grupo no-ondansetrón (18,5% frente a 2,2%). Solo 52 pacientes (6,3%) presentaron deshidratación, y no se encontraron diferencias significativas entre ambos grupos estudiados (p = 0,730). En el grupo al que se administró ondansetrón, solo 19 pacientes (5,9%) presentaron deshidratación, y en todos los casos el grado de deshidratación fue leve.
Un total de 89 pacientes (10,8%) recibieron rehidratación intravenosa y la administración de ondansetrón no se asoció de forma significativa a una reducción de la necesidad de la misma (OR 0,65; IC 95%: 0,40 a 1,05). Sin embargo, si analizamos separadamente al pequeño subgrupo de pacientes que presentaron deshidratación, encontramos que la rehidratación intravenosa se utilizó en menor frecuencia en los que recibieron ondansetrón que en aquellos que no lo recibieron (OR 0,16; IC 95%: 0,04 a 0,57).
Solo dos pacientes (0,63%) requirieron ingreso en el grupo al que se administró ondansetrón y 16 (3,17%) en el grupo no-ondansetrón, mostrando una reducción del riesgo de ingreso cuando se administra ondansetrón (OR 0,19; IC 95%: 0,04 a 0,84).
Un 7,7% de los pacientes (63 en total) acudieron de nuevo a Urgencias en las primeras 72 horas. Sin embargo, la administración de ondansetrón no se asoció de manera significativa con las nuevas consultas en UPED en las siguientes 72 horas (OR 1,38; IC 95%: 0,82 a 2,31). El tiempo de estancia en UPED fue significativamente mayor en el grupo al que se administró ondansetrón (p = 0,000) (Tabla 5).
| Tabla 5. Variables resultado de interés | ||||||
|---|---|---|---|---|---|---|
| Variables principales y secundarias | N (%) | Ondansetrón (n = 320) (%) |
No ondansetrón (n = 505) (%) |
p valor | IC 95% | Odds ratio (OR) |
| Rehidratación IV | 89 (10,8) | 27 (8,44) | 62 (12,28) | 0,079 | 0,409-1,059 | 0,658 |
| Rehidratación IV en pacientes deshidratados (n = 52) | 35 (67,3) | (n = 19) (%) | (n = 33) (%) | 0,003 | 0,045-0,575 | 0,162 |
| 8 (42,11) | 27 (81,82) | |||||
| Ingresos | 18 (2,18) | 2 (0,63) | 16 (3,17) | 0,008 | 0,044-0,842 | 0,192 |
| Nueva consulta a UPED (<72 horas) | 63 (7,7) | 29 (9,06) | 34 (6,73) | 0,224 | 0,824-2,314 | 1,381 |
| Tiempo de permanencia en UPED (minutos) | 825 (100) | 320 (100) | 505 (100) | |||
|
116,5 | 56 | 0,000 | |||
|
162,46 (195,516) |
128,79 (188,926) |
||||
|
(14;1234) | (13;1185) | ||||

Tras eliminar a los menores de 6 meses de edad del estudio (31 pacientes), vemos que solo dos pertenecían al grupo al que se administró ondansetrón, mientras que los otros 29 pacientes pertenecían al grupo no-ondansetrón. Al excluir a dichos pacientes, siguieron sin encontrarse diferencias significativas en ambos grupos en cuanto al tratamiento con rehidratación intravenosa (OR 0,68; IC 95%: 0,42 a 1,10) y a las nuevas consultas a UPED dentro de las 72 horas posteriores (OR 1,29; IC 95%: 0,76 a 2,19). Por otro lado, al eliminar a estos menores de 6 meses del análisis, solo encontramos 8 ingresos (1,68%) en el grupo al que no se administró ondansetrón, perdiéndose significación estadística (p = 0,173).
En el caso del tiempo de estancia en UPED, se continúan viendo diferencias significativas en las medianas de tiempo de ambos grupos estudiados (p = 0,000) (Tabla 6).
| Tabla 6. Variables resultado de interés tras excluir a los menores de 6 meses del análisis | ||||||
|---|---|---|---|---|---|---|
| Variables principales y secundarias | N (%) | Ondansetrón (n = 318) (%) |
No ondansetrón (n = 476) (%) |
p valor | IC 95% | Odds ratio (OR) |
| Rehidratación IV | 84 (10,58) | 27 (8,49) | 57 (11,97) | 0,113 | 0,421-1,104 | 0,680 |
| Ingresos | 10 (1,26) | 2 (0,63) | 8 (1,68) | 0,173 | 0,07-1,775 | 0,370 |
| Nueva consulta a UPED (<72 horas) | 61 (7,68) | 28 (8,8) | 33 (6,93) | 0,335 | 0,767-2,191 | 1,296 |
| Tiempo de permanencia en UPED (minutos) | 794 (100) | 318 (100) | 476 (100) | |||
|
116,5 | 54 | 0,000 | |||
|
162,29 | 123,53 | ||||
|
(14;1234) | (13;1185) | ||||

DISCUSIÓN
En este estudio retrospectivo observamos que una gran proporción de pacientes (38,7%) con vómitos asociados a gastritis/GEA recibieron ondansetrón sublingual. Estos hallazgos son concordantes con algunos estudios publicados, que evidencian un incremento llamativo del uso de ondansetrón para el tratamiento de vómitos secundarios a gastritis/GEA en los últimos años26.
Para limitar el tamaño muestral y reducir sesgos en la recogida de datos, seleccionamos dos días de la semana al azar de todas las semanas del año 2019 para que estuvieran representados todos los periodos estacionales, días festivos y laborales, y todos los horarios. Con esto intentamos reducir la influencia que los distintos factores pudieran tener en determinados periodos concretos del año, así como intentar representar el proceder de un mayor número de personal sanitario que si hubiéramos seleccionado al azar meses completos.
Nuestros hallazgos sugieren que el ondansetrón no disminuye la frecuencia de rehidratación intravenosa, lo que contrasta con la gran mayoría de estudios publicados17,18,27. Esto podría deberse a las diferencias entre la población estudiada, ya que la mayoría de los participantes de nuestro estudio (observacional en la práctica clínica) no presentaron deshidratación, mientras que presentar algún grado de deshidratación fue considerado como criterio de inclusión en dichos estudios (experimentales). Además, en nuestro estudio, un número considerable de pacientes que no presentaron deshidratación (301 pacientes) fueron tratados con ondansetrón. Esto podría reflejar un mal uso de este fármaco, ya que no existe por el momento ninguna evidencia científica de que el ondansetrón suponga un beneficio en este tipo de pacientes18,20 y, por tanto, una mala indicación de aplicación del ondansetrón en nuestra muestra impide demostrar ese beneficio.
Un ensayo clínico llevado a cabo por Freedman y cols. en 201920, en el que se incluyeron pacientes no deshidratados, muestra unos resultados similares a los obtenidos en nuestro estudio, donde el ondansetrón no se asoció de manera significativa a una reducción de las tasas de rehidratación intravenosa. Consideramos que este estudio podría asemejarse al nuestro al incluir exclusivamente a pacientes sin deshidratación, ya que una sorprendente mayoría de participantes en nuestro estudio no presentaron deshidratación (93,7%). De hecho, si analizamos en nuestro estudio al subgrupo de pacientes con deshidratación, encontramos que el ondansetrón reduce de manera estadísticamente significativa la necesidad de rehidratación intravenosa (OR 0,16; IC 95%: 0,04 a 0,57).
Por otro lado, en un estudio llevado a cabo por Benary y cols. publicado en 202019, más de la mitad (55,1%) de los pacientes que recibieron rehidratación intravenosa habían recibido previamente ondansetrón. Esto difiere con nuestros resultados, donde la mayoría de los pacientes que recibieron rehidratación intravenosa no habían sido tratados con ondansetrón (69,66%), pudiendo sugerir un uso excesivo de la rehidratación intravenosa o un uso no adecuado del ondansetrón, ya que presumiblemente uno de los principales objetivos de su administración es evitar la rehidratación intravenosa.
Existe discrepancia en la literatura sobre la disminución de los ingresos. Algunos estudios parecen indicar que administrar ondansetrón disminuye las tasas de hospitalización, lo que concuerda con los resultados globales obtenidos en nuestro trabajo14,18. Sin embargo, otros estudios no han encontrado diferencias significativas en cuanto a ingresos en ambos grupos17,27, y nuestro artículo también podría sumarse a estos hallazgos, ya que al excluir a los pacientes menores de 6 meses no observamos diferencias en ambos grupos. Esto podría atribuirse a la población seleccionada, ya que en la mayor parte de estos trabajos excluyeron a los menores de 6 meses, debido a que típicamente no suele administrarse ondansetrón a esta edad. Todo ello sugiere que los hallazgos obtenidos deben ser evaluados en el contexto de la población estudiada.
En cuanto a las nuevas consultas a UPED dentro de las 72 horas posteriores, no se encontraron diferencias significativas. Un 7,6% de pacientes acudieron de nuevo a UPED en nuestro estudio, mientras que dicho porcentaje en otros estudios ronda el 4,7%19. Aunque este dato podría ser importante, ya que podría reflejar un fracaso en el tratamiento, debemos considerar la educación sanitaria de la población y la facilidad de acceso a urgencias hospitalarias de cada país como posibles responsables de dicha discordancia.
Otro estudio, liderado por Freedman y cols.17, muestra una reducción del tiempo en UPED de un 12% en el grupo al que se administró ondansetrón, con una media de tiempo de 106 minutos. Los resultados de nuestro estudio se desmarcan de los obtenidos en dicho estudio, ya que el tiempo de estancia en UPED en minutos fue mayor en el grupo al que se administró ondansetrón (162,46 vs. 128,79). Esto podría ser explicado por diferentes factores. El tiempo de permanencia en Urgencias podría estar condicionado por la hora a la que se atendió al paciente, ya que existe cierta tendencia a permanecer menos tiempo en UPED cuando el paciente acude por la noche. Además, en el caso de la administración de ondansetrón, se suele dejar al paciente en observación 30 minutos antes de reiniciar la rehidratación oral, lo que supone un incremento en el tiempo de permanencia en dicho grupo. Por otro lado, sospechamos que en el grupo no tratado con ondansetrón, muchos de los pacientes que reciben rehidratación intravenosa son ingresados en las primeras horas tras la asistencia permaneciendo, a su vez, menos tiempo en UPED. Además, todos los pacientes que no recibieron ningún tipo de tratamiento se encuentran incluidos dentro del grupo no-ondansetrón, concentrándose probablemente en este grupo los pacientes de menor gravedad y los que reciben un alta más precoz.
Por otro lado, durante la recogida de datos, se obtuvo información controvertida en la forma de uso de ondansetrón. Algunos facultativos administraron ondansetrón de manera simultánea con la colocación de una vía para rehidratación intravenosa, lo que impide uno de sus principales beneficios, que es evitar la rehidratación intravenosa. También, en ocasiones, no se esperaba un tiempo prudencial entre la administración de ondansetrón y la rehidratación intravenosa, de manera que un vómito inmediatamente posterior a la administración de este antiemético era considerado como un fracaso en el tratamiento. Sin embargo, el ondansetrón, al administrarse por vía sublingual, no sufre el fenómeno de primer paso hepático, y la aparición de vómitos en los primeros minutos tras su administración no debería considerarse como fracaso terapéutico.
Finalmente, un metanálisis recientemente publicado18, atribuye la disparidad de resultados de los estudios publicados hasta la fecha a las diferencias basales de la población estudiada y a los distintos enfoques metodológicos de los autores en el diseño de los estudios.
Es importante analizar las limitaciones de este estudio. Una de ellas deriva de las características de todo estudio retrospectivo, por lo que solo se pudieron recoger los datos detallados en las historias clínicas, con la consiguiente pérdida de información. Además, los pacientes no fueron aleatorizados, pudiendo encontrar diferencias en las características de la población en ambos grupos estudiados. De hecho, la diferencia en la distribución de pacientes menores de 6 meses nos ha obligado a realizar un subanálisis de los resultados. Por otro lado, nuestro estudio no incluye a la totalidad de pacientes atendidos en UPED con diagnóstico de gastritis/GEA en el año 2019 (solo un 30,6%). Aun así, es un tamaño muestral considerable (n = 825) y representativo para valorar nuestra práctica clínica habitual. Además, algunas variables recogidas están sujetas a la subjetividad (como el número de vómitos o deposiciones líquidas y el grado de deshidratación) y no fueron estudiadas otras variables como la diarrea, una de las principales complicaciones del ondansetrón. Asimismo, podrían existir factores de confusión, especialmente los relacionados con la edad o la gravedad del paciente. A pesar de ello, nuestro estudio ha sido realizado en la práctica clínica real, permitiéndonos realizar un primer análisis de nuestra experiencia clínica con el uso de ondansetrón.
Las conclusiones de nuestro estudio son:
- Se evidencia un mal uso y abuso del ondansetrón para el control de vómitos asociados a gastritis/GEA en Urgencias de Pediatría de nuestro hospital. Un 38,8% del total de pacientes incluidos en el estudio fueron tratados con ondansetrón y solo 19 (5,9%) presentaron deshidratación, siendo en todos los casos de grado leve.
- Los resultados obtenidos parecen indicar que el ondansetrón no disminuye la necesidad de rehidratación intravenosa, especialmente en pacientes no deshidratados. Sin embargo, es probable que sea útil en pacientes con deshidratación.
- El ondansetrón parece disminuir las tasas de ingresos, pero es probable que no tenga el mismo efecto cuando se excluyen a los menores de 6 meses de edad.
- El ondansetrón no parece disminuir las visitas a Urgencias de Pediatría en las 72 horas posteriores.
- El tiempo de permanencia en Urgencias de Pediatría podría aumentar con la administración de ondansetrón. Sin embargo, otros factores podrían influir en este resultado, como la gravedad del paciente, la hora de atención o la administración adicional de otros tratamientos.
Por tanto, el uso del ondansetrón en el manejo de los vómitos asociados a gastritis/GEA en UPED de nuestro hospital demuestra un abuso y mal uso en su utilización. Nuestra recomendación de uso adecuado en función de nuestra experiencia clínica (evidencia basada en la medicina) y la revisión de la literatura científica (medicina basada en la evidencia) incluye: (1) no recomendar de forma rutinaria el uso de ondansetrón en estos pacientes; y (2) considerar su uso en pacientes pediátricos (mayores de 6 meses) con vómitos por gastritis/GEA y que presenten deshidratación leve-moderada.
Estas recomendaciones son coherentes con el documento de consenso publicado recientemente por el Grupo de Trabajo de Gastroenterología y Nutrición de la AEPap en cuanto a la buena relación riesgo-beneficio del ondansetrón en los vómitos asociados a GEA28. Sin embargo, consideramos que el problema fundamental de este fármaco es su correcta indicación, pues si hemos constatado abuso en la utilización del ondansetrón en UPED, podría traducirse en una situación similar en Atención Primaria.
CONFLICTO DE INTERESES
Los autores declaran no presentar conflictos de intereses en relación con la preparación y publicación de este artículo.
ABREVIATURAS
AEPap: Asociación Española de Pediatría de Atención Primaria · GEA: gastroenteritis aguda · IC: intervalo de confianza · OR: odds ratio · UPED: urgencias de Pediatría.
BIBLIOGRAFÍA
- American Academy of Pediatrics. Practice parameter: the management of acute gastroenteritis in young children. Pediatrics. 1996;97:424-35.
- Guarino A, Ashkenazi S, Gendrel D, Lo Vecchio A, Shamir R, Szajewska H; European Society for Pediatric Gastroenterology, Hepatology, and Nutrition; European Society for Pediatric Infectious Diseases. European Society for Pediatric Gastroenterology, Hepatology, and Nutrition/European Society for Pediatric Infectious Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe: update 2014. J Pediatr Gastroenterol Nutr. 2014;59:132-52.
- Florez ID, Niño-Serna LF, Beltrán-Arroyave CP. Acute Infectious Diarrhea and Gastroenteritis in Children. Curr Infect Dis Rep. 2020;22:4.
- De la Torre Espí M, Molina Cabañero JC. Vómitos [en línea] [consultado el 09/04/2020]. Disponible en https://docplayer.es/93245-Vomitos-mercedes-de-la-torre-espi-juan-carlos-molina-cabanero.html
- Martín-Gavilán C, García-Avilés B, González-Montero R. Gastroenteritis aguda. Protocolos diagnóstico-terapéuticos de la AEP: Infectología pediátrica [en línea] [consultado el 09/04/2020]. Disponible en https://xdoc.mx/documents/gastroenteritis-aguda-asociacion-espaola-de-pediatria-5eed2271d94c9
- Romano C, Dipasquale V, Scarpignato C. Antiemetic Drug Use in Children: What the Clinician Needs to Know. J Pediatr Gastroenterol Nutr. 2019;68:466-71.
- Fedorowicz Z, Jagannath VA, Carter B. Antiemetics for reducing vomiting related to acute gastroenteritis in children and adolescents. Cochrane Database Syst Rev. 2011;9:CD005506.
- DeCamp LR, Byerley JS, Doshi N, Steiner MJ. Use of antiemetic agents in acute gastroenteritis: a systematic review and meta-analysis. Arch Pediatr Adolesc Med 2008;162:858-65.
- Metoclopramida: restricciones de uso en niños y adolescentes. Agencia española de medicamentos y productos sanitarios. En: Ministerio de Sanidad, Política Social e Igualdad. Madrid; 2011 [en línea] [consultado el 09/04/2020]. Disponible en www.aemps.gob.es/informa/notasInformativas/medicamentosUsoHumano/seguridad/2011/docs/NI-MUH_20-2011.pdf?x38929
- Ficha técnica Zofran® 4 mg solucion inyectable. Agencia española de medicamentos y productos sanitarios. Madrid; 2019 [en línea] [consultado el 09/04/2020]. Disponible en https://cima.aemps.es/cima/dochtml/ft/59071/FT_59071.html
- Mosqueda Peña R, Rojo Conejo P. Gastroenteritis aguda. Asociación Española de Pediatría [en línea] [consultado el 09/04/2020]. Disponible en https://www.yumpu.com/es/document/view/16068833/12-gastroenteritis-aguda-asociacion-espanola-de-pediatria
- Hagbom M, Novak D, Ekström M, Khalid Y, Andersson M, Lindh M, et al. Ondansetron treatment reduces rotavirus symptoms-A randomized double-blinded placebo-controlled trial. PLoS One. 2017;12:e0186824.
- Freedman SB, Pasichnyk D, Black KJL, Fitzpatrick E, Gouin S, Milne A, et al. Gastroenteritis therapies in developed countries: Systematic review and meta-analysis. PLoS One. 2015; 10:e0128754.
- Yilmaz HL, Yildizdas RD, Sertdemir Y. Clinical trial: oral ondansetron for reducing vomiting secondary to acute gastroenteritis in children - a double-blind randomized study. Aliment Pharmacol Ther. 2010;31:82-91.
- Marchetti F, Bonati M, Maestro A, Zanon D, Rovere F, Arrighini A, et al. Oral ondansetron versus domperidone for acute gastroenteritis in pediatric emergency departments: Multicenter double blind randomized controlled trial. PLoS One. 2016;11:e0165441.
- Ondansetrón. En: Asociación Española de Pediatría. Pediamécum [en línea] [consultado el 09/04/2020]. Disponible en https://www.aeped.es/comite-medicamentos/pediamecum/ondansetron
- Freedman SB, Adler M, Seshadri R, Powell EC. Oral ondansetron for gastroenteritis in a pediatric emergency department. N Engl J Med. 2006;354:1698-705.
- Wu HL, Zhan X. Effect of ondansetron on vomiting associated with acute gastroenteritis in a developing country: a meta-analysis. Eur J Pediatr. 2020;179:1181-9.
- Benary D, Lozano JM, Higley R, Lowe D. Ondansetron Prescription is associated with reduced return visits to the Pediatric Emergency Department for children with gastroenteritis. Ann Emerg Med. 2020;76:625-34.
- Freedman SB, Soofi SB, Willan AR, Williamson-Urquhart S, Ali N, Xie J, et al. Oral ondansetron administration to nondehydrated children with diarrhea and associated vomiting in Emergency Departments in Pakistan: a randomized controlled rrial. Ann Emerg Med. 2019;73:255-65.
- Cheng A. Emergency department use of oral ondansetron for acute gastroenteritis-related vomiting in infants and children. Paediatr Child Health. 2011;16:177-82.
- Diarrhoea and vomiting caused by gastroenteritis in under 5s: diagnosis and management. En: National Institute for Health and Care Excellence. UK; 2019 [en línea] [consultado el 09/04/2020]. Disponible en www.nice.org.uk/guidance/cg84/chapter/2-Research-recommendations#other-therapies-ondansetron
- Li ST, DiGiuseppe DL, Christakis DA. Antiemetic use for acute gastroenteritis in children. Arch Pediatr Adolesc Med. 2003;157:475-9.
- García de Paredes Esteban JC, Abdelkader Maanan M, Querol Gutiérrez JJ, Mohamed Haddu M, García Muñiz D. Protocolos conjunto de Atención Primaria-Atención Especializada para el manejo de medicamentos: Protocolo de uso racional de consansetrón. Madrid: Instituto Nacional de Gestión Sanitaria;2020 [en línea] [consultado el 26/05/2022]. Disponible en https://ingesa.sanidad.gob.es/bibliotecaPublicaciones/publicaciones/periodicasRevistas/docs/2020/ProtocolosC_V2_N2_2020.pdf
- Gorelick MH, Shaw KN, Murphy KO. Validity and reliability of clinical signs in the diagnosis of dehydration in children. Pediatrics. 1997;99:E6.
- Freedman SB, Hall M, Shah SS, Kharbanda AB, Aronson PL, Florin TA, et al. Impact of increasing ondansetron use on clinical outcomes in children with gastroenteritis. JAMA Pediatr. 2014;168:321-9.
- Freedman SB, Soofi SB, Willan AR, Williamson-Urquhart S, Siddiqui E, Xie J, et al. Oral ondansetron administration to dehydrated children in Pakistan: a randomized clinical trial. Pediatrics. 2019;144:e20192161.
- Rodríguez Delgado J, Castell Miñana M, González Martín l, Hoyos Vázquez MS, Blesa Baviera LC; Grupo de Trabajo de Gastroenterología y Nutrición de la Asociación Española de Pediatría de Atención Primaria (AEPap). Uso de ondansetrón en el manejo de los vómitos asociados a gastroenteritis aguda en Pediatría de Atención Primaria. Posicionamiento del Grupo de Trabajo de Gastroenterología y Nutrición de la AEPap. Rev Pediatr Aten Primaria. 2021;23:e55-e64.




