Otitis media aguda: una causa poco frecuente de síndrome de Lemierre
Marta Marín Andrésa, Aída M.ª Gutiérrez Sánchezb, Carmelo Guerrero Laleonab, Matilde Bustillo Alonsoc
aMIR-Pediatría. Hospital Universitario Miguel Servet. Zaragoza. España.
bServicio de Pediatría. Hospital Infantil Universitario Miguel Servet. Zaragoza. España.
cUnidad de Infectología Pediátrica. Servicio de Pediatría. Hospital Universitario Miguel Servet. Zaragoza. España.
Correspondencia: M Marín. Correo electrónico: marta_marin91@hotmail.com
Cómo citar este artículo: Marín Andrés M, Gutiérrez Sánchez AM, Guerrero Laleona C, Bustillo Alonso M. Otitis media aguda: una causa poco frecuente de síndrome de Lemierre. Rev Pediatr Aten Primaria. 2019;21:e145-e149.
Publicado en Internet: 13-09-2019 - Número de visitas: 19005
Resumen
El síndrome de Lemierre es una patología poco frecuente y potencialmente letal, que se origina como complicación de una infección localizada a nivel de cabeza y cuello que se extiende al espacio carotídeo. Se asocia a tromboflebitis séptica de la vena yugular interna y con frecuencia produce embolias sépticas a distancia. Se presenta generalmente como un cuadro de fiebre y odinofagia de varios días de evolución tras el antecedente de una infección orofaríngea aparentemente resuelta. Otros focos infecciosos menos frecuentes pueden corresponder a mastoiditis, sinusitis u otitis media aguda. El diagnóstico es fundamentalmente clínico y apoyado en las pruebas de imagen, como la ecografía Doppler y la tomografía computarizada cervical con contraste. El tratamiento consiste en antibioterapia prolongada con adecuada cobertura para anaerobios, especialmente Fusobacterium necrophorum, el patógeno más frecuente. El papel de la anticoagulación en el síndrome de Lemierre es controvertido. Se presenta un caso de síndrome de Lemierre secundario a una otitis media aguda.
Palabras clave
● Embolia ● Otitis media ● Síndrome de Lemierre ● Tromboflebitis séptica ● Vena yugular internaINTRODUCCIÓN
El síndrome de Lemierre, también denominado sepsis posangina o necrobacilosis, es una patología poco frecuente hoy en día, pero potencialmente grave y letal. Este síndrome fue descrito por primera vez por Lemierre en el año 1936. Era considerada una enfermedad relativamente común y con una alta mortalidad en la era preantibiótica. En los últimos años se considera una enfermedad olvidada para algunos autores, por su relativa baja frecuencia1,2. Sin embargo, el aumento de las resistencias a los antibióticos está influyendo negativamente en su prevalencia3.
Este síndrome se origina como complicación de una infección localizada a nivel de cabeza y cuello que se extiende al espacio carotídeo y que origina una tromboflebitis séptica de la vena yugular interna. Con frecuencia se asocia a embolias sépticas a distancia, el compromiso pulmonar es el más frecuente. En la mayoría de los casos el proceso infeccioso inicial se localiza en la orofaringe. Sin embargo, se han reportado casos secundarios a otro tipo de infecciones menos frecuentes, como mastoiditis, sinusitis, otitis media y celulitis4.
CASO CLÍNICO
Mujer de 14 años que acude al servicio de urgencias de un hospital terciario por presentar otalgia izquierda de siete días de evolución asociada a fiebre de hasta 39,2 °C, desde hace 48 horas. Refiere además dolor retroauricular y occipital desde hace 24 horas. Fue valorada el día previo en el mismo servicio de urgencias y se indicó iniciar tratamiento con amoxicilina-clavulánico. La paciente había sido diagnosticada de otitis media aguda izquierda 15 días antes del episodio actual y había recibido tratamiento con amoxicilina durante siete días. Como antecedentes personales destaca la presencia de obesidad y otitis medias agudas de repetición.
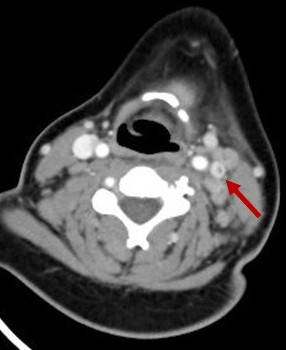
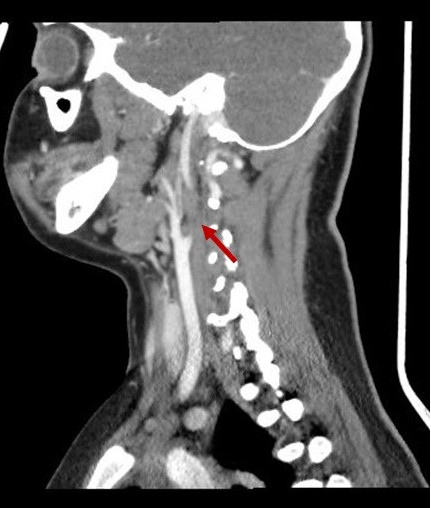
En la exploración física presenta edema retroauricular izquierdo, sin despegamiento del pabellón auricular, adenopatía submandibular izquierda dolorosa y en la otoscopia izquierda se visualiza el tímpano abombado y deslustrado. Se realiza analítica sanguínea en la que destaca: proteína C reactiva 16,78 mg/dl, procalcitonina 0,17 ng/ml, leucocitos 19 800/mm3 (neutrófilos 77,4%). Se decide ingresar a la paciente en planta de hospitalización e iniciar tratamiento con amoxicilina-clavulánico intravenoso. A las 24 horas del ingreso presenta empeoramiento clínico con aparición de tumefacción laterocervical izquierda de unos 2-3 cm de diámetro, caliente y dolorosa, junto con limitación a la movilización cervical. Es valorada por el servicio de otorrinolaringología y se indica realización de tomografía computarizada (TC) cervical urgente, que muestra una otomastoiditis izquierda, trombosis yugular interna izquierda (Figs. 1 y 2) y adenoflemón izquierdo.
Se modifica la antibioterapia por cefotaxima más clindamicina intravenosas y se añade tratamiento con corticoide intravenoso y heparina de bajo peso molecular subcutánea. Se completa el estudio realizando una radiografía de tórax y ecocardiograma, que descartan complicaciones asociadas. A los cuatro días del empeoramiento clínico se aísla Streptococus intermedius en el hemocultivo extraído al ingreso. Tras contacto con el servicio de microbiología, se acuerda mantener tratamiento con clindamicina y sustituir cefotaxima por amoxicilina-clavulánico.
Inicia mejoría clínica progresiva en los siguientes días. Se completaron 14 días de antibioterapia intravenosa. Al alta continua tratamiento con amoxicilina-clavulánico oral durante tres semanas y heparina de bajo peso molecular subcutánea durante tres meses.
Se completa un estudio genético de mutaciones más frecuentes asociadas a trombofilia familiar, sin detectar ninguna mutación en la paciente. Se realizan controles ambulatorios de la paciente, que se mantiene asintomática y se ajusta la anticoagulación. Se solicita a los cuatro meses una ecografía Doppler cervical, que muestra permeabilidad de la vena yugular interna.
DISCUSIÓN
El síndrome de Lemierre fue en el pasado una entidad frecuente y con pronóstico fatal. Sin embargo, el uso generalizado de antibióticos en las infecciones amigdalares la han convertido en una entidad rara y poco conocida1,4. El síndrome de Lemierre afecta típicamente a adolescentes y adultos jóvenes inmunocompetentes, aunque tiene un segundo pico de incidencia en ancianos1,5.
El agente causal más frecuente es Fusobacterium necrophorum, una bacteria gramnegativa, anaerobia estricta, que forma parte de la flora normal de la cavidad oral, gastrointestinal y del aparato genital femenino1,5. Se han descrito otros patógenos aerobios y anaerobios implicados, incluyendo Bacteroides, Staphylococus, Streptococus, Peptostreptococus, Proteus y Eikenella corrodens. Con frecuencia la enfermedad es causada por más de un microorganismo, en forma de coinfección por bacterias aerobias y anaerobias. Ocasionalmente pueden encontrarse en forma aislada, pero es posible que esos casos reflejen la dificultad para cultivar organismos anaerobios estrictos1,5. En el caso clínico presentado se aisló Streptococus intermedius en el hemocultivo. Este microorganismo pertenece al grupo de Streptococcus anginosus (o Streptococcus milleri) y se ha descrito como agente causal de tromboflebitis séptica6. Además, este microorganismo se asocia con frecuencia con bacterias anaerobias relacionadas con frecuencia con el síndrome de Lemierre. Sin embargo, dado que no se recibió muestra de hemocultivo para anaerobios y por tanto no se pudo descartar la coinfección, se sustituyó cefotaxima por amoxicilina-clavulánico.
Aunque la patogenia de la enfermedad no está bien definida, se cree que la alteración de las barreras mucosas en el contexto de la infección primaria facilita que el microorganismo atraviese la mucosa, produzca intensa inflamación del espacio parafaríngeo lateral e invada los vasos linfáticos de la zona. Por contigüidad, la pared de la vena yugular interna se vería afectada sufriendo un proceso de tromboflebitis con la consiguiente embolización de material infectado a distancia, pudiendo afectar órganos como el pulmón, corazón, hígado o articulaciones1,4.
Se presenta generalmente como un cuadro caracterizado por fiebre y odinofagia de varios días de evolución tras el antecedente de una infección faríngea aparentemente resuelta o que no remite pasados 3-7 días. En cerca del 90% de los casos las amígdalas palatinas y el tejido periamigdalino son el origen de la infección primaria. Otros focos infecciosos iniciales menos frecuentes pueden corresponder a otitis media aguda, como en el caso clínico presentado, o infecciones de origen dental5. Independientemente del origen de la infección, una vez afectada la vena yugular interna, el paciente suele presentar dolor alrededor del ángulo de la mandíbula o paralelo al músculo esternocleidomastoideo, asociado a tumefacción dolorosa o signos inflamatorios locales en la cara lateral del cuello. Asimismo, se asocia sintomatología sistémica con fiebre elevada, mal estado general y signos de sepsis3. Puede haber además trismus, disfagia, síndrome de Horner, parálisis de pares craneales (III, V, VI) e incluso rotura carotídea2,3.
El diagnóstico es fundamentalmente clínico y apoyado en las pruebas de imagen como la ecografía Doppler y la TC cervical con contraste. Ante la sospecha de trombosis de la vena yugular interna, la ecografía Doppler cervical es el estudio de primera línea, con una sensibilidad y especificidad muy elevadas. La ausencia de flujo al Doppler color y la falta de compresibilidad de la vena representan hallazgos de alta sensibilidad, mientras que el signo más específico es la visualización del trombo. La TC permite visualizar de forma completa la vena yugular interna, así como la posible extensión de la trombosis a las estructuras vasculares venosas del tórax5.
El tratamiento consiste en antibioterapia prolongada, de entre 4-6 semanas de duración, con adecuada cobertura para anaerobios, especialmente dirigidos contra Fusobacterium necrophorum4,7,8. Fusobacterium necrophorum ha demostrado ser sensible in vitro a antibióticos de amplio espectro, incluyendo penicilina, cloramfenicol, clindamicina y metronidazol; es resistente a los aminoglucósidos, aztreonam y trimetropin sulfametoxazol, y presenta una sensibilidad variable a cefalosporinas, eritromicina y tetraciclina1. Dentro de los estreptococos del grupo viridans, el grupo S. milleri o anginosus tiene en general los índices de resistencia antibiótica más bajos. Streptococus intermedius, agente etiológico de nuestro caso, es el que tiene menos resistencias a penicilina en nuestro medio6. La evolución, una vez iniciado el tratamiento antibiótico correcto, suele ser favorable en la mayoría de los pacientes7,9. La mortalidad actualmente con el uso de terapia antibiótica oscila entre el 4% y 22%8.
El papel de la anticoagulación en el síndrome de Lemierre es controvertido4,7,10. Los riesgos y beneficios del tratamiento anticoagulante en esta patología no se han evaluado adecuadamente en ensayos clínicos debido, en parte, a la baja incidencia de la enfermedad9. En la mayoría de los casos los pacientes evolucionan de forma favorable sin el uso de esta7. Además, existe el riesgo de que la anticoagulación pueda facilitar la diseminación de la infección4. Algunos autores sugieren que el uso de heparina se asocia con resolución más rápida del trombo de la vena yugular interna mientras que otros recomiendan usarla solo en casos de producción de nuevos émbolos sépticos a pesar de antibioterapia adecuada4,7.
En conclusión, si bien el cuadro clínico del síndrome Lemierre es muy característico, actualmente puede ser una entidad difícil de identificar de no estar familiarizado con ella, en parte debido a su baja incidencia. Sin embargo, debido a la potencial evolución fatal del cuadro resulta fundamental su reconocimiento.
CONFLICTO DE INTERESES
Los autores declaran no presentar conflictos de intereses en relación con la preparación y publicación de este artículo.
ABREVIATURAS
PCR: proteína C reactiva · PCT: procalcitonina · TC: tomografía computarizada.
BIBLIOGRAFÍA
- Montiel R, Quintero A, Hernández A, de Benito MT, García I, Tinoco I, et al. Síndrome de Lemierre. La enfermedad olvidada. Med Intensiva. 2005;29:437-40.
- Tellería A, Jiménez I, Susperregui I, Ramos J, Gutiérrez A. Síndrome de Lemierre. Med Intensiva. 2005;29:441-4.
- Cantero AM, Carrasco MC, Forte M, Bazo AV, Callejo J. Síndrome de Lemierre, una complicación grave de la sinusitis aguda. Actual Med. 2016;101:112-4.
- Andrade JT, San Martín JT, Grau C. Síndrome de Lemierre, secundario a otitis media aguda. Revisión a partir de un caso. Rev Otorrinolaringol Cir Cabeza Cuello. 2013;73:263-7.
- Maldonado I, Gutiérrez JM, Wilkens A, Weitz C, Rojas A, Varela C. Síndrome de Lemierre: una entidad clínica casi en el olvido. Reporte de tres casos y revisión de la literatura. Rev Chil Radiol. 2015;21:34-40.
- Alcaide F. Aspectos microbiológicos de los estreptococos del grupo viridans. En: Sociedad Española de Enfermedades Infecciosas y Microobiología Clínica [en línea] [consultado el 10/09/2019]. Disponible en www.seimc.org/contenidos/ccs/revisionestematicas/bacteriologia/SGVirid.pdf
- Ballesteros MM, Gil E, Medina C, Baquero M, Martínez A, Palomares JJ. Síndrome de Lemierre. An Pediatr (Barc). 2007;66:417-8.
- Winter M, Saavedra A, Grau C, Caro J. Síndrome de Lemierre, reporte de un caso. Rev Otorrinolaringol Cir Cabeza Cuello. 2013;73:164-8.
- Chirinos JA, García J, Alcaide ML, Toledo G, Baracco GJ, Lichtstein DM. Septic thrombophlebitis: diagnosis and management. Am J Cardiovasc Drugs. 2006;6:9-14.
- Karkos PD, Asrani S, Karkos CD, Leong SC, Theochari EG, Alexopoulou TD, et al. Lemierre’s syndrome: a systematic review. Laryngoscope. 2009;119:1552-9.