Vol. 16 - Num. 62
Grupo PrevInfad/PAPPS Infancia y Adolescencia
Suplementación de yodo en la gestación y lactancia
Carmen Rosa Pallás Alonsoa, Julia Colomer Revueltab, Olga Cortés Ricoc, M.ª Jesús Esparza Olcinad, José Galbe Sánchez-Venturae, Jaime García Aguadod, Ana Martínez Rubiof, José M.ª Mengual Gilg, Manuel Merino Moínah, Francisco Javier Sánchez Ruiz-Cabelloi, Javier Soriano Fauraj
aServicio de Neonatología. Hospital Universitario 12 de Octubre. Madrid. España.
bDepartamento de Pediatría, Obstetricia y Ginecología. Unidad de Pediatría. Universidad de Valencia. Valencia. España.
cPediatra. CS Canillejas. Madrid. España.
dPediatra. Madrid. España.
ePediatra. CS Torrero La Paz. Zaragoza. España.
fPediatra. CS de Camas. Sevilla. España.
gPediatra. CS Delicias Sur. Zaragoza. España.
hPediatra. CS El Greco. Getafe. Madrid. España.
iPediatra. CS Zaidín Sur. Granada. España.
jPediatra. CS Fuensanta. Valencia. España.
Correspondencia: CR Pallás. Correo electrónico: kpallas.hdoc@gmail.com
Cómo citar este artículo: Pallás Alonso CR, Colomer Revuelta J, Cortés Rico O, Esparza Olcina MJ, Galbe Sánchez-Ventura J, García Aguado J, et al. Suplementación de yodo en la gestación y lactancia. Rev Pediatr Aten Primaria. 2014;16:147-53.
Publicado en Internet: 30-06-2014 - Número de visitas: 26978
Resumen
El beneficio de la suplementación con yodo durante la gestación en las áreas con deficiencia grave de yodo está bien establecido. En el año 2004 la Organización Mundial de la Salud incluyó a España entre los países con adecuada ingesta de yodo y varios estudios recientes confirman que la ingesta de yodo es suficiente en la población española. Los profesionales españoles, sin embargo, se han encontrado con recomendaciones contradictorias, lo que ha generado confusión e incertidumbre en la práctica a seguir en cuanto a la suplementación de yodo a la mujer gestante o en periodo de lactancia. A los clínicos e investigadores les preocupa que las situaciones de déficit de yodo leve o moderado puedan relacionarse con un peor desarrollo de los niños, pero la suplementación rutinaria de yodo en la gestación no está exenta de riesgo. PrevInfad considera que, al tratarse de una medida profiláctica que afecta a dos individuos –madre e hijo– y que se aplica al conjunto de una población sana, debe primar el principio de precaución y que no existen pruebas de calidad suficiente para determinar el balance entre los beneficios y los riesgos de la suplementación farmacológica de yodo durante la gestación y la lactancia, por lo que sugiere que no se realice esta intervención.
Palabras clave
● Gestación ● Hormonas tiroideas ● Lactancia ● YodoIMPORTANCIA DEL YODO
El yodo es un elemento esencial para la producción de la hormona tiroidea y por tanto desempeña un papel fundamental en el crecimiento y desarrollo de los niños. La deficiencia grave de yodo en la gestación es causa de cretinismo y de daño cerebral irreversible en el niño. El beneficio de la suplementación con yodo durante la gestación en las áreas con deficiencia grave de yodo está bien establecido1. Sin embargo, en las regiones con deficiencia leve o moderada de este elemento, la evidencia de los beneficios solo se sugiere indirectamente por los resultados en los biomarcadores (aumento de la eliminación del yodo urinario, disminución del tamaño del tiroides materno y del recién nacido y disminución de la tiroglobulina neonatal), pero no hay ni un solo ensayo clínico que haya comunicado los resultados de la suplementación durante el embarazo en el desarrollo de los niños o en su crecimiento.
SITUACIÓN EN ESPAÑA
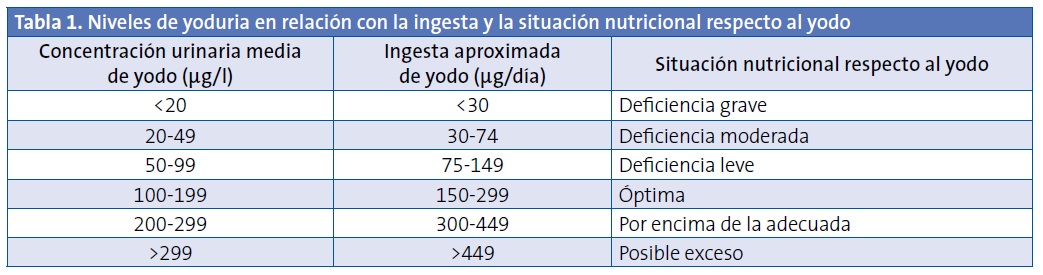
En el año 2004, la Organización Mundial de la Salud (OMS) incluyó a España entre los países con adecuada ingesta de yodo2. Varios estudios recientes realizados en niños3 y adultos4 muestran medianas de yoduria superiores a 100 µg/l, lo que confirma que la ingesta de yodo es suficiente en la población española. En la Tabla 1 se muestran los valores de yoduria más utilizados para definir la situación de una población con relación a la ingesta de yodo.
En octubre de 2012, la Dirección de Salud Pública del Gobierno Vasco y la Dirección General de Investigación y Salud Pública de la Generalidad Valenciana organizaron un taller sobre suplementación con yodo y ácido fólico durante la gestación y la lactancia5. Una de las recomendaciones finales de este taller fue: “En estos momentos, la suplementación universal con comprimidos de yoduro potásico durante la gestación y la lactancia materna no está justificada en España”. En este taller se consideró que el contenido de yodo de la leche, los derivados lácteos y la sal yodada cubre las necesidades de yodo en la gestación y la lactancia, siempre que la madre consuma estos alimentos en cantidad suficiente.
En gestantes, tres raciones de leche o derivados lácteos y 2 g de sal yodada cubren alrededor del 100% de las necesidades de yodo y en madres lactantes el 90%. A ello hay que añadir otras fuentes de yodo que proporcionan el resto de alimentos de la dieta, como el pescado.
Las leches y derivados lácteos con denominación de “ecológicos” no están suplementados con yodo, puesto que las vacas que producen esta leche no se alimentan con piensos suplementados. Por tanto, la suplementación farmacológica de yodo durante la gestación y la lactancia solo estaría indicada en mujeres con hábitos de alimentación que supongan alto riesgo de ingesta insuficiente de yodo o que presenten riesgo de desarrollar disfunción tiroidea en estas etapas.
Sin embargo, en un artículo posterior6 a la difusión de la recomendación anteriormente mencionada, el Grupo de Trabajo sobre Trastornos Relacionados con la Deficiencia de Yodo y Disfunción Tiroidea (TDY-DT) de la Sociedad Española de Endocrinología y Nutrición analiza la situación en España y hace una revisión de los estudios realizados en zonas de deficiencia de yodo leve o moderada. En las conclusiones finales, el Grupo de Trabajo TDY-DT incluye la siguiente recomendación: “En espera de alcanzar la meta de que la inmensa mayoría de la población gestante de nuestro país presente un adecuado estado nutricional de yodo, se mantiene la recomendación explícita de la prescripción de yoduro potásico antes de la gestación, si es posible, durante la gestación y en el periodo de lactancia”. Esta recomendación se apoya en el hecho de que existen numerosos estudios en España realizados en población gestante, previos7 y posteriores8-10 a la disponibilidad de suplementos de yoduro potásico, que muestran que las embarazadas, incluso las que consumen sal yodada, no consiguen alcanzar el adecuado estado nutricional de yodo requerido en la gestación. Por otro lado, en esta revisión del Grupo de Trabajo TDY-DT se refiere que la mayoría de los estudios realizados en nuestro país muestran que solo el 50% de los hogares consumen sal yodada, porcentaje aún muy alejado del 90 %, uno de los criterios de “yodosuficiencia” establecido por distintos organismos internacionales11.
Por lo tanto, los profesionales españoles, con una diferencia de poco más de seis meses, se han encontrado con recomendaciones muy diferentes en relación con una medida que afecta a una proporción importante de la población. Esto ha generado confusión e incertidumbre en la práctica a seguir en cuanto a la suplementación de yodo a la mujer gestante o en periodo de lactancia.
RESULTADOS DE LA SUPLEMENTACIÓN EN ZONAS CON DEFICIENCIA LEVE O MODERADA DE YODO
En la Tabla 2 se resume la información de los seis ensayos clínicos sobre la suplementación de yodo en la gestación y la lactancia, realizados en áreas con deficiencia leve o moderada de yodo12-17. En ninguno de estos estudios se refieren datos sobre la evolución de los niños, ni en relación con el crecimiento, ni sobre el desarrollo. Hasta este momento no se dispone de ninguna información de calidad sobre el efecto de la suplementación de yodo en la evolución de los niños. La información disponible se refiere a biomarcadores. Los datos sobre el desarrollo infantil provienen de estudios observacionales, algunos de ellos refieren una mejor evolución en los niños suplementados18.
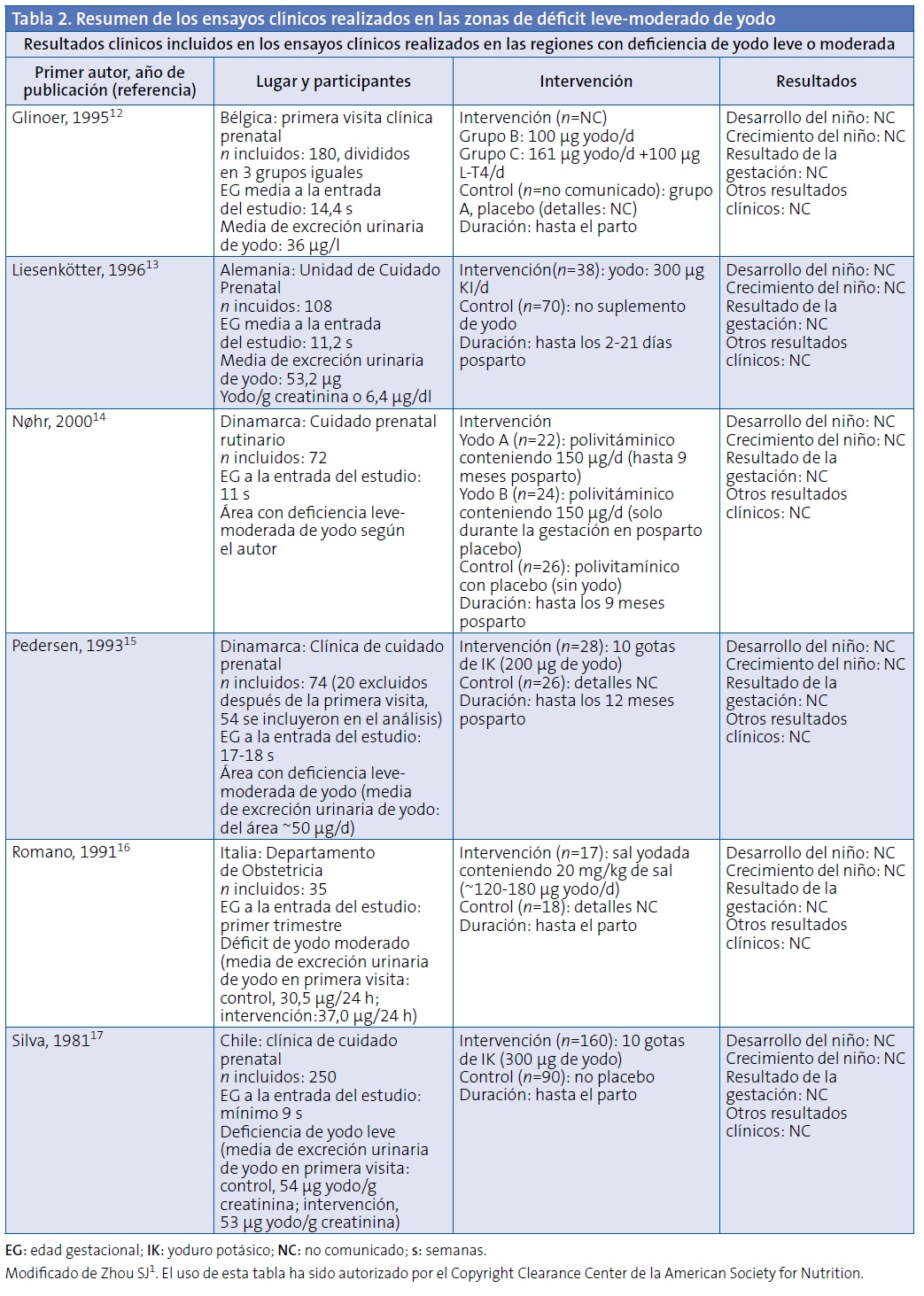
La suplementación de yodo aumenta la excreción urinaria de yodo, tanto en la madre como en el niño12-17. No se ha visto una clara relación dosis-respuesta. Los efectos de la suplementación en los niveles de hormona tiroidea de la madre y del niño no son consistentes. Se encontró aumento de tiroxina en uno de los cinco ensayos que lo evalúan, hormona tiroestimulante (TSH) más baja en las madres en uno de los seis estudios revisados y una reducción significativa de la tiroglobulina en sangre de cordón en los hijos de madres suplementadas en dos de los cuatro ensayos que lo estudian12,15,17.
A los clínicos e investigadores les preocupa que las situaciones de déficit de yodo leve o moderado puedan relacionarse con un peor desarrollo de los niños. Esta preocupación se fundamenta en los resultados de los estudios que muestran que los niveles de tiroxina bajos o la TSH alta en la gestación se asocian con coeficiente intelectual (CI) más bajo en los niños19,20. Sin embargo, un reciente ensayo clínico21, que incluyó a más de 21 000 mujeres, mostró que la corrección de los niveles de TSH o de tiroxina en la gestación no mejoraba el CI de los niños a los tres años. Que los resultados de los estudios observacionales no coincidan con los de los ensayos clínicos está ampliamente descrito y probablemente tenga que ver con factores de confusión que no siempre se identifican y por tanto no se pueden realizar los adecuados ajustes.
Actualmente, con los estudios disponibles, no se puede determinar si la suplementación con yodo durante la gestación y la lactancia tiene beneficios para los niños. Se están realizando dos ensayos clínicos en áreas de deficiencia leve o moderada de yodo que tienen previsto incluir la evolución de los niños22,23. Esta información será fundamental para establecer los beneficios reales de la suplementación prenatal.
RIESGOS DE LA SUPLEMENTACIÓN DE YODO EN ZONAS DE DEFICIENCIA LEVE O MODERADA DE YODO
La suplementación rutinaria de yodo en la gestación no está exenta de riesgos. El límite superior que puede considerarse seguro en la gestación no está establecido, ya que el tiroides fetal es vulnerable al exceso de yodo24. Se han descrito casos de hipotiroidismo congénito en recién nacidos hijos de madres que habían tenido una ingesta de yodo excesiva durante la gestación25,26.
Por otro lado, se ha comunicado que la suplementación de 150 µg/día en la gestación se asocia a un peor desarrollo de los niños27.
La posibilidad de que en áreas con deficiencia de yodo leve o moderada la suplementación de yodo durante la gestación pudiera incrementar la prevalencia de tiroiditis posparto y la autoinmunidad materna, parece que se ha descartado con los resultados de estudios recientes28-30.
A la vista de la información referida anteriormente, parece que la suplementación de yodo durante la gestación y lactancia no está exenta de riesgos, aunque la calidad de la información no permite establecer la magnitud de los mismos.
ASPECTOS ÉTICOS
La OMS y el International Council for the Control of Iodine Deficiency Disorders han establecido cuáles son los niveles de yoduria deseables para las mujeres gestantes (150-249 µg/l)11. Para conseguir estos niveles, parece que las mujeres gestantes de las zonas de deficiencia leve o moderada de yodo deberían recibir suplementos. Algunos autores31 dan tanto valor a estas recomendaciones, aunque ya se ha referido que en ningún caso se ha comunicado el posible beneficio en los niños, que consideran no ético que se hagan ensayos clínicos y que el grupo control no reciba suplemento de yodo. Por el contrario, otros autores32 insisten en que estos estudios son imprescindibles; de hecho, se están realizando dos, y refieren que en el Reino Unido no se recomienda la profilaxis durante la gestación y la lactancia y que no se establecerá la recomendación hasta que haya pruebas de calidad del beneficio de la suplementación farmacológica.
RECOMENDACIONES
A pesar de las recomendaciones nacionales e internacionales sobre la suplementación farmacológica de yodo en la gestación y la lactancia, el grupo PrevInfad no ha encontrado información de calidad que permita establecer un balance entre los beneficios y los riesgos de esta intervención. Probablemente, los resultados de las investigaciones que se están llevando a cabo aporten una información esencial que llevará a modificar las recomendaciones. PrevInfad considera que, al tratarse de una medida profiláctica que afecta a dos individuos –madre e hijo– y que se aplica al conjunto de una población sana, debe primar el principio de precaución.
Por lo tanto, PrevInfad considera que no existen pruebas de calidad suficiente para determinar el balance entre los beneficios y los riesgos de la suplementación farmacológica de yodo durante la gestación y la lactancia, y sugiere que no se realice esta intervención (recomendación débil en contrasegún la metodología GRADE).
ESTRATEGIA DE BÚSQUEDA
Cochrane Central Register of Controlled Trials (http://goo.gl/pFaPRU); EMBASE (www.embase.com); PubMed (www.ncbi.nlm.nih.gov/pubmed/).
("iodine"[MeSH Terms] OR "iodine"[All Fields] OR "iodides"[MeSH Terms] OR "iodides"[All Fields]) AND ("dietary supplements"[MeSH Terms] OR ("dietary"[All Fields] AND "supplements"[All Fields]) OR "dietary supplements"[All Fields] OR "supplementation"[All Fields]).
("iodine"[MeSH Terms] OR "iodine"[All Fields] OR "iodides"[MeSH Terms] OR "iodides"[All Fields]) AND ("pregnancy"[MeSH Terms] OR "pregnancy"[All Fields]).
("iodine"[MeSH Terms] OR "iodine"[All Fields] OR "iodides"[MeSH Terms] OR "iodides"[All Fields]) AND ("deficiency"[Subheading] OR "deficiency"[All Fields]).
("iodine"[MeSH Terms] OR "iodine"[All Fields] OR "iodides"[MeSH Terms] OR "iodides"[All Fields]) AND ("breast feeding"[MeSH Terms] OR ("breast"[All Fields] AND "feeding"[All Fields]) OR "breast feeding"[All Fields] OR "breastfeeding"[All Fields]).
CONFLICTO DE INTERESES
Los autores declaran no presentar conflictos de intereses en relación con la preparación y publicación de este artículo.
ABREVIATURAS: CI: coeficiente intelectual •OMS: Organización Mundial de la Salud •TDY-DT: Grupo de Trabajo sobre Trastornos Relacionados con la Deficiencia de Yodo y Disfunción Tiroidea de la Sociedad Española de Endocrinología y Nutrición •TSH: hormona tiroestimulante.
BIBLIOGRAFÍA
- Zhou SJ, Anderson AJ, Gibson RA, Makrides M. Effect of iodine supplementation in pregnancy on child development and other clinical outcomes: a systematic review of randomized controlled trials. Am J Clin Nutr. 2014;99:408-22.
- de Benoist B, Andersson M, Egli I, Takkouche B, Allen H (eds.). Iodine status worldwide. WHO Global Database on Iodine Deficiency. Geneva: WHO; 2004.
- Arena J, Emparanza JI. Study of iodine intake in children from 6 months to three years-old in Guipúzcoa. An Pediatr (Barc). 2012;76:65-8.
- Soriguer F, García-Fuentes E, Gutiérrez-Repisco C, Rojo-Martínez G, Velasco I, Goday A, et al. Iodine intake in the adult population. Di@bet.es study. Clin Nutr. 2012;31:882-8.
- Suplementación con yodo y ácido fólico durante el embarazo y la lactancia. Resumen y recomendaciones del taller llevado a cabo en Bilbao, el 30 de octubre de 2012 [en línea] [consultado el 14/10/2013]. Disponible en: http://goo.gl/g9y1bK
- Donnay S. Suplementación con yodo durante el embarazo y la lactancia. Toma de posición del Grupo de Trabajo de Trastornos relacionados con la Deficiencia de Yodo y Disfunción Tiroidea de la Sociedad Española de Endocrinología y Nutrición. Endocrinol Nutr. 2014;61:27-34.
- Donnay S. Rational use of potassium iodide during pregnancy and lactation. Endocrinol Nutr. 2008;55 Suppl 1:29-34.
- Soriguer F, Santiago P, Vila L, Arena JM, Delgado E, Díaz CF, et al. Clinical dilemmas arising from the increased intake oh iodine in the Spanish population and the recommendation for systematic prescription of potassium iodide in pregnant and lactating women. J Endocrinol Invest. 2009;32:184-91.
- Santiago P, Velasco I, Muela JA, Sánchez B, Martínez J, Rodríguez A, et al. Infant neurocognitive development is independent of the use of iodised salt or iodine supplements given during pregnancy. Br J Nutr. 2013;110:831-9.
- Julvez J, Álvarez-Pederol M, Rebagliato M, Murcia M, Forns J, García-Esteban R, et al. Thyroxine levels during pregnancy in healthy women and early child neurodevelopment. Epidemiology. 2013;24:150-7.
- World Health Organization, United Nations Children's Fund, and International Council for the Control of Iodine Deficiency Disorders. Assessment of Iodine Deficiency Disorders and Monitoring Their Elimination: A Guide for Programme Managers. 3rd ed. Geneva, Switzerland: World Health Organization; 2007.
- Glinoer D, De Nayer P, Delange F, Lemone M, Toppet V, Spehl M, et al. A randomized trial for the treatment of mild iodine deficiency during pregnancy: maternal and neonatal effects. J Clin Endocrinol Metab. 1995;80:258-69.
- Liesenkötter KP, Gopel W, Bogner U, Stach B, Gruters A. Earliest prevention of endemic goiter by iodine supplementation during pregnancy. Eur J Endocrinol. 1996;134:443-8.
- Nøhr SB, Jorgensen A, Pedersen KM, Laurberg P. Postpartum thyroid dysfunction in pregnant thyroid peroxidase antibody-positive women living in an area with mild to moderate iodine deficiency: is iodine supplementation safe? J Clin Endocrinol Metab. 2000;85:3191-8.
- Pedersen KM, Laurberg P, Iversen E, Knudsen PR, Gregersen HE, Rasmussen OS, et al. Amelioration of some pregnancy-associated variations in thyroid function by iodine supplementation. J Clin Endocrinol Metab. 1993;77:1078-83.
- Romano R, Jannini EA, Pepe M, Grimaldi A, Olivieri M, Spennati P, et al. The effects of iodoprophylaxis on thyroid size during pregnancy. Am J Obstet Gynecol. 1991;164:482-5.
- Silva JE, Silva S. Interrelationships among serum thyroxine, triiodothyronine, reverse triiodothyronine, and thyroid-stimulating hormone in iodine-deficient pregnant women and their offspring: effects of iodine supplementation. J Clin Endocrinol Metab. 1981;52:671-7.
- Riano Galán I, Sánchez Martínez P, Mosteiro Díaz P, Rivas Crespo MF. Psycho-intellectual development of 3 year-old children with early gestational iodine deficiency. J Pediatr Endocrinol Metab. 2005;18:1265-72.
- Julvez J, Álvarez-Pedrerol M, Rebagliato M, Murcia M, Forns J, García-Esteban R, et al. Thyroxine levels during pregnancy in healthy women and early child neurodevelopment. Epidemiology. 2013;24:150-7.
- Li Y, Shan Z, Teng W, Yu X, Li Y, Fan C, et al. Abnormalities of maternal thyroid function during pregnancy affect neuropsychological development of their children at 25-30 months. Clin Endocrinol (Oxf). 2010;72:825-9.
- Lazarus JH, Bestwick JP, Channon S, Paradice R, Maina A, Rees R, et al. Antenatal thyroid screening and childhood cognitive function. N Engl J Med. 2012;366:493-501.
- Melse-Boonstra A, Gowachirapant S, Jaiswal N, Winichagoon P, Srinivasan K, Zimmermann MB. Iodine supplementation in pregnancy and its effect on child cognition. J Trace Elem Med Biol. 2012;26:134-6.
- Australian New Zealand Clinical Trials Registry, ANZCTR. Pregnancy iodine and neurodevelopment in kids (PINK) [en línea] [consultado el 06/02/2013]. Disponible en: http://goo.gl/T5DQUs
- Pearce EN. Monitoring and effects of iodine deficiency in pregnancy: still an unsolved problem? Eur J Clin Nutr. 2013;67:481-4.
- Connelly KJ, Boston BA, Pearce EN, Sesser D, Snyder D, Braverman LE, et al. Congenital hypothyroidism caused by excess prenatal maternal iodine ingestion. J Pediatr. 2012;161:760-2.
- Crawford BA, Cowell CT, Emder PJ, Learoyd DL, Chua EL, Sinn J, et al. Iodine toxicity from soy milk and seaweed ingestion is associated with serious thyroid dysfunction. Med J Aust. 2010;193:413-5.
- Rebagliato M, Murcia M, Alvárez-Pedrerol M, Espada M, Fernández-Somoano A, Lertxundi N, et al. Iodine supplementation during pregnancy and infant neuropsychological development: INMA mother and child cohort study. Am J Epidemiol. 2013;177:944-53.
- Antonangeli L, Maccherini D, Cavaliere R, di Giulio C, Rein-hardt B, Pinchera A, et al. Comparison of two different doses of iodide in the prevention of gestational goiter in marginal iodine deficiency: a longitudinal study. Eur J Endocrinol. 2002;147:29-34.
- Nohr S, Jorgensen A, Pedersen KM, Laurberg P. Post-partum thyroid dysfunction in pregnant thyroid peroxidase antibody-positive women living in an area with mild to moderate iodine deficiency: is iodine supplementation safe? J Clin Endocrinol Metab. 2003;85:3191-8.
- Reinhard W, Kohl S, Hollmann D, Klapp G, Benker G, Reinwein D, et al. Efficacy and safety of iodine in the postpartum period in an area of mild iodine deficiency. Eur J Med Res. 1998;3:203-10.
- Stagnaro-Green A, Sullivan S, Pearce EN. Iodine supplementation during pregnancy and lactation. JAMA. 2012;308:2463-4.
- Bath SC, Jolly KB, Rayman MP. Iodine supplements during and after pregnancy. JAMA. 2013;309(13):1345.




