Vol. 13 - Num. 51
Grupo PrevInfad/PAPPS Infancia y Adolescencia
Promoción de la salud bucodental
I Vitoria Miñanaa, Grupo PrevInfad/PAPPS Infancia y Adolescenciab
aUnidad de Nutrición y Metabolopatías. Hospital La Fe. Valencia. España.
bJosé María Mengual Gil (coord.).
Cómo citar este artículo: Vitoria Miñana I, Grupo PrevInfad/PAPPS Infancia y Adolescencia. Promoción de la salud bucodental. Rev Pediatr Aten Primaria. 2011;13:435-58.
Publicado en Internet: 11-10-2011 - Número de visitas: 64049
Resumen
Los tres factores principales implicados en la caries son las bacterias, los azúcares y la susceptibilidad del huésped, mientras que los procedimientos más útiles como profilácticos de la misma son el empleo de flúor, las medidas dietéticas, la higiene dental y el tratamiento de las lesiones activas.
El flúor más efectivo para la prevención de la caries es el tópico administrado de forma continua. Este dato, junto con el conocimiento de que el exceso de flúor sistémico en la fase preeruptiva se asocia con la fluorosis dental hace que el cepillado dental con una pasta que contenga flúor es actualmente la medida más recomendable para la prevención de la caries. Es más importante la minuciosidad del cepillado dental que el tipo de técnica empleada.
Solamente se recomiendan suplementos de fluoruro si se pertenece a un grupo de riesgo de caries dental y la cantidad que debe administrarse está en función de la concentración de ion flúor del agua de consumo, ya que los alimentos no constituyen una fuente importante de flúor.
Los colutorios de fluoruro que se emplean para realizar enjuagues bucales diarios o semanales, deben recomendarse a partir de los seis años para asegurar que el niño no ingerirá el líquido.
La cariogenicidad de los azúcares depende más del tipo de hidrato de carbono y del tiempo de retención bucal que de la cantidad consumida, por lo que se desaconseja especialmente la ingesta de biberones durante el sueño.
Palabras clave
● Caries dental ● Flúor ● Salud bucodentalNota:
bGrupo PrevInfad (AEPap): J. Pericas Bosch, FJ. Sánchez Ruiz-Cabello, FJ. Soriano Faura, J. Colomer Revuelta, O. Cortés Rico, MJ. Esparza Olcina, J. Galbe Sánchez-Ventura, J. García Aguado, A. Martínez Rubio, M. Merino Moína, CR. Pallás Alonso.
Grupo PrevInfad de la AEPap, previnfad@aepap.org.
Introducción
La promoción de la salud bucodental infantil incluye la prevención primaria de la caries dental (CD), el tratamiento precoz de los traumatismos dentales, y la prevención primaria y el diagnóstico precoz de la maloclusión dentaria.
De los tres procesos, el más prevalente es la CD. Los últimos estudios epidemiológicos en preescolares españoles indican que, independientemente de la comunidad autónoma, casi el 20% de los niños tiene caries a los tres años y el 40% a los cinco años1. Afecta a la calidad de vida infantil, por producir dolor e infecciones que pueden desencadenar enfermedades sistémicas o la destrucción de la pieza dental. Las medidas de prevención primaria de la caries son más eficientes que las recomendaciones frente a las maloclusiones o los traumatismos2,3, por lo que nos dedicaremos con mayor profundidad a la CD.
La caries dental
Según la Organización Mundial de la Salud (OMS), la CD se puede definir como un proceso patológico, localizado, de origen externo, que se inicia tras la erupción y que determina un reblandecimiento del tejido duro del diente, evolucionando hacia la formación de una cavidad.
La caries se caracteriza por una serie de complejas reacciones químicas y microbiológicas que acaban destruyendo el diente. Se acepta que esta destrucción es el resultado de la acción de ácidos producidos por bacterias en el medio ambiente de la placa dental. Clínicamente, la caries se caracteriza por cambio de color, pérdida de translucidez y descalcificación de los tejidos afectos. A medida que el proceso avanza, se destruyen tejidos y se forman cavidades.
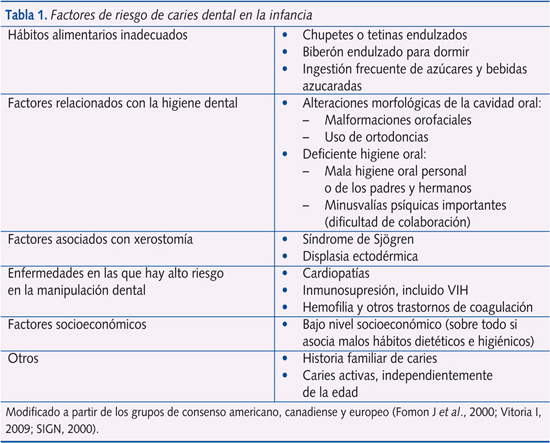
En cuanto a los grupos de riesgo de CD en la infancia, todos los niños pueden padecer CD, pero existen grupos de riesgo que tienen mayor probabilidad de desarrollarla (tabla 1).
Con respecto a las medidas de prevención de la CD, los procedimientos más útiles en la profilaxis de la caries se pueden agrupar en cuatro apartados: empleo de flúor (F), higiene bucodental, medidas dietéticas y tratamiento de las lesiones activas.
Empleo de flúor
Cuando se consume en cantidades óptimas, se consigue aumentar la mineralización dental y la densidad ósea, reducir el riesgo y prevalencia de la CD y ayudar a la remineralización del esmalte en todas las épocas de la vida.
Desde 1909 se conoce el efecto preventivo del F sobre la CD. Los trabajos de Cox, Dean y Armstrong4 permitieron concluir que el F aumentaba la resistencia a la CD, pero producía manchas en el esmalte, y que la concentración de 1 ppm de fluoruro en el agua se relacionaba con la máxima reducción de CD y el mínimo porcentaje de moteado dental. Este moteado dental se denominó más tarde fluorosis dental (FD) debido a su relación causal con el F5.
En las últimas décadas, la prevalencia de CD en los niños había disminuido en la mayoría de países industrializados. Esto se atribuyó al empleo de F tanto sistémico (agua de consumo, bebidas y alimentos) como tópico (dentífricos, geles, colutorios), así como a una mejoría del estado de nutrición y de la higiene dental6,7. Sin embargo, de nuevo se asiste a un aumento de prevalencia, posiblemente por un abandono de las medidas de salud pública anteriores8.
Mecanismos de acción del flúor
El mecanismo de acción del F es múltiple:
- Transformación de la hidroxiapatita (HAP) en fluoropatita (FAP), que es más resistente a la descalcificación. Esta reacción química entre la HAP y la FAP presenta una reversibilidad en función de la concentración de F en el entorno del esmalte dental, de modo que la FAP no sería una situación definitiva y estable9.
- Inhibición de la desmineralización y catálisis de la remineralización del esmalte desmineralizado. Este proceso es dinámico y dura toda la vida del diente. La reversibilidad de este mecanismo justifica, por un lado, la recomendación del empleo de F durante toda la vida y no solo durante la infancia. Además, el empleo de F tópico a bajas dosis, de forma continua, induce la remineralización dental10.
- Inhibición de las reacciones de glucólisis de las bacterias de la placa dental (sobre todo Streptococcus mutans), con lo que disminuye la formación de ácidos.
- Reducción de la producción de polisacáridos de la matriz extracelular en la placa dental11,12.
En todos los casos, parece que el factor más importante en la prevención de la CD es la exposición a dosis bajas pero continuadas de fluoruro en la cavidad oral.
Efectos sistémico y tópico del flúor (figura 1)
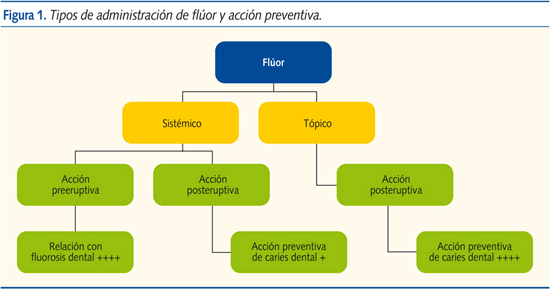
Efecto sistémico
- Preeruptivo. Tras su absorción intestinal y su paso a la sangre, el F se incorpora a la estructura mineralizada de los dientes en desarrollo y probablemente incrementa levemente la resistencia a la desmineralización frente a la acción de ácidos orgánicos, ya que solamente un 8-10% de los cristales del esmalte están compuestos por FAP en niños residentes en zonas con agua fluorada13. Al principio de la investigación sobre el F, este se creía que era el efecto más importante. Por ello se recomendaba dar F a la embarazada, así como antes de los seis meses de vida (antes de la erupción del primer diente) y se aconsejaba retirar los suplementos tras la erupción de la segunda dentición, pues no tendría sentido su administración tras el desarrollo dental.
- Posteruptivo. Tras la erupción dental, el F sistémico sigue estando poco implicado en la formación de la estructura orgánica dental. Tan solo la fracción excretada por saliva tendría una acción significativa protectora de CD10.
Efecto tópico (posteruptivo)
El F presente en la fase fluida de la superficie dental es el que realmente disminuye la desmineralización y aumenta la remineralización del esmalte, siendo clave la frecuencia de la exposición al F. Este efecto posteruptivo tópico es el que se cree más adecuado para prevenir la CD.
La saliva es el principal transportador del F tópico. La concentración de F en el ductus salivar tras la secreción de las glándulas salivares es bajo (0,016 ppm en zonas con agua fluorada y 0,0006 ppm en áreas con agua no fluorada)14. Esta concentración probablemente tenga una débil actividad cariostática. Sin embargo, la pasta dentífrica o los geles logran una concentración en la boca 100 a 1000 veces superior.
Así pues, con esta perspectiva, y a diferencia de lo que se creía inicialmente, se debe:
- Hacer más hincapié en los distintos medios de administración tópica del F.
- Recomendar el F tópico toda la vida y no solo restringir nuestras recomendaciones a la época del desarrollo y erupción dental.
- Desaconsejar el empleo de excesivo F sistémico, sobre todo antes de la erupción dental (en la embarazada y antes de los seis meses de vida).
- Insistir en el papel remineralizador de dosis bajas de F administradas de forma continua.
Fluorosis dental
La FD es la hipomineralización del esmalte dental por aumento de la porosidad. Se debe a una excesiva ingesta de F durante el desarrollo del esmalte antes de la erupción. La FD presenta una relación dosis-respuesta15. Así, en la FD leve hay estrías o líneas a través de la superficie del diente; en la FD moderada, los dientes son altamente resistentes a la CD pero tienen manchas blancas opacas, y en la FD severa, el esmalte es quebradizo, contiene manchas marrones y se acompaña de lesiones óseas.
El aumento de FD moderada en los últimos años se atribuye a la ingesta acumulada de F en la fase de desarrollo dental, aunque la gravedad depende no solo de la dosis sino también de la duración y el momento de la ingesta de F16. Las fuentes de F en esta época de la vida son la ingesta de la pasta dentífrica (sobre todo hasta los seis años de edad), el empleo inadecuado de los suplementos de F, la reconstitución de la fórmula para lactantes con agua fluorada y los alimentos y bebidas elaboradas con agua fluorada procedente de abastecimientos de agua de consumo público, por el efecto de difusión del F a los mismos.
No se cree que la fluoración del agua sea la causa más importante de la FD17,18. Así, los países con amplia tradición de fluoración de las aguas de consumo, como es el caso de EE. UU., tienen una prevalencia de FD en personas de 9-19 años del 22%, siendo la mayoría de tipo leve o muy leve y solo un 1% de tipo moderado o intenso19; la prevalencia de FD disminuye cuando se interrumpe la fluoración del agua20. La FD ha sido importante en los países con aguas fluoradas solo cuando el agua era la única fuente de exposición al F. En Europa, los mayores índices de FD se asocian con el F del agua y con el empleo de suplementos fluorados21. En España, la incidencia de FD media en 1994 fue del 2,3-5%, habiéndose descrito fluorosis solamente en Canarias22 y en niños refugiados saharianos que residen temporalmente en nuestro país por motivos humanitarios23.
Para poder prevenir la FD es necesario conocer que el desarrollo de cada una de las dos denticiones, temporal y definitiva, atraviesa tres fases: fase proliferativa, que se extiende desde la aparición de un engrosamiento del ectodermo oral o lámina dentaria hasta el inicio de la calcificación del germen; fase de calcificación; y fase de erupción.
La FD se produce por el acúmulo de F en el diente en la fase de calcificación preeruptiva, probablemente por una alteración en la actividad de los ameloblastos, de modo que interfiere la aposición de cristales de calcio dando lugar a hipocalcificaciones. A partir de los ocho años se calcifican los últimos dientes definitivos (terceros molares). Así pues, esta edad supone el límite hasta el cual existe un riesgo teórico de FD de la dentición permanente24. Sin embargo, la mayoría de los grupos de consenso sobre la administración de F establece el límite superior real en seis años, ya que uno de los factores más importantes como es la ingesta de la pasta dentífrica desaparece a esta edad, pues ya hay una adecuada coordinación del reflejo de deglución25,26. Además, a los seis años los únicos dientes que quedan susceptibles a la FD son muy posteriores, por tanto, no habría una afectación estética importante.
En definitiva, la FD puede ser prevenida si se enfoca la administración de F sistémico por edades (menores de 2-3 años, de tres a seis años y mayores de seis años), pues en los 2-3 primeros años es cuando no hay que sobrepasar las dosis recomendadas de F para evitar la FD de las piezas, que se verán tras la erupción. A partir de los tres años, si hay FD, el problema estético sería menor, pues afectaría a los premolares y molares. Sin embargo, en los primeros años también debe prevenirse la caries de las piezas de la dentición temporal, tanto por el biberón nocturno como por el consumo de azúcares.
El debate actual entre exceso de F sistémico como factor de riesgo de FD (problema estético) frente a la falta de F como factor de riesgo de CD (problema infeccioso) ha llevado a numerosos autores a plantear el debate de si no estaremos primando demasiado los factores estéticos de una parte de la población frente a un problema médico de otra parte de la sociedad27.
En resumen, y en relación a la acción preventiva del F, actualmente se acepta que:
- El F tópico administrado tras la erupción dental es el principal responsable de la acción preventiva de la CD.
- El exceso de F sistémico administrado antes de los seis años es un factor importante responsable de FD.
Modos de administración del flúor
La administración de F puede realizarse de forma sistémica o tópica. La administración sistémica puede, a su vez, hacerse de modo colectivo (fluoración del agua potable) o individual. La aplicación tópica también puede realizarse mediante preparados concentrados (geles, barnices), colutorios o pastas dentífricas (figura 2).
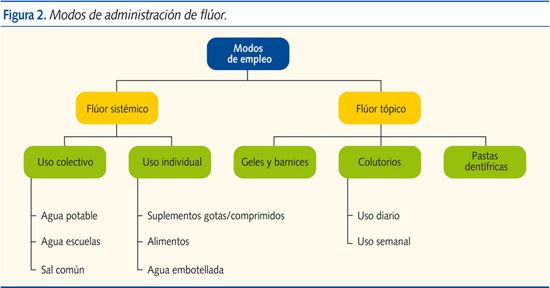
Flúor sistémico colectivo
La fluoración artificial del agua de consumo público ha sido la medida más eficaz y económica para la profilaxis colectiva de la CD, ya que no necesita cooperación diaria y consciente de los interesados. Aprobada por numerosas organizaciones internacionales, tales como la OMS y la Federación Dental Internacional, entre otras, ha sido utilizada en más de 39 países desde los años 40, beneficiándose cerca de 246 millones de personas. Inicialmente se le atribuyó una reducción de la incidencia de caries de un 40-50% si se trataba de la dentición de leche y de un 50-60% en el caso de la dentición definitiva28. Estudios más recientes cifran estos descensos entre un 18 y un 40%17, ya que habría otros factores implicados en la reducción de la caries.
En España hay plantas de fluoración en algunas poblaciones tales como Córdoba, Sevilla, Badajoz, algunas ciudades del País Vasco, Girona, Linares y Lorca.
Así pues, la fluoración del agua continúa siendo la medida más efectiva y la mejor elección como actuación de Salud Pública si hay una prevalencia elevada de CD. Sin embargo, en poblaciones con baja prevalencia de CD y con alternativas de F bien instauradas, la fluoración del agua no es ya la única opción.
El motivo del aumento de FD en los países con aguas fluoradas artificialmente se atribuye además a la amplia difusión de dentífricos y colutorios muy ricos en F. Por tanto, son los países más desarrollados los que más riesgo tienen de padecer FD, ya que hay mayores cantidades de alimentos elaborados con agua fluorada y mayor higiene dental (más F tópico que puede ser ingerido).
Cuando no se fluorura el agua de consumo público por no haber una red centralizada del agua, se puede recurrir a la fluoración de la sal común (200 mg F/kg), medida poco útil en la infancia ante la necesidad de realizar una prevención global de las enfermedades cardiovasculares. Asimismo, la fluoración del agua de las escuelas se ha empleado en el caso de viviendas aisladas. Hay que controlar mucho mejor el nivel de fluoruros añadidos, ya que el consumo se realiza solamente unos días determinados.
La leche fluorada artificialmente, utilizada en algunos programas preventivos en Suiza y países del este europeo, permite la absorción más lentamente que en el caso del agua, probablemente por la unión del F a los iones del calcio y al mayor pH gástrico por la capacidad tampón de la leche. Sin embargo, la menor importancia del F sistémico, junto con la dificultad en saber la dosis finalmente ingerida, ha hecho abandonar este tipo de medida preventiva25.
Flúor sistémico individual. Suplementos orales de fluoruros
Los suplementos orales de fluoruro (SOF) se establecieron para ofrecer F a comunidades donde no se podía fluorar el agua. Por ello, la cantidad de suplemento administrada se realiza en función de la concentración de ion F del agua de consumo. Para conocer el nivel de F en una comunidad concreta puede recurrirse a la bibliografía29 o a las Consejerías de Salud o de Medio Ambiente de las comunidades autónomas.
El fluoruro sódico (FNa) se absorbe entre un 90 y un 97% si se toma sin alimentos. La biodisponibilidad desciende hasta un 53,7% cuando se toma con leche y otros productos lácteos. Se distribuye tanto de forma libre como unido a proteínas y se deposita en los dientes, así como en el tejido óseo. La semivida de distribución es de una hora. Se excreta fundamentalmente a nivel renal. Así pues, los SOF deben administrarse en ayunas y alejados de las tomas de productos lácteos, para evitar la precipitación de fluoruro cálcico. Pueden usarse gotas desde los seis meses al año o los dos años, continuando después con comprimidos. Para aprovechar el papel tópico del F, lo ideal sería darlo en forma de comprimidos masticables o comprimidos que al chuparse se disuelvan lentamente25,26. En el caso de querer utilizar una fórmula magistral, esta se puede preparar con 110 mg de FNa en 1 l de agua, de modo que 5 ml contienen 0,25 mg de ion F.
Postura de los distintos grupos o comités de consenso frente a los suplementos orales de flurouro
- Academia Americana de Pediatría (AAP). En primer lugar, la AAP, al apoyar las recomendaciones para el uso del F en la prevención y control de la CD en EE. UU.18, sigue indicando las dosis que estableció conjuntamente con la Asociación Dental Americana en 1995 (tabla 2)30, en las que se indica el empleo de SOF desde los seis meses hasta los 16 años en función del F del agua de consumo. Estas recomendaciones eran más restrictivas que las previas, en las que se indicaba el límite máximo de 0,7 en vez de 0,6 mg/l (o ppm) de F en el agua, como la cifra a partir de la cual no habría que dar SOF. Además, se empezaba al nacimiento y se acababa a los 13 años. Sin embargo, en una revisión reciente de la Academia Americana de Dentistas Pediátricos se recomienda una valoración individual del riesgo de CD antes de prescribir un suplemento de F31, y en una publicación conjunta con la Academia Americana de Pediatría también se indica que la administración de todas las modalidades de F debe estar basada en la valoración individual del riesgo de CD32. En la embarazada no se recomienda la administración de F sistémico, ya que hay una baja efectividad preeruptiva y no se ha demostrado que atraviese la placenta.
- Comité de Nutrición de la Sociedad Canadiense de Pediatría. Por su parte, el Comité de Nutrición de la Sociedad Canadiense de Pediatría26 es más restrictivo en cuanto a las dosis e indicaciones de los SOF. Así, y tal como se observa en la tabla 2, no se ofrecen SOF a los niños que consumen agua con más de 0,3 mg/l de F, independientemente de la edad. Pero, además, indica que los SOF se administren solo si el niño no se cepilla (o lo hacen sus padres) los dientes dos veces al día o si el niño pertenece a un grupo de riesgo de CD. Además, añaden en sus recomendaciones que el niño visite al dentista antes del primer año de vida y que los padres deben ser informados de los riesgos y beneficios que el empleo de F puede suponer a largo plazo. Para el consenso canadiense, la efectividad de los SOF en la prevención de la CD es baja en la edad escolar y no está bien establecida en lactantes26.
- Asociación Europea de Dentistas Pediátricos. Por último, la Asociación Europea de Dentistas Pediátricos25 aún es más restrictiva y propone un esquema de dosificación en el que solo se emplean SOF a partir de los dos años de vida y hace hincapié en que únicamente se deben dar si hay riesgo aumentado de CD (tabla 2).
Todas estas limitaciones en las recomendaciones sobre el empleo de los SOF se relacionan con la probabilidad que tienen de producir FD. Sin embargo, es importante que el pediatra no olvide que hay niños en los que sí que hay que administrar SOF por pertenecer a grupos de riesgo. Una aproximación a los posibles grupos de riesgo se indica en la tabla 1, basada en criterios de los distintos comités antes indicados18,25,26,32.
Recomendaciones del grupo PrevInfad sobre los suplementos de flúor
Tras los comentarios anteriores y según el informe más reciente de la Asociación Dental Americana sobre recomendaciones de SOF33, el grupo PrevInfad recomienda SOF en los niños que pertenecen a grupos de riesgo en las cantidades indicadas por la AAP30,32 y que se indican en la tabla 2.
En el caso de administrar SOF, los medicamentos comercializados en nuestro país se indican en la tabla 3.
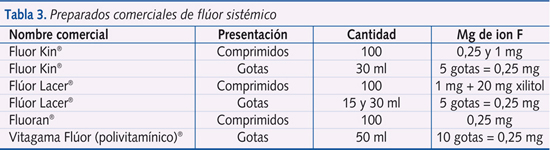
¿Cuál es la cantidad adecuada de ingesta diaria de flúor en el lactante?
Si el problema de la FD se restringe al niño pequeño, debemos conocer con exactitud cuáles son las necesidades de F. Las dietary reference intakes (DRI) para el F hacen referencia a las recomendaciones nutricionales que pueden usarse para planificar y valorar dietas en personas sanas. En el caso del F se han establecido dos tipos de DRI: las ingestas adecuadas (IA) y el nivel de ingesta máximo tolerable (NIMT)34. Estos valores suponen unos valores aproximados de 0,05 mg/kg/día para la IA y de 0,1 mg/kg/día para el NIMT.
Tal como se indica en la tabla 4, la ingesta diaria total de F viene determinada fundamentalmente por la concentración de F en el agua con la que se preparan las comidas y la leche de fórmula. La leche humana contiene de 0,005 a 0,01 mg/l, la fórmula reconstituida contiene unos 0,14 mg/l34 y los alimentos que constituyen la base de una alimentación variada aportan entre 0,2 y 0,77 mg35. Las frutas, los vegetales, las carnes y pescados aportan poco F. La mayoría de los vegetales y la carne contienen menos de 1 mg/kg de fluoruros en estado seco. En cambio, el té puede contener hasta 150 mg/kg y algunos pescados (enlatados y ahumados sobre todo) y mariscos pueden llegar a tener 20 mg/kg. Ninguno de ellos, no obstante, constituye una parte importante de la dieta en la infancia.
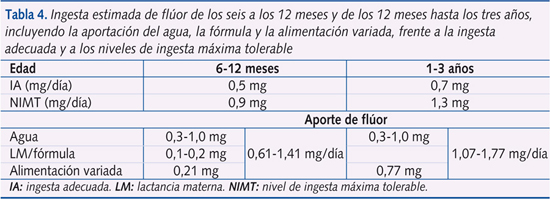
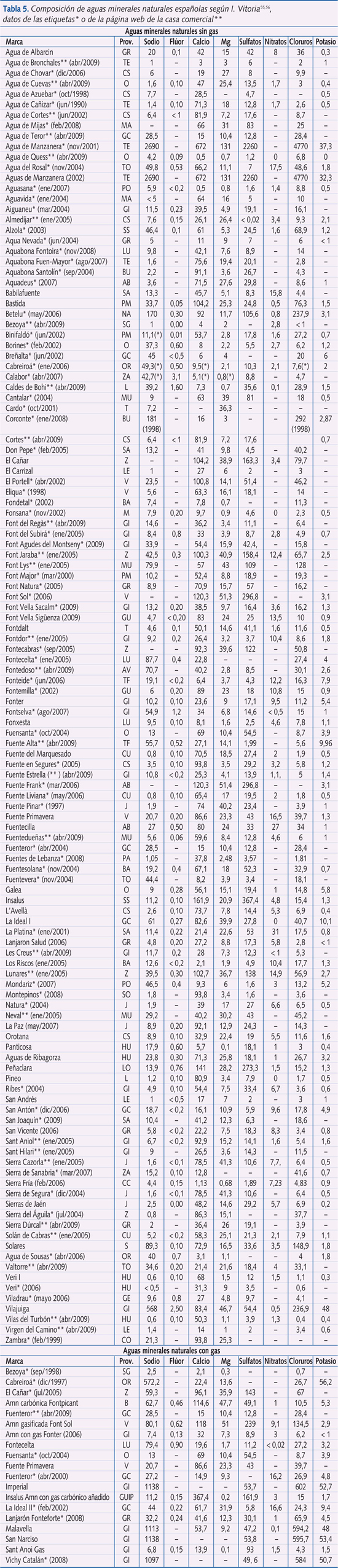
Del mismo modo, basándose en el NIMT de F para evitar la FD y en el contenido que aportan la leche artificial y la alimentación complementaria, Fomon36 concluye que en el primer año de vida el agua debe contener menos de 0,3 mg/l de F, reservándose la posibilidad de dar suplementos de F, especialmente para los niños con riesgo de presentar caries a partir de los seis meses, como indica la AAP. Sin embargo, a partir del primer año de edad y dado que los niveles máximos tolerables son más elevados, no habría ningún inconveniente en recomendar la bebida de agua fluorada (hasta 1 mg/l de F) para aprovechar el efecto tópico y continuado de la bebida. Así pues, si el niño toma agua de bebida envasada, se debe conocer la concentración en F del agua empleada (tabla 5), para lo que se puede recurrir a una base de datos actualizada on-line, como www.aguainfant.com, disponible para aguas españolas.
Aplicación tópica de flúor
Durante mucho tiempo se creyó que el efecto protector del F se debía a su incorporación a los cristales de apatita, de modo que aumentaría la resistencia del esmalte. Esta idea es más teórica que real. La acción protectora del F se manifiesta en una disminución de la desmineralización y un aumento de la remineralización de las lesiones incipientes, para lo que es importante contar con suficiente F en la superficie dental, de ahí la importancia del F tópico38,39.
Aplicación tópica de geles y barnices con elevada concentración de flúor
Constituyen procedimientos restringidos al estomatólogo. Su frecuencia debe ser adaptada por el dentista en función del grado de riesgo de CD del niño.
Los geles se aplican mediante cubetas ajustables a las arcadas dentales. Se utiliza FNa al 2% con una concentración de 9040 ppm de F o geles de fluorofosfato acidulado al 1,2% con un contenido de 12 000 ppm de F. Para evitar intoxicaciones, se recomienda no llenar más de un 40% de la cubeta; el paciente debe permanecer sentado con la cabeza inclinada hacia delante; y aspirar entre las dos cubetas durante todo el proceso.
Los geles se aplican, en general, una vez al año en los pacientes con riesgo elevado de CD. En una reciente revisión Cochrane, basada en 14 ensayos clínicos controlados, se concluye que los geles pueden reducir un 21% el índice CAO (dientes cariados, ausentes y obturados)40.
Los barnices de F tienen una consistencia viscosa. Se aplican sobre la superficie de los dientes con un pincel o una sonda curva. El Duraphat® contiene un 5% de FNa, lo que supone una concentración de ion F del 2,26%. Endurecen en presencia de la saliva. Estudios realizados, en países tanto en vías de desarrollo como desarrollados, han demostrado su utilidad en los niños con riesgo elevado de CD, ya que proporciona concentraciones más elevadas de F en la saliva a las dos horas de su empleo que el resto de tipos de F tópico. Son de fácil aplicación y útiles en niños con minusvalías psíquicas o físicas y que no vayan a tolerar la cubeta con gel en la boca. Asimismo, permiten aplicar el F en zonas seleccionadas del diente. En la correspondiente revisión Cochrane, basada en nueve ensayos clínicos controlados, se concluye que los barnices pueden llegar a producir una reducción de fracción prevenida del índice CAO hasta en un 46% (la fracción prevenida es el descenso de caries en el grupo tratado, expresado como porcentaje del grupo control) y el índice CAO (dentición temporal) un 33%40.
Los geles y barnices de F son un método efectivo de administración tópica de F para el Departamento de Salud Pública de EE. UU. y el grupo diana serían las personas de alto riesgo de CD (tabla 1).
Colutorios
Se emplean soluciones diluidas de sales de F con las que se realizan enjuagues bucales diarios o semanales. Deben recomendarse a partir de los seis años para asegurarnos de que el niño no ingerirá el líquido41.
Para uso diario, puede emplearse una solución de FNa al 0,05% con la que se enjuagará durante un minuto con unos 10 ml de colutorio, evitando su ingestión posterior. Como alternativa, puede practicarse un enjuague semanal de FNa al 0,2%, aconsejándose no ingerir nada en la siguiente media hora. Este último tipo de colutorio es el que suele emplearse en los programas escolares de prevención comunitaria de la CD. El empleo de colutorios fluorados es un método efectivo de administración tópica de F (evidencia I, nivel de recomendación A, para el consenso canadiense)26.
El empleo de colutorios fluorados es un método efectivo de administración tópica de F.
Higiene bucodental
El cepillado
Antes de que erupcionen los primeros dientes se debe empezar con la estimulación oral para acostumbrar al bebé a la manipulación de la boca e instaurar un hábito precoz. La limpieza debe hacerse una vez al día, aprovechando el momento del baño. Para esta etapa se pueden utilizar dedales de silicona o una gasa humedecida en agua.
Después de que erupcionen los primeros dientes se debe comenzar con la limpieza bucodental dos veces al día. Para esta etapa se pueden utilizar dedales de silicona o cepillos dentales infantiles42,43.
Después de que erupcionen los primeros molares primarios, alrededor de los 18 meses, se debe optar por el uso del cepillo dental. El cepillo debe presentar un mango recto y largo; una empuñadura gruesa, cerdas suaves con las puntas redondeadas y un tamaño compatible con la boca del niño.
La técnica debe ser sencilla para los padres. Se recomienda limpiar las superficies dentales laterales (linguales y vestibulares) con movimientos circulares y las superficies masticatorias con movimientos antero-posteriores. La posición del adulto debe permitir una buena visibilidad de la boca, manteniendo la cabeza del niño en una posición estable.
Se explicará al niño y a los padres (hasta la adolescencia) la técnica del cepillado. Es más importante la minuciosidad que el tipo de técnica empleada; con un cepillado minucioso la mayoría de las técnicas resultan eficaces. Si hay problemas de alineación, ausencia de dientes, prótesis bucales o el niño es torpe para cepillarse, es preciso recomendar técnicas especiales. Se debe recomendar un cepillo de cabeza pequeña, de cerdas sintéticas y puntas redondeadas para evitar la lesión de la encía si el niño lo usa con fuerza44.
El cepillado debe comenzar con un barrido siguiendo el eje del diente, empezando por la encía y sin desplazamientos horizontales, tanto en la cara exterior como en la cara interior. Posteriormente se realiza un movimiento a modo de remolino sobre la cara oclusal, de atrás hacia delante, limpiando posteriormente con suavidad la lengua. Debe enjuagarse varias veces.
El cepillado debe completarse en algunos casos con el empleo de seda dental, particularmente para las áreas interproximales y mesiales de los primeros molares permanentes. Para ello se emplea hilo compuesto de fibras microscópicas de nylon no enceradas, facilitando la operación el uso de pinzas especiales. En cualquier caso, el empleo de colorantes diagnósticos de la placa dental (eritrosina o fluoresceína sódica) permite su eliminación completa.
El dentífrico
El uso de un dentífrico adecuado aumenta los beneficios del cepillado. En general, una pasta dentífrica se compone de un producto abrasivo y un agente cariostático. Se recomiendan abrasivos suaves (pirofosfato de calcio, metafosfato insoluble de sodio, etc.) y compuestos fluorados, como se ha indicado anteriormente.
La utilización de dentífricos fluorados es el método más recomendado para la prevención de la CD, tanto por el aspecto tópico y continuado de su aplicación, como por la aceptación social de la higiene dental mediante el cepillado dental.
En cuanto a su concentración en F, las pastas dentífricas fluoradas carecen prácticamente de contraindicaciones en el adulto por su acción exclusivamente local. Sin embargo, se ha calculado que un preescolar, con dos cepillados diarios, puede deglutir alrededor de 1 g de pasta dental al día, debido a la inmadurez del reflejo de deglución. Por ello y para evitar la FD, debe conocerse la concentración de F de los dentífricos a emplear en el niño45,46. En este sentido, en el etiquetado no siempre consta la concentración en ppm de fluoruro, que se puede calcular fácilmente (2,2 g de NaF = 1000 mg de ion fluoruro = 9,34 g de PO3FK2 = 7,6 g de PO3FNa2).
Así se ha calculado la concentración en F de dentífricos españoles, lista que está actualizada on-line en www.aguainfant.com (tabla 6).
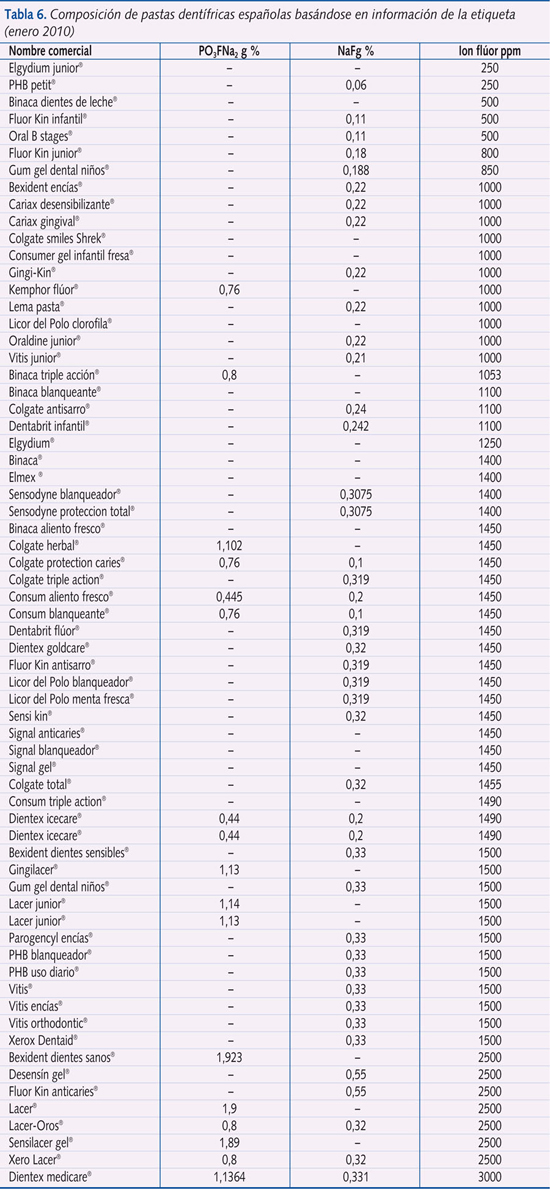
Según las investigaciones más recientes, las pastas con menos de 1000 ppm no parece que tengan ningún papel en la prevención de la caries dental47. Sin embargo, en niños pequeños el riesgo de ingestión de la pasta dentífrica es muy alto48. En niños menores de 2-3 años el cepillado deben realizarlo los padres, para hacerlo progresivamente el propio niño49. Las recomendaciones clínicas para el uso de pasta de dientes con F son las siguientes50:
- Hasta los dos años se recomienda la pasta que puede ponerse como “raspado o mancha sobre el cepillo” de pastas con 1000 ppm.
- Entre los dos y los seis años, con una pasta de dientes con entre 1000 y 1450 ppm de F y la cantidad similar a un guisante.
- Por encima de los seis años, dos veces al día con una pasta de dientes con 1450 ppm de F y la cantidad de 1-2 cm (sobre el cepillo).
El empleo de pastas dentífricas fluoradas es un método efectivo de administración tópica de F. El grupo de personas al que se dirige es a toda la población.
Los niños deben cepillarse sus dientes dos veces diarias con pasta fluorada51 y los mayores de seis años deben escupir la pasta pero sin enjuagarse excesivamente la boca con agua44.
Compatibilidad de las aplicaciones de flúor sistémico y tópico
No está justificado emplear a la vez más de una forma de aplicación sistémica (por ejemplo, agua de bebida fluorada y suplementos de F en comprimidos) para evitar el riesgo de fluorosis. Sin embargo, sí se pueden combinar varias formas de F tópico (por ejemplo, dentífricos, colutorios y geles), pero siempre a partir de una edad en la que nos aseguremos de que el niño no se tragará el F tópico, como puede ser los seis años.
Medidas dietéticas: hidratos de carbono
Los efectos cariógenos de cualquier azúcar derivan, sobre todo, de su capacidad de favorecer el crecimiento de ciertas bacterias y de su subsecuente formación de ácidos y polisacáridos. Probablemente, la sacarosa es el glúcido que más favorece la caries por el hecho de que su hidrólisis en glucosa y fructosa se sigue de la liberación de una elevada energía de hidrólisis, que se aprovecharía para la polimerización de la propia molécula de glucosa en glucanos, los cuales tienen un elevado coeficiente de adhesividad.
Otros hidratos de carbono con capacidad cariógena son la glucosa y el almidón; este último, cuyas fuentes son los cereales y las legumbres, resulta más perjudicial tras su modificación por los procesos de refinado industrial.
Así pues, los alimentos con mayor potencial cariógeno son los que contienen azúcares refinados y sobre todo pegajosos, teniendo en cuenta que la frecuencia de su ingestión es más importante que la cantidad ingerida de una vez.
Por tanto, y dado que el tipo de hidratos de carbono y el tiempo de retención bucal son más importantes que la cantidad consumida, se debe:
- Evitar las ingestas frecuentes entre comidas, así como la retención de alimentos azucarados en la boca (biberón para dormir y chupete endulzado).
- Procurar que los carbohidratos sean en forma diluida o acuosa (retención mínima), evitando los azúcares de textura pegajosa o adhesiva.
- Evitar utilizar los caramelos como regalos entre las comidas.
- Los refrescos azucarados entre las comidas son una fuente no despreciable de azúcares.
En resumen: los azúcares y bebidas o refrescos azucarados deben restringirse en la infancia a las comidas para conseguir una mayor prevención de la caries, evitando sobre todo su ingesta entre las comidas y al acostarse44,54.
Otras medidas dietéticas
Los chicles sin azúcar que contienen xilitol y sorbitol tienen propiedades anticaries a través de la producción de saliva. El xilitol es más efectivo por su añadida capacidad antibacteriana52.
El consumo de chicles sin azúcar puede ser beneficioso para la prevención de la caries, sobre todo, los que contienen xilitol.
Hasta hace unos años, los medicamentos para niños se endulzaban para que fuesen más fáciles de tomar. Sin embargo, no debe despreciarse tampoco este aporte de azúcar, pues puede ser una fuente añadida iatrógena de caries53.
Los pediatras deben prescribir medicamentos sin azúcar cuando sea posible.
Tratamiento de lesiones activas
El tratamiento de las lesiones activas debe efectuarse en la dentición caduca y en la permanente, pues se reduce la colonización bacteriana y el riesgo de destrucción para los dientes sanos. Es una medida especializada reservada al estomatólogo. La rápida formación de nuevas caries o la destrucción acelerada de piezas ya dañadas obliga a exámenes periódicos de la dentadura por parte del odontólogo.
Traumatismos dentales
A los 12 años, cerca de una cuarta parte de los niños han sufrido las consecuencias de traumatismos dentales, principalmente a nivel de los incisivos superiores.
Es importante tratar de reimplantar el diente lo más pronto posible, según el proceso siguiente: sostener el diente por la corona, no tocar la raíz; enjuagarlo con una solución salina o con agua, preferiblemente estéril; reimplantar inmediatamente el diente de modo suave; acudir al odontólogo.
Si no se ha podido reimplantar el diente, enviar al niño al odontólogo llevando el diente en un medio húmedo como leche o suero fisiológico.
Maloclusiones dentales
La distribución desigual de la presión de la mandíbula y el maxilar superior, como consecuencia de la mala alineación de los dientes, da lugar a una oclusión incorrecta de la dentición.
Se detecta haciendo deglutir al niño con la boca cerrada, para que así los dientes estén en oclusión. Normalmente los dientes de la arcada inferior quedan situados por dentro de los superiores.
Hay varios tipos de maloclusiones:
- Maloclusión del plano anteroposterior: clase I: la oclusión es normal, pero los dientes no están bien alineados en la arcada; clase II: la arcada inferior está retrasada con relación a la superior, y clase III: la arcada inferior está adelantada respecto a la superior.
- Maloclusión del eje vertical o axial: cuando uno o varios dientes exceden, pasan la línea de oclusión (sobre mordida), o por el contrario no llegan a ella (mordida abierta).
- Maloclusión en el eje transversal: las caras externas o vestibulares de las coronas de las piezas superiores están por dentro de las inferiores.
Hay causas que son prevenibles y en las que la educación sanitaria puede ser importante: evitar el empleo prolongado del chupete y evitar la succión del pulgar o la succión labial.
Resumen de actividades de promoción de la salud bucodental
De 0 a 2 años
- Exploración neonatal de la cavidad oral (dientes neonatales, malformaciones u otras alteraciones).
- Seguimiento de la erupción de la dentición primaria. Se considerará anormal la falta de erupción de la primera pieza a los 15 meses y la erupción de dientes malformados. Asimismo, se considerará anormal la falta de alguna pieza (20 en total) a los 30 meses.
- Profilaxis de la caries:
- Prevención de la caries rampante de los incisivos: se desaconsejará firmemente endulzar el chupete y dejar dormir al niño con un biberón de leche o zumo en la boca.
- Solamente si se pertenece a un grupo de riesgo de CD se darán suplementos de F por vía oral a partir de los seis meses, según el contenido del agua de bebida, ya sea agua de consumo público o embotellada.
- Inicio del cepillado dental. En niños menores de dos años, el cepillado deben realizarlo los padres con una pasta de dientes que contenga 1000 ppm de F y una cantidad similar a un “raspado o mancha” sobre el cepillo dental.
- Información a los padres sobre alimentos cariógenos. Se debe informar de que:
- La sacarosa es el hidrato de carbono más cariógeno.
- Los azúcares complejos, como los almidones y otras sustancias presentes en las legumbres y los cereales, son menos cariógenos, sobre todo en estado no refinado.
- Es más importante la frecuencia de las tomas que la cantidad total ingerida.
- Los azúcares con textura pegajosa o blanda son más cariógenos que los líquidos o duros.
- Vigilar la aparición de:
- Gingivitis (por falta de cepillado, maloclusiones, medicaciones).
- Maloclusiones (mordida abierta) evitando hábitos perjudiciales (chupete, succión del pulgar).
De 2 a 6 años
- Exploración de la dentición primaria. Se derivarán al odontólogo aquellos niños con piezas cariadas, según la disponibilidad de los recursos sanitarios.
- Profilaxis de la caries y de la enfermedad periodontal:
- Información a los padres sobre alimentos cariógenos.
- Inicio del cepillado dental. A partir de los dos años se aconsejará a los padres que se cepillen los dientes por la noche en presencia del niño. Este se "cepillará" también para ir adquiriendo el hábito y posteriormente alguno de los padres repasará el cepillado limpiando cuidadosamente los restos de comida. Entre los dos y seis años, el niño se cepillará con un dentífrico con entre 1000 y 1450 ppm de F en cantidad similar a un guisante. Deberá cepillarse al menos dos veces al día y de forma especial antes de acostarse.
- Aplicación de F: suplementos orales solamente si se pertenece a un grupo de riesgo de CD y en función del contenido de F en el agua de bebida, y F tópico (compatible con suplementos orales de F).
De 6 a 14 años
- Exploración bucal: presencia de sarro, flemones, abscesos, gingivitis, caries, mordida cruzada, mordida anterior, diastemas y frenillos, maloclusiones y apiñamientos. Se derivará al niño al odontólogo cuando presente alguna caries en las piezas definitivas, o bien cuatro o más en las dentición primaria. También se derivarán las hipoplasias de esmalte y las maloclusiones.
- Profilaxis de la caries y la enfermedad periodontal:
- Solamente si se pertenece a un grupo de riesgo de CD se darán suplementos de F por vía oral, según el contenido de F en el agua, ya sea agua de consumo público o embotellada.
- Colutorios diarios (0,05% FNa) o semanales (0,2%), recomendables para realizar en el colegio, estrategia que asegura su aplicación. Hay que comprobar que el niño hace bien el colutorio durante un minuto y que no se traga el líquido, (en general, a partir de los seis años). En los siguientes 30 minutos no debe ingerir nada.
- Geles y barnices de F: aplicados siempre por especialistas con periodicidad variable, en función del riesgo de caries.
- Cepillado dental después de las comidas y al acostarse con una pasta dentífrica que contenga 1450 ppm de F y la cantidad de 1-2 cm (sobre el cepillo).
Enlaces de interés en salud bucodental en Internet
- Portal Web sobre agua y salud: www.aguainfant.com
- Visión didáctica de los dientes y la caries dental: www.caries.info/cariologia.htm
- Recursos didácticos para reforzar el hábito de la higiene dental en niños: http://clic.xtec.cat/db/act_es.jsp?id=1089
- Páginas oficiales de la OMS; datos epidemiológicos de muchos países: www.who.int/ncd/orh/index.htm y www.whocollab.od.mah.se/
- Recomendaciones de la CDC norteamericana sobre la prevención de la caries: www.cdc.gov/mmwr/preview/mmwrhtml/rr5014a1.htm
Bibliografía
- Bravo Pérez M, Llodra Calvo JC, Cortés Martinicorena FJ, Casals Peidró E. Encuesta de Salud Oral de Preescolares en España 2007. RCOE. 2007;12:143-68.
- American Academy of Pediatrics. Policy Statement. Section on Pediatric Dentistry. Oral Health Risk Assessment Timing and Establishment of the Dental Home [consultado el 08/02/2010]. Disponible en http://aappolicy.aappublications.org/cgi/reprint/pediatrics;111/5/1113.pdf
- García Sábada JI, López Pérez P, Badillo C, Cabello A, Lozano M. Evaluación de la efectividad de un programa de educación bucodental en centros escolares. Arch Odontoestomatol Prev Comunit. 1997;13:755-64.
- OMS. Fluoruros y salud. Serie de monografías n.º 59.1.ª ed. Ginebra: OMS; 1972.
- Browne D, Whelton H, O’Mullane D. Fluoride metabolism and fluorosis. J Dent. 2005;33:177-86.
- Amid I, Hasson H. Fluoride supplements, dental caries and fluorosis: A systematic review. J Am Dent Assoc. 2008;139;1457-68.
- Sheiham A. Dietary effects on dental diseases. Public Health Nutr. 2001;4:569-91.
- Bagramian RA, García-Godoy F, Volpe AR. The global increase in dental caries. A pending public health crisis. Am J Dent. 2009;22:3-8.
- Hellwig E, Lennon AM. Systemic versus topical fluoride. Caries Res. 2004;38:258-62.
- Robinson C. Fluoride and the caries lesion: interactions and mechanism of action. Eur Arch Paediatr Dent. 2009;10:136-40.
- Marquis RE, Clock SA, Mota-Meira M. Fluoride and organic weak acids as modulators of microbial physiology. FEMS Microbiol Rev. 2003;26:493-510.
- Clarkson JJ, McLoughlin J. Role of fluoride in oral health promotion. Int Dent J. 2000;50:119-28.
- American Dietetic Association. The impact of fluoride on health. J Am Diet Assoc. 2000;100:1208-13.
- Oliveby A, Twetman S, Ekstrand J. Diurnal fluoride concentration in whole saliva in children living in a high-and a low-fluoride area. Caries Res. 1990;24:44-7.
- Bronckers AL, Lyaruu DM, DenBesten PK. The impact of fluoride on ameloblasts and the mechanisms of enamel fluorosis. J Dent Res. 2009;88:877-93.
- Marinho VC. Evidence-based effectiveness of topical fluorides. Adv Dent Res. 2008;20:3-7.
- Parnell C, Whelton H, O’Mullane D. Water Fluoridation. Eur Arch Paediatr Dent. 2009;10:141-8.
- Centers for Disease Control and Prevention. Recommendations for using fluoride to prevent and control dental caries in the United States. MMWR Recomm Rep. 2001;50(RR-14):1-42.
- Beltran-Aguilar ED, Griffin SO, Lockwood SA. Prevalence and trends in enamel fluorosis in the United States from the 1930s to the 1980s. J Am Dent Assoc. 2002;133:157-65.
- Clark DC, Shulman JD, Maupome G, Levy SM. Changes in dental fluorosis following the cessation of water fluoridation. Community Dent Oral Epidemiol. 2006;34:197-204.
- Cochran JA, Ketley CE, Arnadóttir IB, Fernandes B, Koletsi-Kounari H, Oila AM et al. A comparison of the prevalence of fluorosis in 8-year-old children from seven European study sites using a standardized methodology. Community Dent Oral Epidemiol. 2004;32(Suppl 1):28-33.
- Gómez-Santos G, González-Sierra MA, Vázquez-García-Machiñena J. Evolution of caries and fluorosis in schoolchildren of the Canary Islands (Spain): 1991, 1998, 2006. Med Oral Patol Oral Cir Bucal. 2008;13:E599-608.
- Almerich-Silla JM, Montiel-Company JM, Ruiz-Miravet A. Caries and dental fluorosis in a western Saharan population of refugee children. Eur J Oral Sci. 2008;116:512-7.
- Abanto JA, Rezende KM, Marocho SM, Alves FB, Celiberti P, Ciamponi AL. Dental fluorosis: Exposure, prevention and management. Med Oral Patol Oral Cir Bucal. 2009;14(2):E103-7.
- European Academy of Paediatric Dentistry Guidelines on the use of fluoride in children: an EAPD policy document. Eur Arch Paediatr Dent. 2009;10:129-35.
- Nutrition Committee, Canadian Paediatric Society. The use of fluoride in infants and children. Paediatr Child Health. 2002;7:569-72.
- Marthaler TM. Dentistry between pathology and cosmetics. Community Dent Oral Epidemiol. 2002;30:3-15.
- Brunelle JA, Carlos JP. Recent trends in dental caries in U.S. children and the effect of water fluoridation. J Dent Res.1990;69(special issue):723-7.
- Vitoria I, Arias T. Importancia nutricional del agua de consumo público y del agua de bebida envasada en la alimentación del lactante. Estudio descriptivo de base poblacional. IV Premio Especial Nestlé. Barcelona: Ed. Asociación Española de Pediatría; 2000.
- American Academy of Pediatrics, Committee on Nutrition. Fluoride supplementation for children: interin policy recommendations. Pediatrics. 1995;95:777.
- American Academy on Pediatric Dentistry. Guideline on fluoride therapy. Pediatr Dent. 2008;30(Suppl):121-4.
- American Academy of Pediatrics. Section on Pediatric Dentistry and Oral Health. Preventive oral health intervention for pediatricians. Pediatrics. 2008;122:1387-94.
- Rozier RG, Adair S, Graham F, Iafolla T, Kingman A, Kohn W et al. Evidence-based clinical recommendations on the prescription of dietary fluoride supplements for caries prevention: a report of the American Dental Association Council on Scientific Affairs. J Am Dent Assoc. 2010;141:1480-9.
- Institute of Medicine. Fluoride. In: Dietary reference intakes for calcium, phosphorus, magnesium, vitamin D, and fluoride. Washington, DC: National Academy Press; 1997. p. 288-313.
- Taves DR. Dietary intake of fluoride ashed (total fluoride) v. unashed (inorganic fluoride) analysis of individual foods. Br J Nutr. 1983;49:295-301.
- Fomon SJ, Ekstrand J, Zieglesr EE. Fluoride intake and prevalence of dental fluorosis: Trends in fluoride intake with special attention to infants. J Pub Health Dent. 2000;60:131-9.
- Vitoria I. Agua de bebida en el niño. Recomendaciones prácticas. Acta Pediatr Esp. 2009;67:255-66.
- Vitoria I. El flúor y la prevención de la caries en la infancia. Actualización. Rev Pediatr Aten Primaria. 2002;15:95-126.
- Cuenca E, Martínez I. Uso racional del flúor. En: Cuenca E, Manau C, Serra LL (eds.). Odontología preventiva y comunitaria, 2.ª ed. Barcelona: Masson; 1999. p. 109-28.
- Marinho VC, Higgins JP, Logan S, Sheiham A. Fluoride gels for preventing dental caries in children and adolescents (Review). Cochrane Database of Systematic Reviews 2002;2:CDO002280.
- Poulsen S. Fluoride-containing gels, mouth rinses and varnishes: an update of evidence of efficacy. Eur Arch Paediatr Dent. 2009;10:157-61.
- Palma C, Cahuana A, Gómez L. Guía de orientación para la salud bucal en los primeros años de vida. Acta Pediatr Esp. 2010;68:351-7.
- American Academy of Pediatrics. Policy Statement: Preventive Oral Health Intervention for Pediatricians. Pediatrics. 2008;122:1387-94.
- Scottish Intercollegiate Guidelines Network Preventing Dental Caries in Children at High Caries Risk Targeted prevention of dental caries in the permanent teeth of 6-16 year olds presenting for dental care. SIGN. 2000;47:1-33. Disponible en www.show.scot.nhs.uk/sign/pdf/sign47.pdf
- Stephen KW. Fluoride prospects for the new millenium-community and individual patient aspects. Acta Odontol Scand. 1999;57:352-5.
- Riordan PJ. Dental fluorosis decline alter changes to supplement and toothpaste regimens. Community Dent Oral Epidemiol. 2002;30:233-40.
- Walsh T, Worthington HV, Glenny AM, Appelbe P, Marinho VC, Shi X. Fluoride toothpastes of different concentrations for preventing dental caries in children and adolescents. Cochrane Database Syst Rev. 2010;20:CD007868.
- Twetman S. Caries prevention with fluoride toothpaste in children: an update. Eur Arch Paediatr Dent. 2009;10:162-7.
- Ellwood RP, Cury JA. How much toothpaste should a child under the age of 6 years use? Eur Arch Paediatr Dent. 2009;10:168-74.
- Sociedad Española de Odontopediatría (SEO). Documento de consenso de la European Academy of Paediatric Dentistry (EAPD) y la SEO. Protocolo para el uso del flúor en niños [consultado el 11/09/2011]. Disponible en www.odontologiapediatrica.com/img/EAPD_Fluoride_Guideline_%28Spanish%29%5B1%5D.pdf
- Marinho VC. Cochrane reviews of randomized trials of fluoride therapies for preventing dental caries. Eur Arch Paediatr Dent. 2009;10:183-91.
- Mäkinen KK, Bennett CA, Hujoel PP, Isokangas PJ, Isotupa KP, Pape HR Jr et al. Xylitol chewing gums and caries rates: a 40-month cohort study. J Dent Res.1995;74:1904-13.
- Maguire A, Rugg-Gunn A, Butler TJ. Dental health of children taking antimicrobial and non-antimicrobial liquid oral medication long-term. Caries Res. 1996;30:16-21.
- Vitoria I. Flúor y prevención de las caries en la infancia. Actualización 2002. Rev Pediatr Aten Primaria. 2002;15:95-126.
CONFLICTO DE INTERESES
Los autores declaran no presentar conflictos de intereses en relación con la preparación y publicación de este artículo.