Vol. 19 - Num. 75
Originales
¿Es posible el manejo ambulatorio de la invaginación intestinal?
Paula Ortolá Fortesa, Anna Domènech Tàrregaa, Patricia Rodríguez Iglesiasa, Lucía Rodríguez Caraballoa, Cinta Sangüesa Nebotb, Juan José Vila Carbóa
aServicio Cirugía Pediátrica. Hospital Universitario y Politécnico La Fe. Valencia. España.
bServicio de Radiodiagnóstico. Hospital Universitario y Politécnico La Fe. Valencia. España.
Correspondencia: P Ortolá. Correo electrónico: paula.ortola.fortes@gmail.com
Cómo citar este artículo: Ortolá Fortes P, Domènech Tàrrega A, Rodríguez Iglesias P, Rodríguez Caraballo L, Sangüesa Nebot C, Vila Carbó JJ. ¿Es posible el manejo ambulatorio de la invaginación intestinal? Rev Pediatr Aten Primaria. 2017;19:231-9.
Publicado en Internet: 04-07-2017 - Número de visitas: 29842
Resumen
Introducción: la invaginación intestinal es la causa más frecuente de obstrucción intestinal en menores de tres años. Habitualmente, tras la desinvaginación, los pacientes permanecen ingresados 24-48 horas. Recientemente se ha propuesto el manejo ambulatorio mediante observación clínica durante 12 horas. Nuestro objetivo es valorar la implementación de esta actitud terapéutica.
Material y métodos: revisión retrospectiva de las invaginaciones intestinales atendidas en nuestro centro durante los últimos 12 años.
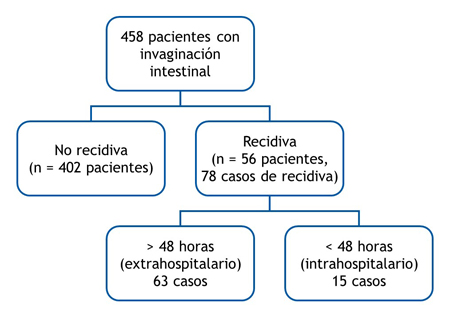
Resultados: se incluye 458 pacientes, el 60,3% de ellos varones. Edad media de 24,1 meses, siendo la localización ileocólica la más frecuente (77,7%). El 2,4% presentó alguna causa secundaria. Se realizó neumoenema en 370 niños, requiriendo cirugía el 10,7%. Se registraron 78 recidivas en 56 pacientes (12,2%), 15 de ellos intrahospitalariamente. El tiempo medio para la reintroducción de la alimentación y la estancia media fueron de 28,6 y 64,4 horas respectivamente, sin diferencias significativas entre aquellos que recidivaron y los que no (60,8 frente a 69 horas; t = -0,4; p = 0,689).
No se registraron diferencias entre el tiempo de evolución clínica y la tasa de éxito del neumoenema (t = 0,478; p = 0,634); aunque hubo diferencias en la necesidad de intervención quirúrgica (χ² = 5,604; p = 0,018), no hubo ninguna complicación. La reintroducción precoz de la alimentación no se relacionó con más recidivas ni diferencias entre los grupos (30,2% en el grupo que recidivó y 23,1% en el grupo sin recidiva, p = 0,608).
Conclusiones: el ingreso hospitalario más allá de 12 horas no disminuye la tasa de complicaciones. Por tanto, consideramos que la observación en urgencias tras la desinvaginación durante 12 horas es una medida segura y coste-efectiva.
Palabras clave
● Ecografía ● Invaginación intestinal ● Neumoenema ● Niños ● Recurrencia ● Tratamiento ambulatorio
INTRODUCCIÓN
La invaginación intestinal es la causa más frecuente de obstrucción intestinal en pacientes pediátricos menores de tres años, pudiendo ocurrir a cualquier edad1-8. Consiste en la introducción o deslizamiento de parte del intestino dentro de otra porción intestinal distal al mismo4,5,7. Su incidencia es de uno a cuatro de cada 1000 niños aproximadamente, siendo mayor entre los 3 y 12 meses de edad (0,6 a 1 de cada 1000)2,4,5. La afectación en varones es más frecuente y la relación niño:niña es de entre 1,2:1 y 2,4:1, según la serie consultada2,5.
En el 60-90% de los casos la etiología es idiopática1,2,5,7,8, habiéndose sugerido la hipótesis infecciosa/inflamatoria como causante de una hiperplasia linfoide intestinal que favorecería el desarrollo de esta entidad3,5,6,9. Aunque menos frecuentes (< 10-12%), determinadas patologías deben ser descartadas como causa secundaria por su importancia: divertículo de Meckel, linfoma intestinal, quiste de duplicación intestinal, celiaquía, fibrosis quística o púrpura de Schönlein-Henoch, entre otras3,5,7-14.
En la mayoría de los pacientes la localización de la invaginación es ileocólica y, con menor frecuencia, ileoileal, colocólica o rectosigmoidea (Tabla 1)2,6.
| Tabla 1. Localización y frecuencia de la invaginación intestinal en la población general y en la muestra estudiada | ||
|---|---|---|
| Tipo de invaginación | Población general (%) | Muestra estudiada (%) |
| Ileocólica | 60-90 | 77,7 |
| Ileoileal | 5-10 | 10,5 |
| Colocólica | < 5 | < 1 |
| Rectosigmoidea | < 1 | < 1 |

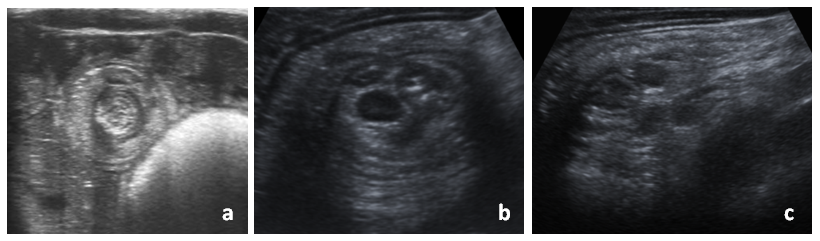
Los pacientes presentan característicamente crisis de dolor abdominal con encogimiento de piernas, seguidas de un periodo de decaimiento. Esto puede ir acompañado de irritabilidad, vómitos, inapetencia y/o deposiciones sanguinolentas (en jalea de grosella)2,3,5,10,13. En el proceso diagnóstico, además de la clínica –que es el pilar principal–, la radiología tiene un papel muy importante. La ecografía, fundamentalmente, y la radiografía simple de abdomen proporcionan imágenes características (en forma de diana, donut o pseudoriñón) (Figs. 1 y2), muy útiles para la identificación de esta patología, así como para su localización y estudio de posibles complicaciones15-20.
| Figura 1. Imágenes ecográficas de invaginación intestinal: a) corte sagital de una invaginación intestinal ileoileal (imagen en diana o donut); b) corte sagital de una invaginación ileocólica, con adenopatías en su interior; c) corte longitudinal de una invaginación ileocólica (imagen en pseudorriñón) |
|---|
 |

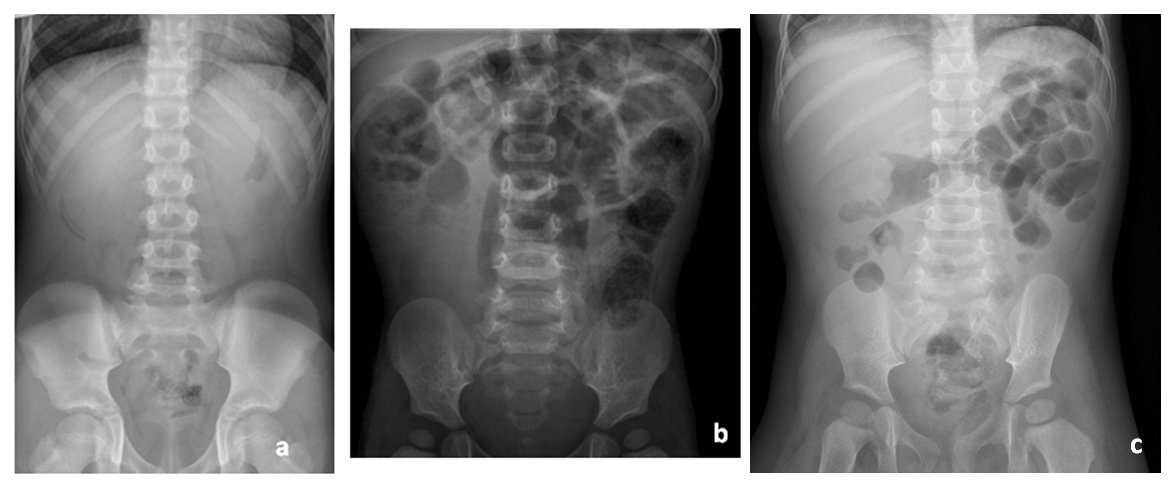
| Figura 2. Radiografía de abdomen en pacientes con invaginación intestinal: a) silencio abdominal; b) ausencia de aireación intestinal en flanco derecho; c) cabeza de invaginación intestinal a nivel de ángulo hepático |
|---|
 |

Es esencial no demorar el tratamiento sintomático de estos pacientes, basado en la administración de analgesia y fluidoterapia. Además, una vez confirmado el diagnóstico, se procederá al tratamiento etiológico en los casos que así lo precisen. Actualmente, el tratamiento más empleado para la reducción de la invaginación intestinal ileocólica no complicada es el neumoenema, basado en la introducción controlada de aire a través del ano para reducir la invaginación, lo que evita en muchos pacientes la necesidad de cirugía. Esto se realiza bajo control radiológico, hasta observar el paso de aire más allá del punto afectado, habitualmente la válvula ileocecal15-19. En los últimos años este procedimiento se realiza en la mayoría de los centros bajo sedación, pues al relajar la musculatura lisa se minimiza el tiempo del procedimiento, la presión necesaria para la reducción y la dosis de radiación recibida por el paciente21,22. Esta técnica tiene un porcentaje de éxito del 70-90% y tasas de complicación inferiores al 1%, siendo la perforación intestinal la más frecuente. En los casos complicados, con causa secundaria conocida o en los que el tratamiento conservador con neumoenema no ha sido efectivo (tras tres intentos habitualmente), está indicada la cirugía15-20. La tasa de pacientes que finalmente requieren dicha intervención se sitúa en torno al 10-30%, según la literatura médica15,19. En estos pacientes el procedimiento puede consistir únicamente en la reducción de la invaginación mediante maniobras manuales de taxis o puede requerir incluso resección intestinal por sufrimiento de asas.
La recidiva se produce en un 8-15% de los casos1,5,7,10,15,16,18, siendo más común en las primeras 24-48 horas debido a la inflamación subyacente. Por ello, la tendencia actual en la mayoría de centros es mantener a los pacientes ingresados durante este tiempo, reintroduciendo la alimentación oral previa al alta. Sin embargo, con el objetivo de reducir las molestias del paciente y sus familiares, así como optimizar los recursos sanitarios, cada vez son más los especialistas y las publicaciones que sugieren que la observación en Urgencias tras la reducción de la invaginación, durante un periodo no superior a 12 horas, es una actitud segura y coste-efectiva, pues no se ha descrito peor evolución en los casos que recurren tras el alta hospitalaria1. Existen protocolos de introducción precoz de la alimentación (fast-track o early oral feeding), basados en la introducción de alimentación oral transcurridas entre 6 y 12 horas de la intervención y empleados también en otro tipo de patologías quirúrgicas, que favorecen la implementación de esta medida sin aumentar las complicaciones ni las recurrencias23-25.
Nuestro objetivo es analizar diferentes características de los episodios de invaginación, incluidas las recidivas, y la evolución de los mismos con el fin de obtener datos fiables que permitan actualizar el protocolo de tratamiento de esta entidad.
MATERIAL Y MÉTODOS
Estudio retrospectivo realizado entre enero de 2004 y diciembre de 2015 que recoge todos los casos de invaginación intestinal en pacientes menores de 15 años atendidos en nuestro centro (hospital terciario, especializado en pacientes pediátricos, en Valencia, España).
Para el diagnóstico radiológico se empleó un ecógrafo (Siemens 2000) con transductor con sonda lineal de alta frecuencia (9-4 MHz o 18-6 MHz). En los casos de invaginación intestinal ileocólica no complicada el Servicio de Radiología Infantil practicó neumoenema, en presencia del servicio de Cirugía Pediátrica y Anestesia Infantil, utilizando una sonda Foley 24 Ch rectal y llenando el balón con 20-22 cc de aire.
Se estudió a los pacientes en función de si habían tenido episodios de recidiva o un único episodio de invaginación intestinal, comparando variables cuantitativas con categóricas mediante el test t de Student y las cualitativas entre ellas con χ². En todas ellas, el análisis estadístico se realizó con un intervalo de confianza del 95% (Excel® 2010, SPSSS® versión 20).
RESULTADOS
Se evaluaron 458 pacientes (60,3% varones y 39,7% mujeres). La edad media en el primer episodio fue de 24,1 meses (desviación estándar [DE] 24,6, rango 0-151,6), registrándose 379 casos (82,8%) en menores de tres años. Más de la mitad (53,7%) fueron remitidos desde otro centro médico y el tiempo medio de evolución del cuadro hasta la consulta en nuestro centro fue de 29,7 horas (DE 35,5; rango 1-336).
Como exploraciones complementarias en el momento agudo, la radiografía de abdomen se empleó en el 81,7% de los pacientes y la ecografía en el 99,6% de los mismos, siendo diagnósticas en el 88,7% y 91,3%, respectivamente. Además, se solicitó de forma ambulatoria gammagrafía con 99 mTc-pertecnetato en un 5% de los casos, con el objetivo de descartar divertículo de Meckel, siendo positivo en uno de ellos.
La localización ileocólica fue la más frecuente (356 casos, 77,7%), seguida por el tipo ileoileal (48 casos, 10,5%). Otros tipos fueron colocólica y rectosigmoidea (Tabla 1).
En todos los pacientes, el tratamiento inicial fue dieta absoluta, fluidoterapia y analgesia. En nuestra serie, 370 pacientes (80,8%) se trataron con neumoenema, siendo exitoso el primer intento en el 91,1% de ellos (media de intentos 1,2, rango: 1-4 (Tabla 2). Las presiones máximas alcanzadas fueron de 120-140 mmHg en los pacientes no sedados y 70-80 mmHg en los sedados, notándose una caída brusca de la misma en el momento en que se producía la desinvaginación. No hubo ninguna complicación derivada de este procedimiento.
| Tabla 2. Número de intentos de neumoenema (hasta reducción de la invaginación o indicación de cirugía) | ||
|---|---|---|
| Número de intentos | Frecuencia | Porcentaje (%) |
| 1 | 337 | 91,1 |
| 2 | 13 | 3,5 |
| 3 | 17 | 4,6 |
| 4 | 3 | 0,8 |
| Total | 370 | 100 |

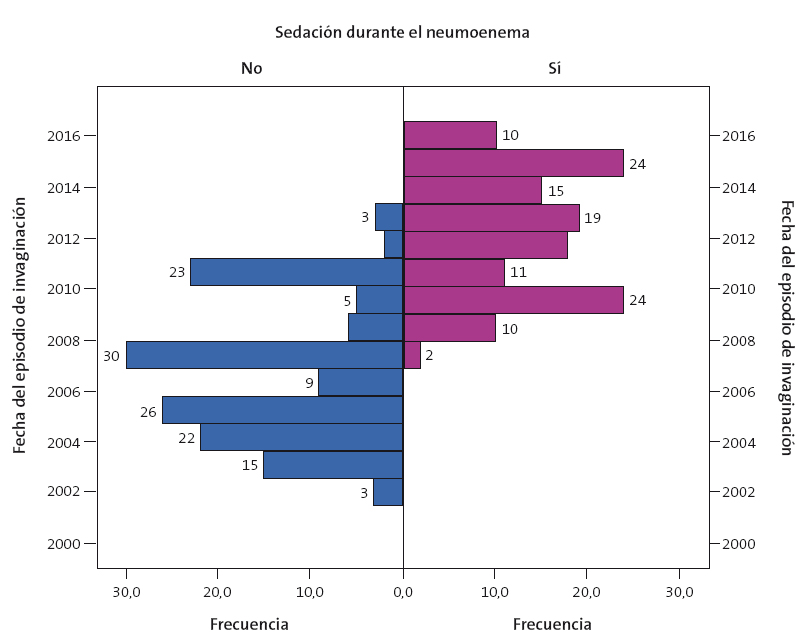
De forma general, a lo largo de los años que abarca el estudio, se empleó sedación durante el procedimiento en el 48,2% de los pacientes. No obstante, analizando los episodios registrados por años, puede verse que en los últimos cinco el porcentaje de neumoenemas realizados bajo sedación ha ido en aumento; a partir de 2010 era del 77,8% y a partir de 2013, del 98,3% (Fig. 3).
| Figura 3. Porcentaje de procedimientos de neumoenema realizados bajo sedación. Nótese un aumento del uso de la sedación a lo largo de los años, siendo prácticamente nulo hasta el año 2008 y aumentando paulatinamente hasta la actualidad, donde se emplea en todos los procedimientos de desinvaginación |
|---|
 |

En los casos de invaginación ileoileal, el tratamiento fue únicamente médico (sintomático), con mejoría clínica en todos ellos.
La cirugía se llevó a cabo tras no conseguir la reducción con neumoenema, por inestabilidad clínica o mal estado general del paciente. En nuestra serie requirieron intervención 49 casos (10,7%) tras el primer episodio de invaginación. Los hallazgos quirúrgicos se muestran en la Tabla 3. Los diagnósticos más frecuentes fueron: invaginación intestinal –de cualquier tipo–, realizándose desinvaginación manual mediante maniobras de taxis; adenitis mesentérica y divertículo de Meckel (Fig. 4). La resección intestinal fue necesaria en 11 pacientes (22,4% de las intervenciones), por isquemia o perforación intestinal.
| Tabla 3. Hallazgos quirúrgicos | ||
|---|---|---|
| Hallazgos quirúrgicos | Frecuencia | Porcentaje (%) |
| Invaginación intestinal sin otros hallazgos | 16 | 32,6 |
| Divertículo de Meckel | 9 | 18,4 |
| Adenitis mesentérica | 3 | 6,1 |
| Apendicitis aguda | 2 | 4,1 |
| Bridas | 2 | 4,1 |
| Quiste de duplicación intestinal | 2 | 4,1 |
| Linfoma intestinal | 1 | 2,0 |
| Isquemia o perforación intestinal | 11 | 22,5 |
| Normalidad | 3 | 6,1 |
| Total | 49 | 100 |

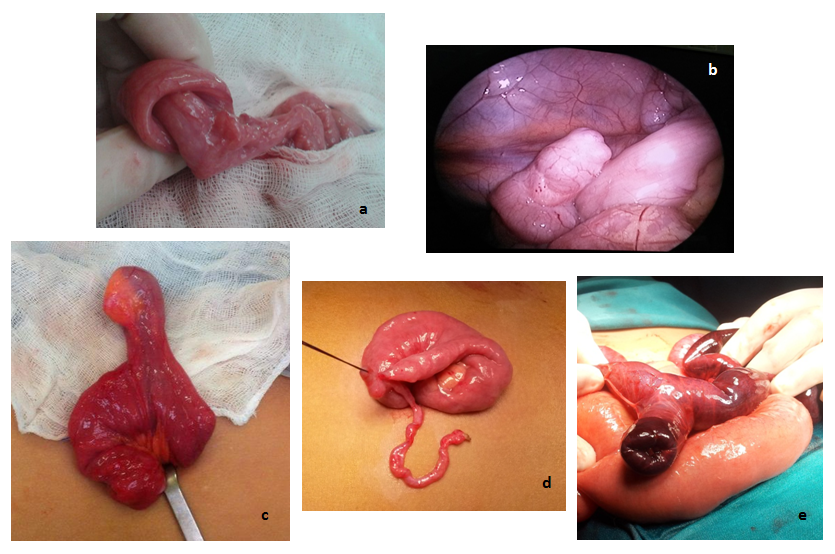
| Figura 4. Imágenes quirúrgicas: a) invaginación intestinal; b) divertículo de Meckel, hallazgo laparoscópico; c) divertículo de Meckel exteriorizado a través de incisión umbilical; d) continuación de divertículo de Meckel con conducto onfalomesentérico obliterado; e) divertículo de Meckel complicado, tras invaginación del mismo |
|---|
 |

Se registraron 78 recidivas en 56 pacientes (12,2% de los casos, rango 1-4), con un intervalo medio de tiempo desde el primer episodio de 173,4 días (DE 284,7, rango 0-1292). Se registraron 15 casos (19,2%) intrahospitalariamente, 11 pacientes con una única recidiva y dos pacientes con dos episodios (Fig. 5). Se empleó neumoenema como tratamiento inicial en el 90% de las primeras recidivas y el 81,8% de las segundas. No hubo complicaciones derivadas de este procedimiento ni se registró ningún exitus.
En cuanto al tiempo medio para la reintroducción de la alimentación tras la resolución del cuadro, este fue de 28,6 horas (DE 31,3, rango 4-144). En el grupo de pacientes que no recidivó, la reintroducción precoz o fast-track (en menos de seis horas) se hizo en el 30,2% de los casos, mientras que, en el grupo que recidivó en alguna ocasión, se pudo realizar en el 23,1% de los casos, sin incidencias en ninguno de ellos. En el análisis estadístico no hay diferencias significativas entre los grupos (p = 0,608).
La estancia media hospitalaria fue de 64,4 horas (DE 90,2, rango 2-1280, mediana 40 horas): 63,8 horas en el grupo de no recidivas (DE 93,26, mediana 40) y 69 horas en el de recidivas (DE 64,46, mediana 45), sin cumplirse criterios de significación estadística (t = -0,4; p = 0,689). Esta estancia tan dilatada en el caso de los pacientes no recidivados, y tan similar al mismo tiempo al grupo con recidiva, se debe fundamentalmente a un caso aislado de un paciente que no recidivó. Este paciente permaneció 1280 horas en nuestro centro por un shock séptico y, en el contexto de un íleo paralítico que requirió cirugía, se realizó reducción manual de una invaginación ileoileal. Excluyendo este caso, la estancia media hospitalaria total hubiera sido de 61,8 horas, siendo de 60,8 horas en el subgrupo de pacientes sin recidiva (t = -0,820; p = 0,454).
DISCUSIÓN
La muestra de pacientes obtenida en nuestro estudio tiene una edad media y distribución por sexos coincidente con lo descrito en la literatura médica (la mayoría varones, menores de tres años). Lo mismo ocurre en cuanto a la localización de la invaginación, de predominio en situación ileocólica, y el porcentaje de pacientes en los que se encuentra causa secundaria de invaginación (2,4%).
La ecografía es también en nuestro centro el estudio complementario más empleado para el diagnóstico de esta entidad, aunque suele acompañarse en múltiples ocasiones de una radiografía de abdomen previa para observar el patrón aéreo intestinal y descartar perforación. Sin embargo, la realización de esta última exploración complementaria es discutida en nuestro centro y en la bibliografía consultada, pues algunos expertos defienden que no aporta suficiente información que justifique la radiación que produce en el paciente, no suele cambiar la actitud (ecografía y neumoenema posterior) y tiene una baja sensibilidad17,20.
De acuerdo a lo publicado hasta la fecha, el tratamiento conservador de la invaginación intestinal con neumoenema es seguro y efectivo en la mayoría de los casos, con tasas de complicación bajas15-20. Esto coincide con lo observado en nuestro estudio (un 91,1% de los casos reducidos tras el primer intento, ninguna complicación y/o exitus).
Cabe señalar que en los últimos años, coincidiendo con un aumento en la utilización de la sedación durante el procedimiento, la tasa de éxito se ha visto aumentada. Esto se debe a una menor resistencia por parte del paciente al producirse una relajación de la musculatura, que se traduce en un menor tiempo necesario en el procedimiento, con la consiguiente reducción de la radiación recibida21-22. Además, en nuestro estudio, en el subgrupo de pacientes que no recibió sedación, la intervención quirúrgica fue necesaria en el 9%, mientras que en el subgrupo de pacientes sedados esto se redujo a la mitad (4,5%). Sin embargo, esta diferencia no fue estadísticamente significativa (p = 0,133). A pesar de ello, la tasa de cirugía registrada en nuestra serie (10,7%) se sitúa por debajo o en el límite inferior del intervalo descrito en las fuentes consultadas (10-30%)15,19.
El porcentaje de recidivas registrado en nuestra muestra (12,2%) se encuentra dentro del rango esperado (8-15%)1,5,7,10,15,16,18, con un intervalo medio de tiempo desde el primer episodio de 5-6 meses, como hemos descrito previamente. De los 78 casos de recidiva, se registraron 15 intrahospitalariamente (19,2%), uno en las primeras 24 horas y el resto durante el segundo día de ingreso. Sin embargo, no hubo diferencias en la evolución de los pacientes (en lo que a morbimortalidad se refiere), independientemente que el episodio de recidiva ocurriera en domicilio o durante el ingreso hospitalario. Por tanto, solo este 19,2% se podrían haber diagnosticado con un ingreso de 48 horas, sin aportar este hecho diferencias en la morbimortalidad.
Como ya hemos comentado, el tiempo medio para la reintroducción de la alimentación tras la reducción y/o desaparición de la clínica (en el caso de las no tratadas con neumoenema) fue de 28,6 horas. No hubo incidencias destacables ni diferencias significativas al comparar los grupos con recidiva y sin recidiva. Por tanto, en nuestra experiencia, la implementación de esta medida parece segura y contribuiría a poder dar el alta de forma más temprana a estos pacientes.
La estancia media en el hospital fue de 61,8 horas (60,8 horas en el grupo no recidivado y 69 horas en el recidivado). Tampoco es una diferencia estadísticamente significativa en este caso entre los grupos (t = -0,4; p = 0,689).
El análisis de los datos revela que un mayor tiempo de evolución no disminuye la tasa de éxito ni aumenta el número de intentos de neumoenema necesarios para la reducción de la invaginación (t = 0,478; p = 0,634), pero sí determina –de forma estadísticamente significativa– una mayor indicación de tratamiento quirúrgico (χ² = 5,604; p = 0,018). Esto podría explicarse por un peor estado general o inestabilidad clínica del paciente a su llegada a nuestro centro. Del mismo modo, hemos observado que la reintroducción precoz de la alimentación (fast-track) no se relaciona con un mayor número de episodios de recidiva en nuestra población (χ² = 0,031; p = 0,608), sin cumplir criterios de significación estadística.
En cuanto a las limitaciones del estudio, se trata de un modelo retrospectivo, susceptible a sesgos. Conocemos la limitación que supone la pérdida de episodios que ocurren en domicilio y se resuelven de forma espontánea o bien consultan en otro centro y no son remitidos al nuestro. Además, durante el periodo que abarca nuestro trabajo ha habido cambios en cuanto a la metodología empleada (neumoenema con o sin sedación) y los radiólogos y cirujanos de nuestro centro han ganado experiencia en el manejo de esta patología. El desarrollo de las técnicas laparoscópicas, que permiten realizar una exploración quirúrgica de la cavidad abdominal en caso de dudas diagnósticas, con menor morbilidad que la cirugía abierta, también ha facilitado el tratamiento de la invaginación. Por otro lado, la ausencia de complicaciones nos hace plantearnos la posibilidad de que nuestra muestra no haya sido lo suficientemente grande para poder detectarlo.
A pesar de que los datos obtenidos apoyan la actitud propuesta basada en la observación sin ingreso de estos pacientes (facilitado a su vez por una introducción temprana de la alimentación oral o fast track), conviene seleccionar bien los casos, pues debe tratarse de pacientes estables, no complicados y sin sospecha de causa secundaria que requiera tratamiento quirúrgico. Además, pacientes que viven lejos del centro médico o con dificultades socioeconómicas tampoco serían los candidatos ideales para esta medida. En caso de poder implementarla, es fundamental un seguimiento ambulatorio por parte de su médico de Atención Primaria, así como la educación de los familiares sobre la patología y la actitud a seguir en caso de recidiva.
CONCLUSIONES
La reducción de los costes sanitarios y la mejoría de la calidad de vida del paciente son objetivos cada vez más buscados por los diferentes centros médicos y sus facultativos. Una estancia menor en el hospital o, incluso, un periodo de observación en Urgencias durante un breve intervalo de tiempo, sin necesidad de ingreso, podrían contribuir a mejorar estos dos propósitos.
Tras la realización de este estudio, tal y como han propuesto algunos grupos de trabajo1, consideramos coste-efectiva y segura la actitud terapéutica propuesta al inicio del trabajo ante la invaginación intestinal. La observación en Urgencias durante un periodo de tiempo aproximado de 12 horas tras la reducción de la invaginación mediante neumoenema no ha demostrado una tasa de complicaciones mayor comparado con el ingreso del paciente. Esto se ha visto favorecido de forma importante por protocolos de actuación como son la implementación de la sedación del paciente durante la realización del neumoenema21-22 y la introducción precoz de la alimentación (fast-track)23-25. Sin embargo, es importante señalar la relevancia de la correcta selección de los pacientes, la adecuada información y educación de los familiares y la necesidad de un seguimiento estrecho posterior de forma ambulatoria por su médico de Atención Primaria.
No obstante, son necesarios estudios prospectivos aleatorizados para demostrar de forma más fiable esta actitud y recomendarla de forma generalizada.
CONFLICTO DE INTERESES
Los autores declaran no presentar conflictos de intereses en relación con la preparación y publicación de este artículo.
ABREVIATURAS
DE: desviación estándar.
BIBLIOGRAFÍA
- Beres AL, Baird R, Fung E, Hsieh H, Abou-Khalil M, Ted Gerstle J. Comparative outcome analysis of the management of pediatric intussusception with or without surgical admission. J Pediatr Surg. 2014;49:750-2.
- Bines J, Ivanoff B. Acute intussusception in infants and children: incidence, clinical presentation and management: a global perspective. Vaccines and biologicals. Document WHO/V&B/02.19. Ginebra: Organización Mundial de la Salud; 2002.
- Wong CW, Chan IH, Chung PH, Lan LC, Lam WW, Wong KK, et al. Childhood intussusception: 17-year experience at a tertiary referral centre in Hong Kong. Hong Kong Med J. 2015;21:518-23.
- Jiang J, Jiang B, Parashar U, Nguyen T, Bines J, Patel MM. Childhood intussusception: a literature review. PLoS One. 2013;8:e68482.
- Huppertz HI, Soriano-Gabarró M, Grimprel E, Franco E, Mezner Z, Desselberger U, et al. Intussusception among young children in Europe. Pediatr Infect Dis J. 2006;25:22-9.
- Mehendale S, Kumar CP, Venkatasubramanian S, Prasanna T. Intussusception in children aged less than five years. Indian J Pediatr. 2016;83:1087-92.
- Esmaeili-Dooki MR, Moslemi L, Hadipoor A, Osia S, Fatemi SA. Pediatric intussusception in Northern Iran: comparison of recurrent with non-recurrent cases. Iran J Pediatr. 2016;26:e3898.
- Trotta F, Da Cas R, Bella A, Santuccio C, Salmaso S. Intussusception hospitalizations incidence in the pediatric population in Italy: a nationwide cross-sectional study. Ital J Pediatr. 2016;42:89.
- Abbas T, AlShahwani N, Jabbour G, Ali M. Retrospective surveillance over 11 years for intussusception in children younger than 14 years in the state of Qatar. Open J Pediatr. 2014;4:1-11.
- Blanch AJ, Perel SB, Acworth JP. Paediatric intussusception: epidemiology and outcome. Emerg Med Australas. 2007;19:45-50.
- Navarro O, Dugougeat F, Kornecki A, Shuckett B, Alton DJ, Daneman A. The impact of imaging in the management of intussusception owing to pathologic lead points in children. A review of 43 cases. Pediatr Radiol. 2000;30:594-603.
- Ludvigsson JF, Nordenskjöld A, Murray JA, Olén O. A large nationwide population-based case-control study of the association between intussusception and later celiac disease. BMC Gastroenterol. 2013;13:89.
- Fallon SC, Lopez ME, Zhang W, Brandt ML, Wesson DE, Lee TC, et al. Risk factors for surgery in pediatric intussusception in the era of pneumatic reduction. J Pediatr Surg. 2013;48:1032-6.
- Singhal BM, Kaval S, Sagar S, Kumar V. Ileoileal intussusception due to Meckel’s diverticulum: An uncommon aetiology. OA Surgery. 2013;1:2.
- Applegate KE. Intussusception in children: diagnostic imaging and treatment. En: Medina LS, Blacmore CC, Applegate KE (eds.). Evidenced-based imaging: improving the quality of imaging in patient care. Atlanta: Springer; 2011. p. 501-14.
- Williams H. Imaging and intussusception. Arch Dis Child Educ Pract Ed. 2008;93:30-6.
- Daneman A, Navarro O. Intussusception Part 1: a review of diagnostic approaches. Pediatr Radiol. 2003;33:79-85.
- Daneman A, Navarro O. Intussusception Part 2: an update on the evolution of management. Pediatr Radiol. 2004;34:97-108.
- Khorana J, Singhavejsakul J, Ukarapol N, Laohapensang M, Wakhanrittee J, Patumanond J. Enema reduction of intussusception: the success rate of hydrostatic and pneumatic reduction. Ther Clin Risk Manag. 2015;11:1837-42.
- Hernandez JA, Swischuk LE, Angel CA. Validity of plain films in intussusceptions. Emerg Radiol. 2004;10:323-6.
- Díaz-Aldagalán González R, Pérez-Martínez A, Pisón-Chacón J, Ayuso-González L, Salcedo-Muñoz B, Goñi-Orayen C. Rescue by pneumoenema under general anaesthesia of apparently non-reducible intestinal intussusceptions. Eur J Pediatr. 2012;171:189-91.
- Ilivitzki A, Shtark LG, Arish K, Engel A. Deep sedation during pneumatic reduction of intussusception. Pediatr Radiol. 2012;42:562-5.
- Adekunle-Ojo AO, Craig AM, Ma L, Caviness AC. Intussusception: postreduction fasting is not necessary to prevent complications and recurrences in the Emergency Department Observation Unit. Pediatr Emerg Care. 2011;27:897-9.
- Sholadoye TT, Suleiman AF, Mshelbwala PM, Ameh EA. Early oral feeding following intestinal anastomoses in children is safe. Afr J Paediatr Surg. 2012;9:113-6.
- Zhuang CL, Ye XZ, Zhang CJ, Dong QT, Chen BC, Yu Z. Early versus traditional postoperative oral feeding in patients undergoing elective colorectal surgery: a meta-analysis of randomized clinical trials. Dig Surg. 2013;30:225-32.
Comentarios
Este artículo aún no tiene comentarios.