Vol. 12 - Num. 19
Presentación del estudio de consenso de bronquiolitis
Recomendaciones de la Conferencia de Consenso de Bronquiolitis Aguda en España: de la evidencia a la práctica
Javier González de Diosa, Carlos Ochoa Sangradorb, en representación del Grupo de Trabajo (Grupo Investigador, Grupo de Revisión y Panel de Expertos) del Proyecto aBREVIADo (BRonquiolitis-Estudio de Variabilidad, Idoneidad y ADecuación)
aServicio de Pediatría. Hospital General Universitario de Alicante. Departamento de Pediatría. Universidad Miguel Hernández. ISABIAL-Instituto de Investigación Sanitaria y Biomédica de Alicante. Alicante. España.
bServicio de Pediatría. Hospital Virgen de la Concha. Zamora. España.
Cómo citar este artículo: González de Dios J, Ochoa Sangrador C, en representación del Grupo de Trabajo (Grupo Investigador, Grupo de Revisión y Panel de Expertos) del Proyecto aBREVIADo (BRonquiolitis-Estudio de Variabilidad, Idoneidad y ADecuación). Recomendaciones de la Conferencia de Consenso de Bronquiolitis Aguda en España: de la evidencia a la práctica. Rev Pediatr Aten Primaria. 2010;12(Supl 19):s107-s128.
Publicado en Internet: 20-11-2010 - Número de visitas: 20328
Resumen
Se describe la metodología de trabajo de la Conferencia de Consenso (revisión bibliográfica, síntesis de la evidencia, método de consenso y fuerza de las recomendaciones por propuesta GRADE) y se resumen la evidencia sobre la frecuencia de bronquiolitis en la población general y en grupos de riesgo, los factores y marcadores de riesgo de formas graves, las escalas de gravedad y el perfil clínico-etiológico. Las pruebas diagnósticas habitualmente empleadas apenas resultan útiles en el manejo de la enfermedad; solo se considera necesaria la medición de la saturación de oxígeno en la valoración inicial o en el control de cambios de pacientes con compromiso respiratorio. Otras pruebas (radiografía torácica, pruebas de diagnóstico rápido de infección por virus respiratorios y pruebas de cribado de infección bacteriana) solo deben emplearse de forma muy selectiva. Existe evidencia suficiente sobre la falta de eficacia de la mayoría de las intervenciones en bronquiolitis. Al margen de la oxigenoterapia, la fluidoterapia, la aspiración de secreciones y la asistencia respiratoria, pocas opciones terapéuticas resultarán beneficiosas. Solo en los casos moderado-graves estaría justificado el ensayo con broncodilatadores inhalados (salbutamol o adrenalina) con suero salino hipertónico o sin él. En casos con fracaso respiratorio podrían emplearse heliox y técnicas de ventilación no invasiva; en pacientes con apneas valorar metilxantinas, y en pacientes graves intubados el uso de surfactante. Ningún tratamiento se ha mostrado eficaz para evitar la persistencia-recurrencia de síntomas postbronquiolitis. En cuanto a la prevención de la bronquiolitis, solo palivizumab reduce el riesgo de ingreso por virus respiratorio sincitial, aunque por su elevado coste su uso solo se justifica en pacientes de alto riesgo.
Palabras clave
● Bronquiolitis viral ● Conferencia de consenso ● Medicina basada en la evidencia ● Pediatría ● Revisión sistemáticaNota:
Financiado con una beca de la Fundación-Hospital Torrevieja (código de protocolo: BECA0001).
Estudio avalado por la Asociación Española de Pediatría (AEP), Asociación Española de Pediatría de Atención Primaria (AEPap), Sociedad Española de Pediatría Extrahospitalaria y Atención Primaria (SEPEAP), Sociedad Española de Urgencias Pediátricas (SEUP), Sociedad Española de Infectología Pediátrica (SEIP), Sociedad Española de Neumología Pediátrica (SENP), Sociedad Española de Inmunología Clínica y Alergia Pediátrica (SEICAP), Sociedad Española de Cuidados Intensivos Pediátricos (SECIP), Sociedad Española de Neonatología (SEN) y Sociedad Española de Cardiología Pediátrica (SECPCC).
Los datos principales del estudio han sido publicados como Conferencia de Consenso en seis artículos en Anales de Pediatría y la publicación en toda su extensión se ha publicado también como Guía de Práctica Clínica en GuiaSalud.
Introducción
La bronquiolitis aguda (BA) es una enfermedad que origina una gran demanda asistencial en Atención Primaria y en los Servicios de Urgencias, pues constituye la principal causa de ingreso por infección respiratoria aguda de vías bajas en el niño menor de dos años. El virus respiratorio sincitial es el agente causal dominante, aunque también están implicados otros virus.
La definición más aceptada de BA es la de McConnochie, que considera bronquiolitis el primer episodio agudo de dificultad respiratoria con sibilancias, precedido por un cuadro catarral de vías altas (rinitis, tos, con/sin fiebre), que afecta a niños menores de dos años, aunque preferentemente se da en el primer año de vida. Sin embargo, no todos los autores están de acuerdo con esta definición y aún no se ha llegado a un consenso acerca de los criterios necesarios para emitir el diagnóstico, especialmente los de edad o número de episodios.
Desde el punto de vista práctico, el principal problema que plantea la BA es la falta de consenso y homogeneidad en su manejo terapéutico y preventivo. Aunque existen algunos protocolos o guías de práctica clínica, estos presentan diferencias en la evaluación de la evidencia disponible y en sus recomendaciones. La literatura publicada en relación con el tratamiento de la BA es muy abundante, con múltiples ensayos clínicos aleatorizados (ECA) en las distintas intervenciones analizadas. La síntesis de la información de estos ECA es también sólida, fundamentada en guías de práctica clínica (GPC) y revisiones sistemáticas.
Destacamos tres GPC sobre BA, actuales y con rigurosa metodología: la de la American Academy of Pediatrics1, la de la Scottish Intercollegiate Guideline Network2 y la del Cincinnati Children´s Hospital Medical Center3. El repertorio de GPC National Guideline Clearinghouse acaba de publicar la síntesis comparativa de estas tres GPC que abordan un mismo problema de salud4. Se reconocen al menos las siguientes revisiones de la Cochrane sobre intervenciones en BA: adrenalina5, antibióticos6, beta-2-adrenérgicos7,8, bromuro de ipratropio9,10, corticoides11-14, fisioterapia15,16, inmunoglobulinas17-19, ribavirina20,21, suero salino hipertónico22 y surfactante23.
Considerando lo anteriormente expuesto, parece importante estudiar cómo se tratan las BA en nuestro medio, evaluando su variabilidad e idoneidad. Para ello llevamos a cabo el proyecto titulado “Variabilidad e idoneidad del manejo diagnóstico y terapéutico de la bronquiolitis aguda”, tras elaborar específicamente unos patrones de referencia de uso apropiado de los mismos sobre la base de la revisión sistemática de la literatura y una posterior Conferencia de Consenso multidisciplinaria. En este artículo se presenta el resumen de las respuestas planteadas en la Conferencia de Consenso (con su nivel de evidencia y grado de recomendación), con especial énfasis en la clasificación de idoneidad de los procedimientos terapéuticos y preventivos en la BA. Los datos principales del estudio han sido publicados como Conferencia de Consenso en seis artículos en Anales de Pediatría24-29 y la publicación en toda su extensión se ha publicado también como Guía de Práctica Clínica en GuiaSalud30.
Material y métodos
Para describir la variabilidad en el manejo de la BA se han recogido una muestra de casos pediátricos menores de dos años diagnosticados de bronquiolitis, atendidos en las consultas, Servicios de Urgencias y hospitalización de una muestra de centros de salud y hospitales españoles durante el periodo epidémico de octubre de 2007 a marzo de 2008, y con representatividad de 90 centros sanitarios de 25 provincias de España, distribuidas en 12 comunidades autónomas. Las principales características de esta muestra se han publicado recientemente31.
Para evaluar la idoneidad debíamos definir el “patrón oro” de manejo terapéutico y preventivo de la BA. Para establecer este patrón oro se han llevado a cabo los siguientes pasos:
1. Creación de un grupo de trabajo para la realización de una revisión bibliográfica sistemática y crítica sobre BA procedente de fuentes bibliográficas primarias, secundarias y terciarias, de carácter internacional (MEDLINE, EMBASE, Cochrane Library) y nacional (Índice Médico Español). No se emplearon restricciones de idioma. No se realizaron restricciones de tiempo para los ensayos clínicos, revisiones sistemáticas y guías de práctica clínica. La búsqueda primaria de estudios observacionales se limitó a la última década en las bases de datos de MEDLINE y EMBASE, pero no en la Cochrane Library ni en el Índice Médico Español. El total de citas bibliográficas identificadas fue de 2794, de las que 953 se recuperaron y revisaron para el análisis de la evidencia.
2. Síntesis de la evidencia: todos los trabajos revisados se valoraron críticamente y se resumieron en tablas de evidencia, siguiendo una metodología explícita. En cada tabla de evidencia se detallaron los siguientes apartados: objetivo del estudio, autor y año de publicación, país de estudio, diseño y calidad del estudio, muestra de estudio e intervención, medidas de efecto y variables evaluadas, resultados (medidas de frecuencia, de efecto, de validez y de impacto), limitaciones, importancia clínica y conflictos de interés. Las tablas de evidencia se agruparon por áreas de interés (epidemiología, diagnóstico, tratamiento, prevención, pronóstico, etc.). Para cada área se elaboró un documento de revisión, con una breve introducción y justificación, un apartado con las Bases para la toma de decisiones y un conjunto de preguntas clínicas relacionadas que debían contestarse en la Conferencia de Consenso.
3. Realización de una Conferencia de Consenso, siguiendo las directrices de los National Institutes of Health americanos32: revisión en profundidad de la literatura con metodología explícita por un grupo de trabajo, formación de un panel de expertos no gubernamental, planteamiento al panel de una serie de preguntas clínicas y elaboración de un documento de consenso con recomendaciones para la buena práctica clínica, y jerarquización del grado de evidencia que sustenta cada recomendación.
La constitución del panel de expertos ha seguido los siguientes criterios: 1) ser profesionales con amplia experiencia en clínica e investigación sobre bronquiolitis y prestigio en el ámbito de su especialidad; 2) proporcionar un carácter multidisciplinario al panel, y 3) procurar una representación regional equilibrada. Se ha incorporado al panel los siguientes expertos de cada una de las siguientes áreas: Atención Primaria (tres), Cardiología Pediátrica (uno), Cuidados Intensivos Pediátricos (uno), Infectología Pediátrica (uno), Inmunología Clínica y Alergia Pediátrica (uno), Neonatología (uno), Neumología Pediátrica (uno) y Urgencias Pediátricas (dos).
Para ponderar la relevancia y aplicabilidad se considerarán medidas de efecto, impacto y validez con traducción clínica. Se propone un sistema de jerarquización de los niveles de evidencia basado en cuatro niveles con criterios relacionados con el volumen, el tipo de diseño y la calidad de los estudios disponibles. Estos criterios se han adaptado de otros sistemas de jerarquización propuestos33-37. Partiendo del nivel asignado en el sistema de clasificación previo, se propone un ajuste del nivel inicial siguiendo las recomendaciones de la propuesta GRADE38-41:
- Disminuir el nivel de evidencia (principalmente en ensayos clínicos) si: 1) existen limitaciones importantes en la calidad de los estudios; 2) existen inconsistencias importantes entre estudios; 3) existen dudas sobre si la evidencia es directa o indirecta; 4) la información disponible es imprecisa o escasa; 5) es muy probable que los resultados tengan sesgos importantes.
- Aumentar el nivel de evidencia (principalmente en estudios observacionales) si: 1) existen pruebas de una asociación muy fuerte (riesgo relativo > 5 o < 0,2) basadas en evidencia directa, sin amenazas importantes para la validez; 2) existen pruebas válidas de un gradiente dosis-respuesta; 3) se ha realizado un ajuste correcto de todos los factores de confusión posibles.
Se propone un sistema simplificado de graduación de las recomendaciones, adaptado de propuestas previas2-6. Además del volumen y la calidad de la evidencia, a la hora de asignar el grado de recomendación se deben tener en cuenta otros criterios38-41: la coherencia entre estudios, la posible influencia de factores de confusión o modificadores de efecto, la precisión de las estimaciones, la intensidad del efecto o la fuerza de la asociación, el grado de relación con la pregunta clínica (relación directa o indirecta), la aplicabilidad de la evidencia (efectividad y riesgo basal en la práctica clínica), el balance entre beneficios y riesgos o costes, la utilidad sobre los pacientes y sus preferencias y el potencial impacto de futuros estudios sobre la evidencia actual.
4. Finalmente, para los procedimientos diagnósticos y terapéuticos en los que se consideró necesario se establecieron las siguientes categorías de clasificación de la idoneidad:
- Opciones de primera elección (indicación rutinaria).
- Opciones de uso alternativo (indicación selectiva u opcional).
- Opciones inapropiadas o no recomendadas (innecesarias).
Resultados
Se realizaron un total de 61 preguntas en la Conferencia de Consenso, que se distribuyeron en: epidemiología y factores de riesgo (dos); perfil etiológico y patrones clínicos asociados (tres); pruebas diagnósticas (diez); factores pronósticos de gravedad (cuatro) y escalas de valoración de síntomas o gravedad (dos); riesgo de asma postbronquiolitis (una); tratamiento (28); prevención (ocho); y evaluación económica (tres).
En la tabla 1 se expone el resumen de las respuestas con las 61 preguntas planteadas en la Conferencia de Consenso, con su nivel de evidencia y grado de recomendación, según acuerdo llevado a cabo tras una reunión presencial de un día de trabajo de todo el Panel de Expertos y dos rondas de discusión por correo electrónico. Se llegó a consenso en 58 preguntas, y no fue posible en tres (las que corresponden a evaluación económica, centradas en el estudio coste-efectividad del palivizumab).


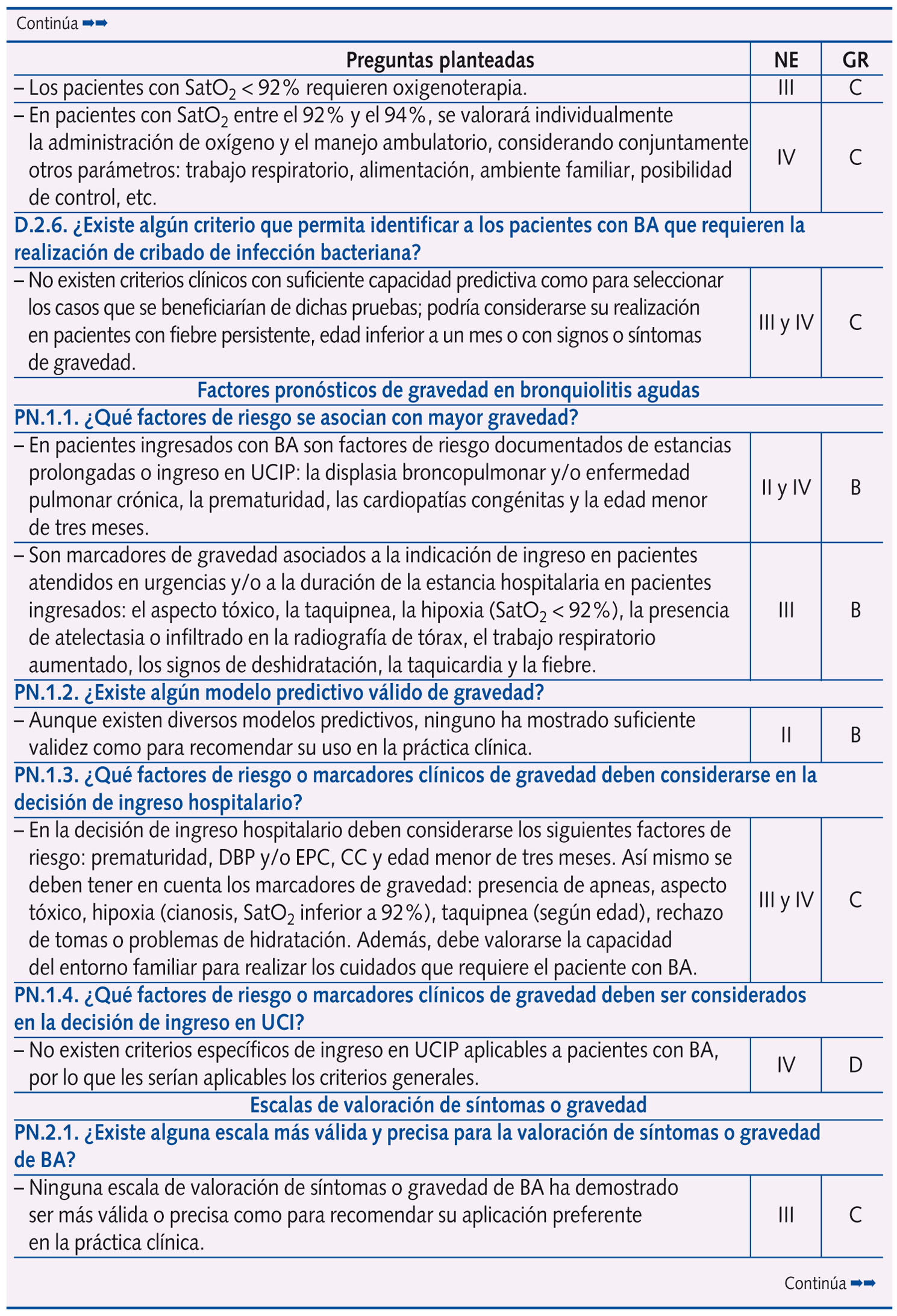
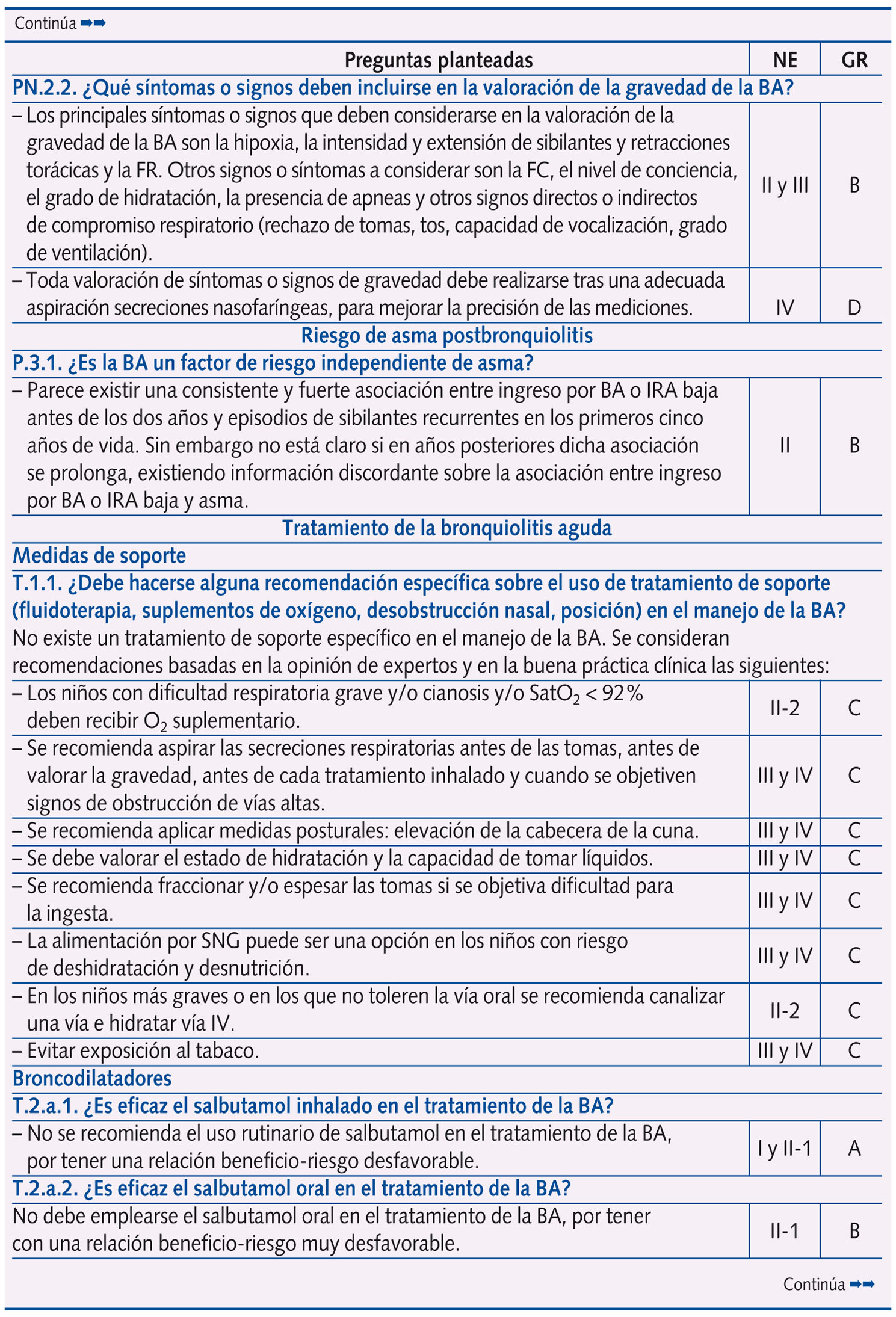

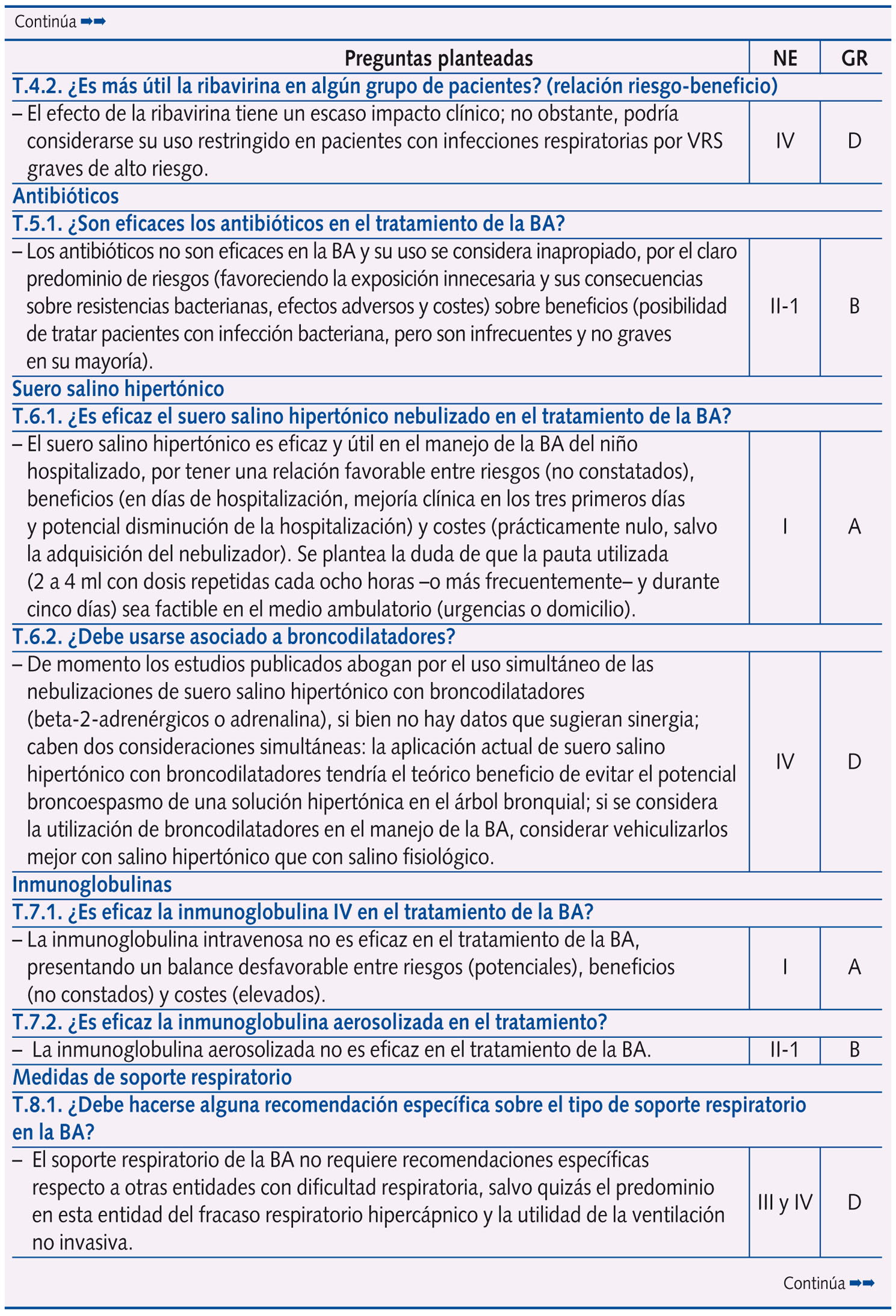

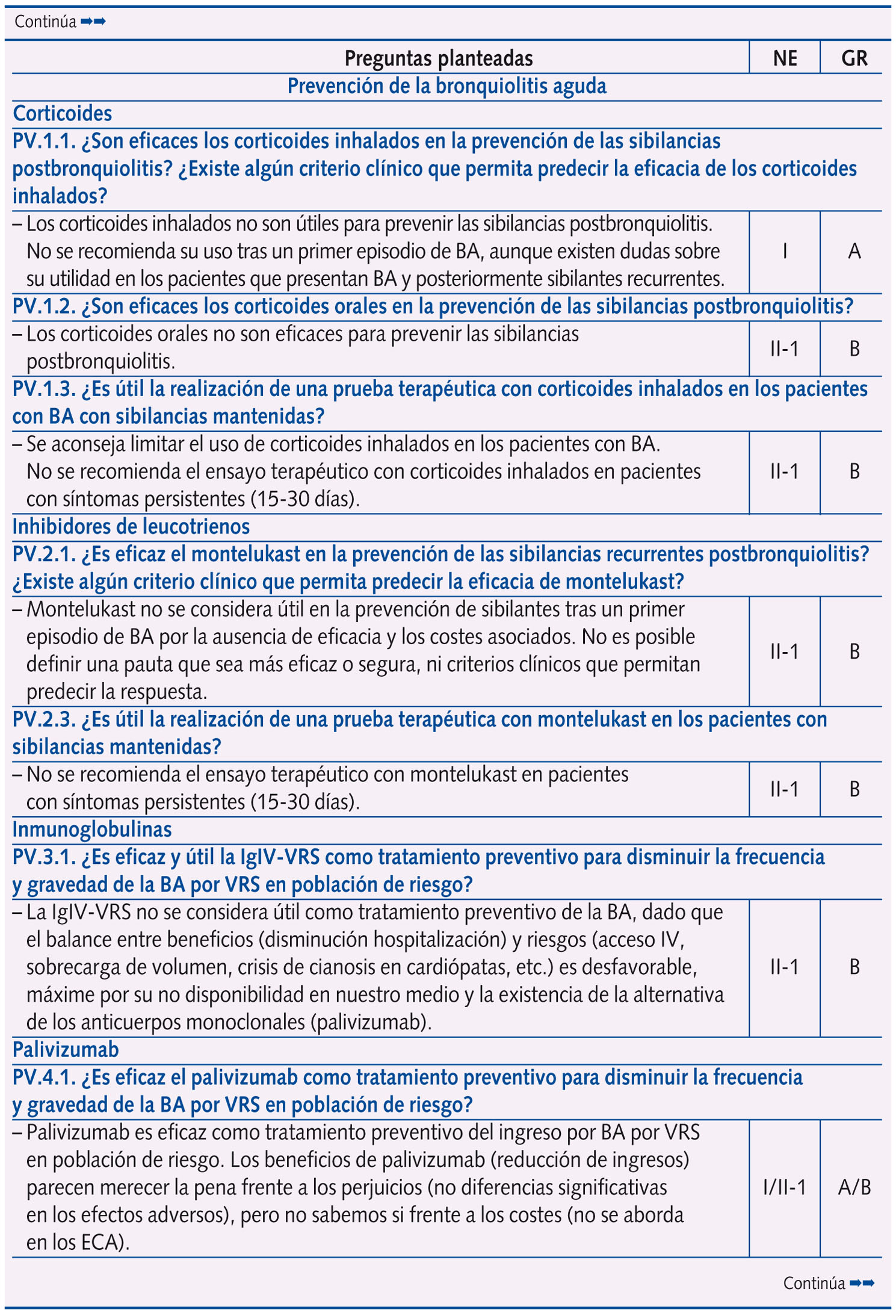
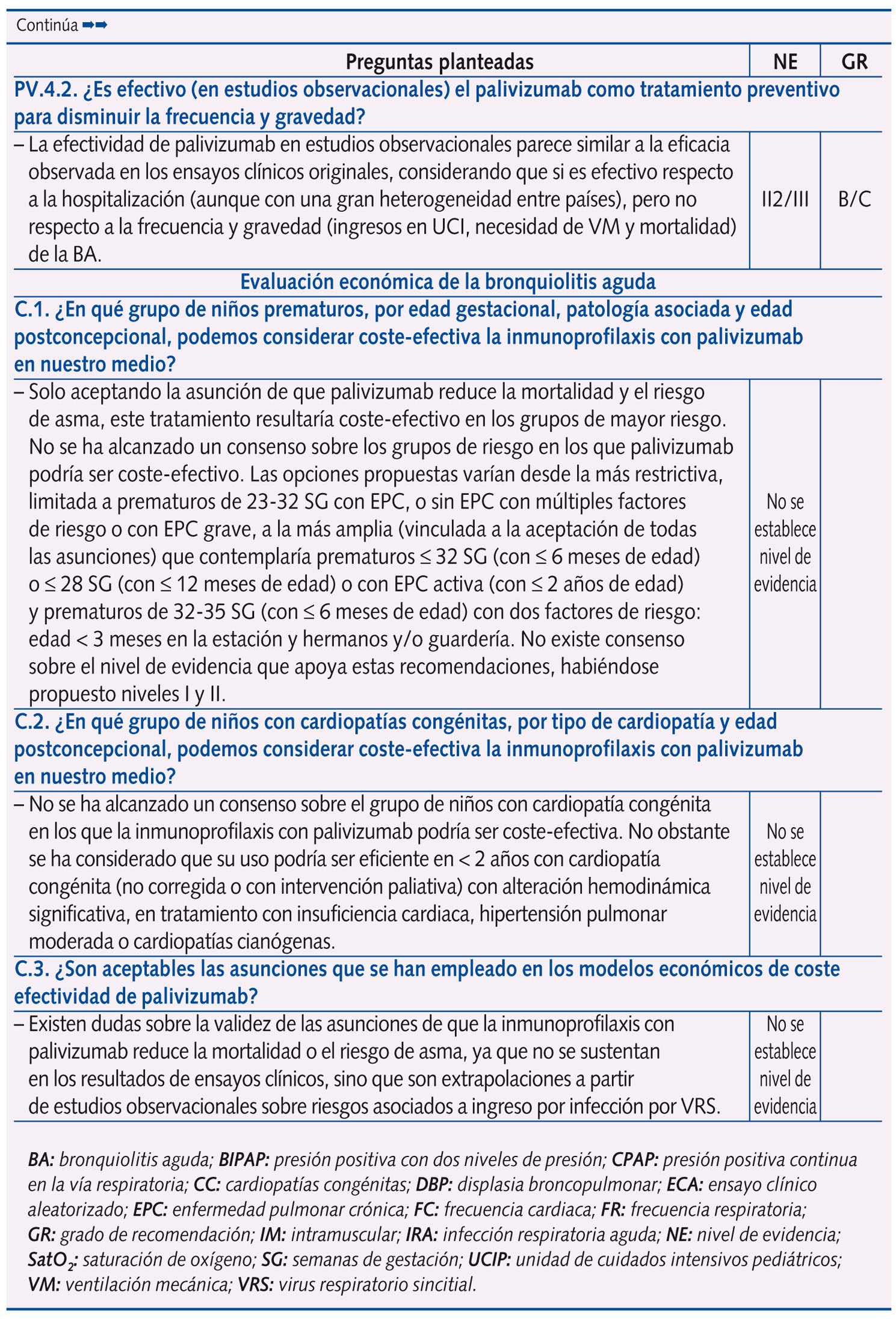
Más de la mitad de las preguntas al Panel de Expertos versan sobre tratamiento y prevención, subdivididas en los siguientes temas:
A. Tratamiento: medidas de soporte (una), broncodilatadores (ocho), corticoides (dos), ribavirina (dos), antibióticos (una), suero salino hipertónico (dos), inmunoglobulinas (dos), medidas de soporte respiratorio (seis), fisioterapia (una) y otras intervenciones (tres).
B. Prevención: corticoides (tres), inhibidores de leucotrienos (dos), inmunoglobulinas (una) y palivizumab (dos).
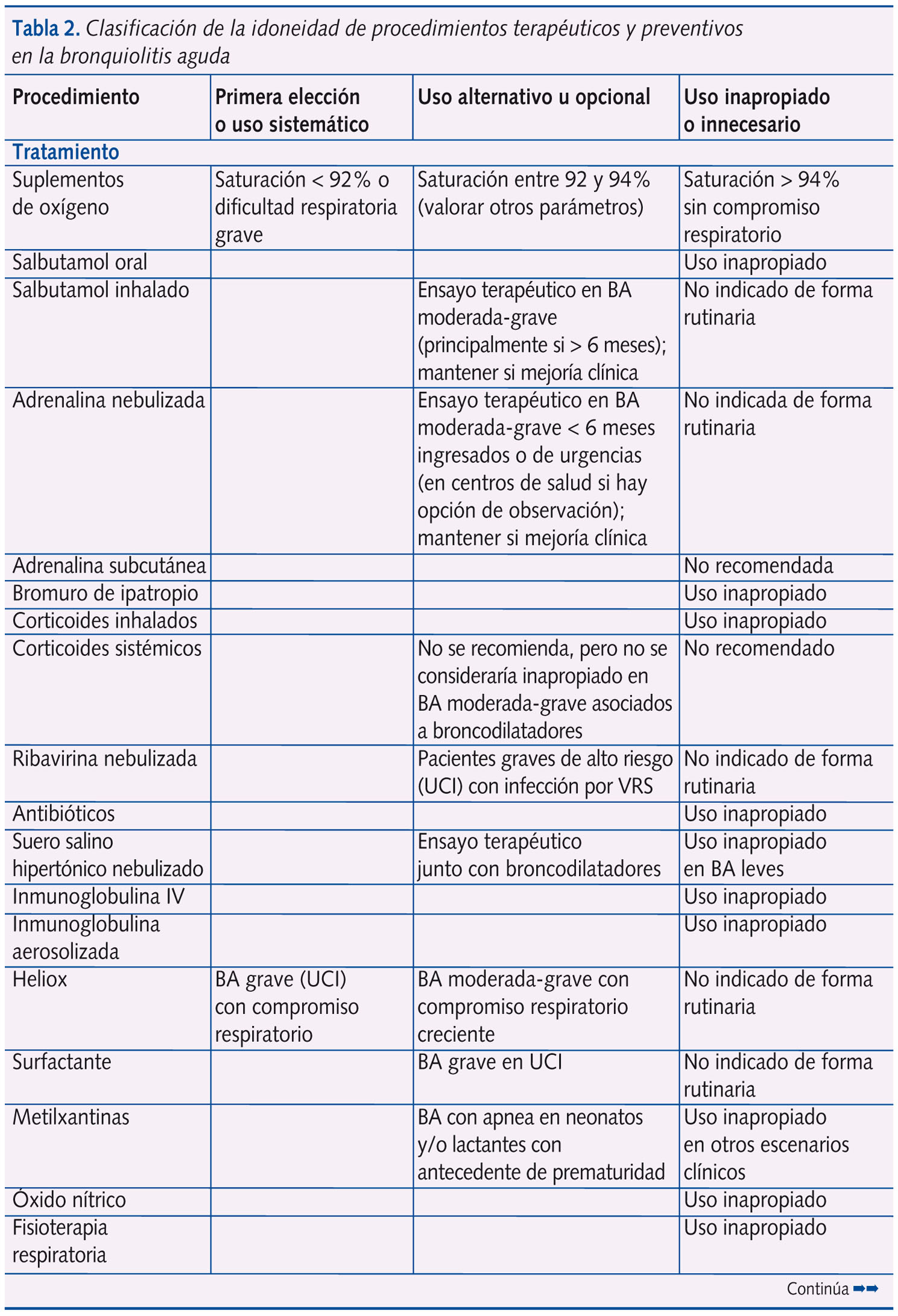
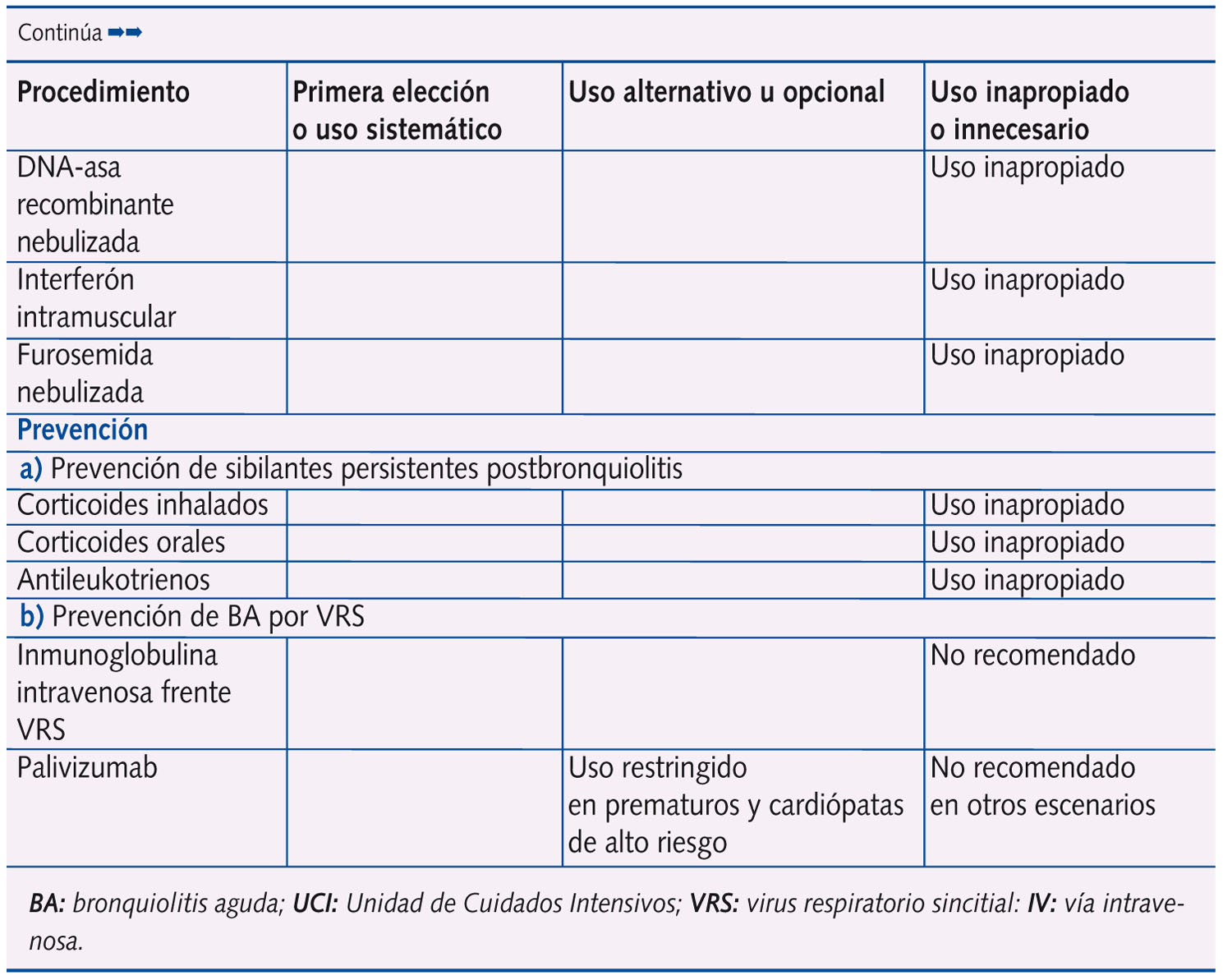
En la tabla 2 se expone la clasificación de la idoneidad (primera elección o uso sistemático; uso alternativo u opcional; uso inapropiado o innecesario) de las distintas intervenciones terapéuticas y preventivas en la BA, sobre la base del análisis de la revisión sistemática, nivel de evidencia y grado de recomendación que se exponen en la tabla 11.
Discusión
La BA es un ejemplo paradigmático de inadecuación de la práctica clínica a la evidencia científica en el campo del tratamiento. El tratamiento de la BA varía en cada brote epidémico anual dependiendo, en muchos casos, del artículo de “moda”. Según esto, no es infrecuente que un Residente de Pediatría en formación pueda haber tratado a estos pacientes un año preferentemente con adrenalina, otro con salbutamol y un tercero con suero salino hipertónico.
Variabilidad injustificada, sin duda. La cuestión está en definir el medicamento correcto para el paciente adecuado en la dosis apropiada y durante el tiempo oportuno42. La existencia de múltiples ECA en los últimos 25 años sobre las potenciales intervenciones farmacológicas en la BA (principalmente broncodilatadores, antiinflamatorios y antivíricos) y el escaso avance en el manejo de los infrecuentes casos de BA moderada-grave llegan a plantear incluso la duda de si es necesario continuar algunas líneas de investigación. El mayor avance en el desarrollo farmacológico de la BA en los últimos años se debe al campo de la prevención (desarrollo de anticuerpos monoclonales como inmunoprofilaxis), mientras que en el tratamiento son menos las novedades (heliox, suero salino hipertónico, etc.). Los objetivos del tratamiento de la BA son: disminuir la morbimortalidad, disminuir los costes sociales y económicos (reducir los ingresos hospitalarios y días de hospitalización) y disminuir las secuelas a largo plazo (patología respiratoria recurrente y, quizás, asma).
Según los resultados de la tabla 2, conviene plantear algunos comentarios:
- Desde el punto de vista terapéutico únicamente se consideran dos intervenciones como de primera elección: el suplemento de oxígeno en los lactantes con BA con una SatO2 < 92% y/o dificultad respiratoria grave, así como la aplicación de heliox en la Unidad de Cuidados Intensivos (UCI) en pacientes con compromiso respiratorio por BA grave.
Existe evidencia suficiente sobre la falta de eficacia de la mayoría de las intervenciones ensayadas en la BA. Al margen de la oxigenoterapia, la fluidoterapia, la aspiración de secreciones y la asistencia respiratoria, pocas opciones terapéuticas resultarán beneficiosas. Solo en los casos moderado-graves estaría justificado el ensayo con broncodilatadores inhalados (salbutamol o adrenalina) con suero salino hipertónico o sin él. En casos con fracaso respiratorio podrían emplearse heliox y técnicas de ventilación no invasiva, en pacientes con apneas se debe valorar el uso de metilxantinas, y en pacientes graves intubados el uso de surfactante.
El resto de intervenciones terapéuticas (salbutamol oral, adrenalina subcutánea, bromuro de ipatropio, corticoides inhalados, orales o sistémicos, antibióticos, inmunoglobulina intravenosa (IV) o aerosolizada, óxido nítrico, fisioterapia respiratoria, etc.) se consideran como uso inapropiado o innecesario. Sin embargo, los datos de campo de nuestro estudio indican que el tratamiento es inadecuado en el 43% de los pacientes con BA en fase aguda y en el 57% en fase de mantenimiento31. - Desde el punto de vista preventivo, ningún tratamiento se ha mostrado eficaz para evitar la persistencia o recurrencia de síntomas postbronquiolitis. En cuanto a la prevención de bronquiolitis, solo palivizumab reduce discretamente el riesgo de ingreso por infecciones respiratorias bajas por virus respiratorio sincitial, aunque por su elevado coste solo se justifica su uso en un reducido grupo de pacientes de alto riesgo (grandes prematuros y cardiopatías hemodinámicamente significativas). Resulta significativo que, de las 61 preguntas al Panel de Expertos en la Conferencia de Consenso1, fue posible el consenso sobre el nivel de evidencia y grado de recomendación en todas salvo en las tres preguntas relacionadas con la eficiencia del palivizumab en la prevención de BA.
Consideramos importante la difusión de esta tabla sobre la clasificación de la idoneidad de procedimientos terapéuticos y preventivos en la BA, máxime en una enfermedad muy prevalente, con alto consumo de recursos y una variabilidad en la práctica clínica no justificada. El desarrollo de la misma se ha elaborado siguiendo las premisas de la medicina basada en la evidencia, cuyo objetivo es conseguir una práctica clínica más eficaz, efectiva, eficiente y segura.
Disponemos de las pruebas científicas (la “evidencia”), pero ahora conviene difundirlas y, sobre todo, implementarlas en la práctica clínica. La pregunta que sobrevuela es: ¿Será posible modificar la variabilidad injustificada en el manejo de la BA?
Bibliografía
- American Academy of Pediatrics (AAP). Subcommittee on Diagnosis and Management of Bronchiolitis. Diagnosis and management of bronchiolitis. Pediatrics. 2006;118:1774-93.
- SIGN. Bronchiolitis in children. A national clinical guideline. Available at: htpp://www.signacuk.2006.
- Bronchiolitis Guideline Team, Cincinnati Children’s Hospital Medical Center. Evidence based clinical practice guideline for medical management of bronchiolitis in infants year of age or less presenting with a first time episode. Cincinnati: Cincinnati Children’s Hospital Medical Center; 2005. [En línea.] [Consultado el 09/05/2009.] Disponible en www.cincinnatichildrens.org/NR/rdonlyres/0B7B99D7-DB3E-4186-B2FC-71539E23421E/0/bronchiolitisguideline.pdf.
- National Guideline Clearinghouse (NGC). Guideline Synthesis. Prevention, diagnosis and treatment of pediatric bronchiolitis. [En línea] [Consultado el 09/05/2009] Disponible en: www.guidelinegov/Compare/comparisonaspx?file=BRONCHIOLITIS1inc.
- Hartling L, Wiebe N, Russell K, Patel H, Klassen TP. Epinephrine for bronchiolitis. Cochrane Database Syst Rev. 2004(1):CD003123.
- Spurling GK, Fonseka K, Doust J, Del Mar C. Antibiotics for bronchiolitis in children. Cochrane Database Syst Rev. 2007(1):CD005189.
- Gadomski AM, Bhasale AL. Broncodilatadores para la bronquiolitis (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, 2007 Número 4 Oxford: Update Software Ltd. Disponible en: http://www.update-software.com (Traducida de The Cochrane Library, 2007 Issue 4 Chichester, UK: John Wiley & Sons, Ltd.).
- Kellner JD, Ohlsson A, Gadomski AM, Wang EE. Bronchodilators for bronchiolitis. Cochrane Database Syst Rev. 2000(2):CD00 1266.
- Everard ML, Bara A, Kurian M, Elliott TM, Ducharme F, Mayowe V. Anticholinergic drugs for wheeze in children under the age of two years. Cochrane Database Syst Rev. 2005(3):CD 001279.
- Everard ML, Bara A, Kurian M, Elliott TM, Ducharme F. Anticholinergic drugs for wheeze in children under the age of two years. Cochrane Database Syst Rev. 2002(1):CD001279.
- Patel H, Platt R, Lozano J. WITHDRAWN: Glucocorticoids for acute viral bronchiolitis in infants and young children. Cochrane Database Syst Rev. 2008(1):CD004878.
- Patel H, Platt R, Lozano JM, Wang EE. Glucocorticoids for acute viral bronchiolitis in infants and young children. Cochrane Database Syst Rev. 2004(3):CD004878.
- McKean M, Ducharme F. Inhaled steroids for episodic viral wheeze of childhood. Cochrane Database Syst Rev. 2000(2):CD001107.
- Blom D, Ermers M, Bont L, Van Aalderen WM, Van Woensel JB. Inhaled corticosteroids during acute bronchiolitis in the prevention of post-bronchiolitic wheezing. Cochrane Database Syst Rev. 2007(1):CD004881.
- Perrotta C, Ortiz Z, Roque M. Chest physiotherapy for acute bronchiolitis in paediatric patients between 0 and 24 months old. Cochrane Database Syst Rev. 2007(1):CD004873.
- Perrotta C, Ortiz Z, Roque M. Chest physiotherapy for acute bronchiolitis in paediatric patients between 0 and 24 months old. Cochrane Database Syst Rev. 2005(2):CD004 873.
- Wang EE, Tang NK. WITHDRAWN: Immunoglobulin for preventing respiratory syncytial virus infection. Cochrane Database Syst Rev. 2006(3):CD001725.
- Wang EE, Tang NK. Immunoglobulin for preventing respiratory syncytial virus infection. Cochrane Database Syst Rev. 2000(2):CD00 1725.
- Fuller H, Del Mar C. Immunoglobulin treatment for respiratory syncytial virus infection. Cochrane Database Syst Rev. 2006(4):CD0048 83.
- Ventre K, Randolph AG. Ribavirin for respiratory syncytial virus infection of the lower respiratory tract in infants and young children. Cochrane Database Syst Rev. 2007(1):CD000 181.
- Ventre K, Randolph A. Ribavirin for respiratory syncytial virus infection of the lower respiratory tract in infants and young children. Cochrane Database Syst Rev. 2004(4):CD000181.
- Zhang L, Mendoza-Sasi RA, Wainwright C, Klassen TP. Nebulized hypertonic saline solution for acute bronchiolitis in infants. Cochrane Database of Systematic Reviews Isue 4 Art No: CD006458 DOI: 101002/14651858CD0064 58pub2. 2008.
- Ventre K, Haroon M, Davison C. Surfactant therapy for bronchiolitis in critically ill infants. Cochrane Database Syst Rev. 2006;3:CD 005150.
- González de Dios J, Ochoa Sangrador C y Grupo de Revisión y Panel de Expertos de la Conferencia de Consenso del Proyecto aBREVIADo (BRonquiolitis-Estudio de Variabilidad Idoneidad y ADecuación). Conferencia de Consenso sobre bronquiolitis aguda (I): metodología y recomendaciones. An Pediatr (Barc). 2010;72: 221.e1-33.
- Ochoa Sangrador C, González de Dios J y Grupo de Revisión del Proyecto aBREVIADo (BRonquiolitis-Estudio de Variabilidad Idoneidad y ADecuación). Conferencia de Consenso sobre bronquiolitis aguda (II): epidemiología de la bronquiolitis aguda. Revisión de la evidencia científica. An Pediatr (Barc). 2010;72:222.e1-26.
- Ochoa Sangrador C, González de Dios J y Grupo de Revisión del Proyecto aBREVIADo (BRonquiolitis-Estudio de Variabilidad Idoneidad y ADecuación). Conferencia de Consenso sobre bronquiolitis aguda (III): diagnóstico en la bronquiolitis aguda. Revisión de la evidencia científica. An Pediatr (Barc). 2010;72:284.e1-23.
- González de Dios J, Ochoa Sangrador C y Grupo de Revisión del Proyecto aBREVIADo (BRonquiolitis-Estudio de Variabilidad Idoneidad y ADecuación). Conferencia de Consenso sobre bronquiolitis aguda (IV): tratamiento de la bronquiolitis aguda. Revisión de la evidencia científica. An Pediatr (Barc). 2010;72:285.e1-42.
- González de Dios J, Ochoa Sangrador C y Grupo de Revisión del Proyecto aBREVIADo (BRonquiolitis-Estudio de Variabilidad Idoneidad y ADecuación). Conferencia de Consenso sobre bronquiolitis aguda (V): prevención de la bronquiolitis aguda. Revisión de la evidencia científica. An Pediatr (Barc). 2010;72:353.e1-26.
- Ochoa Sangrador C, González de Dios J y Grupo de Revisión del Proyecto aBREVIADo (BRonquiolitis-Estudio de Variabilidad Idoneidad, Adecuación ADecuación). Conferencia de Consenso sobre bronquiolitis aguda (VI): pronóstico en la bronquiolitis aguda. Revisión de la evidencia científica. An Pediatr (Barc). 2010;72: 354.e1-34.
- González de Dios, Ochoa Sangrador C. Manejo diagnóstico y terapéutico de la bronquiolitis aguda. GuiaSalud. [En línea] [Consultado el 18/10/2010] Disponible en www.guiasalud.es.
- González de Dios J, Ochoa Sangrador C, y Grupo Investigador del Proyecto aBREVIADo (BRonquiolitis-Estudio de Variabilidad, Idoneidad y ADecuación). Estudio de variabilidad en el manejo de la bronquiolitis aguda en España en relación con la edad de los pacientes. An Pediatr (Barc). 2010;72:4-18.
- Figueras Aloy J, López Sastre J, Medrano López C, Bermúdez-Cañete Fernández R, Fernández Pineda L, Bonillo Perales A et al. Consenso multidisciplinar español sobre la profilaxis de la infección respiratoria pediátrica por virus respiratorio sincitial. An Pediatr (Barc). 2008;69:63-71.
- Castro-Rodríguez JA, Rodrigo GJ. Efficacy of inhaled corticosteroids in infants and preschoolers with recurrent wheezing and asthma: a systematic review with meta-analysis. Pediatrics. 2009;123:e519-25.
- Grupo de Hospitales Benazuza. Quimioprofilaxis con palivizumab en Andalucía. Resultados de la epidemia de VRS 2000-2001. An Esp Pediatr. 2002;56:293-7.
- Groothuis J, Bauman J, Malinoski F, Eggleston M. Strategies for prevention of RSV nosocomial infection. J Perinatol. 2008;28:319-23.
- Kimpen JL, Schaad UB. Treatment of respiratory syncytial virus bronchiolitis: 1995 poll of members of the European Society for Paediatric Infectious Diseases. Pediatr Infect Dis J. 1997;16:479-81.
- New grades for recommendations from the Canadian Task Force on Preventive Health Care. CMAJ. 2003;169:207-8.
- Atkins D, Best D, Briss PA, Eccles M, Falck-Ytter Y, Flottorp S et al. Grading quality of evidence and strength of recommendations. BMJ. 2004;328:1490.
- Guyatt GH, Oxman AD, Vist GE, Kunz R, Falck-Ytter Y, Alonso-Coello P et al. GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 2008;336:924-6.
- Guyatt GH, Oxman AD, Kunz R, Vist GE, Falck-Ytter Y, Schunemann HJ. What is “quality of evidence” and why is it important to clinicians? BMJ. 2008;336:995-8.
- Schunemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE et al. Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ. 2008;336:1106-10.
- Landau LI. Current pharmacological treatments for bronchiolitis are useless. The case for the con's. Paediatr Respir Rev. 2006;7(Suppl.1):S101-3.
CONFLICTO DE INTERESES
Los autores implicados en la elaboración de este documento han realizado una declaración explícita de los conflictos de intereses por escrito. No constan conflictos de intereses que puedan influir en el contenido de este documento.




